Cancerstamhet möter immunitet: från mekanism till terapi (del 1)
Jun 09, 2022
För mer information kontakta gärnadavid.wan@wecistanche.com
Cancerstamceller (CSC) är självförnyande celler som underlättartumörinitiering, främja metastaser och förbättramotstånd mot cancerterapi. Transkriptomiska analyser över många cancertyper har visat ett framträdande samband mellanstamhetochimmunsignaturer, vilket potentiellt innebär en biologisk interaktion mellan sådana kännetecken för cancer. Nya experimentella bevis har styrkt påverkan av CSC på immunceller, inklusive tumörassocierade makrofager, myeloidhärledda suppressorceller och T-celler, i tumörens mikromiljö och, ömsesidigt, betydelsen av sådana immunceller för att upprätthålla CSC stamness och dess överlevnad nisch. Denna översikt täcker de cellulära och molekylära mekanismerna bakom de symbiotiska interaktionerna mellan CSC och immunceller och hur sådanaheterotypisksignalering upprätthåller ett tumörfrämjande ekosystem och informerar om terapeutiska strategier som avlyssnar detta medberoende.

Klicka här för att lära dig mer om Cistanche
INTRODUKTION
Cancerstamcellsparadigmet (CSC) uppstod från studien avakut myeloid leukemi(AML), som identifierade en subpopulation av mindre differentierade CD34*/CD387-celler med stamcellsliknande förnyelsekapacitet och robust tumörinitierande förmåga (Lapi-dot et al, 1994). Cancerceller med dessa biologiska egenskaper har sedan dess upptäckts i praktiskt taget alla solida tumörer, inklusive melanom och cancer i hjärnan, bröst, tjocktarm, sköldkörtel, bukspottkörtel, prostata, lever, lunga, äggstockar, huvud och hals och mage (Turdo et al. ,2019). Den kliniska och biologiska betydelsen av CSC har förstärkts av en positiv korrelation mellan stamcellssignaturer och dålig överlevnad (Ben-Porath et al, 2008). Även om CSC:er delar egenskaper och ytmarkörer med normala stamceller (Turdo et al., 2019), bibehåller de förnyelsekapacitet via specifika förändrade signalvägar med gemensamma och unika mönster över många tumörtyper (Figur 1). Till exempel visar CSC:er för bröstcancer CD44 standardsplits iso-form (CD44s)-aktiverad blodplättshärledd tillväxtfaktorreceptor (PDGFR)/signalomvandlare och aktivator av transkription 3 (STAT3), gaffellåda C1 (FOXC1)-aktiverad sonisk igelkott ( SHH), och sfingosin-1-fosfat (S1P)/S1PR3-aktiverade NOTCH-vägar (Han et al, 2015; Hirata et al, 2014; Zhang et al, 2019b). Däremot CSC stamness i andra cancertyper, såsom gliom och tjocktarmscancer, mag- och prostatacancer, upprätthålls via CD133-medierad fosfatidylinositol-3-kinas (Pl3K)/proteinkinas B(AKT,leucinrikt G-protein- kopplad receptor 5(LGR5)-medierad WNT/-catenin och speckle-type POZ-protein (SPOP)-medierade NANOG-vägar (Morgan et al., 2018; Wang et al., 2010b, 2019a; Wei et al., 2013; Zhang et al., 2019c). Sådana CSC-associerade mönster motsäger en hög grad av biologisk komplexitet och tumörtypspecificitet.
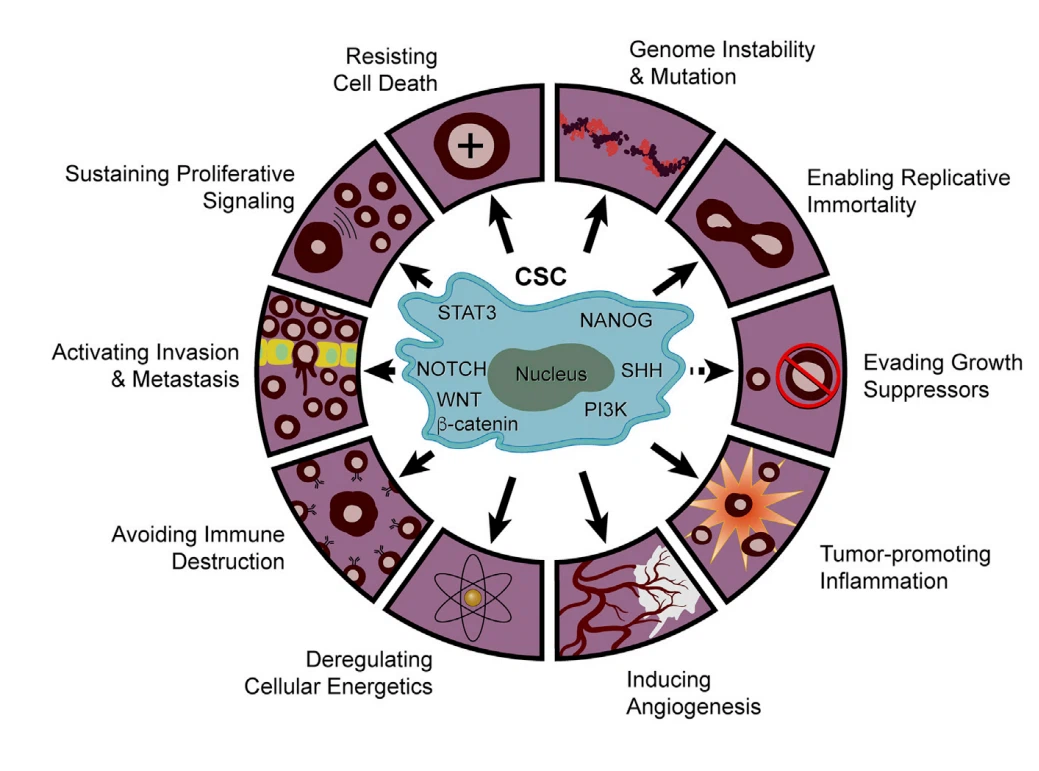
Kännetecknet för CSCs är väletablerade och inkluderar självförnyelse, klonal tumörinitieringskapacitet, klonal långsiktig återpopulationspotential och plasticitet mellan stam- och icke-stamtillstånd (Plaks et al., 2015). Denna plasticitet är särskilt relevant eftersom den gör det möjligt för CSC:er att anpassa sig och överleva inför terapeutiska störningar såväl som de ständigt föränderliga biologiska påfrestningarna i tumörmikromiljön (TME) genom hela tumörevolutionen (Agliano et al., 2017; Hatina, 2012; Müller et al., 2020; Plaks et al., 2015). Mekanistiskt har CSCs roll i tumörinitiering, metastasering och terapiresistens visat sig drivas av interaktioner mellancancercelleroch värdceller i TME (Ayob och Ramasamy, 2018; Plaks et al, 2015), där molekylerna och vägarna som driver CSC-biologin ofta driver flera cancerkännetecken (Figur 1). Till exempel relaterar den tumörinitierande förmågan hos CSCs till deras stamness driven av transkriptionsfaktorns könsbestämmande region Y-box 2 (SOX2), som också uppreglerar gener som styr cancerkännetecknen för proliferation, överlevnad och invasion (Boumahdi et al. ., 2014; Zhou et al, 2009). När det gäller metastasets kännetecken korrelerar stamcellssignaturer positivt med ökad metastatisk benägenhet (Ayob och Ramasamy, 2018); dessutom bidrar olika CSC-vägar och associerade biologiska processer till varje steg i den metastatiska processen - från spridning till metastatisk nischbildning till avlägsen organtillväxt - genom att inducera epitelial-mesenkymal övergång (EMT, stimulera exosomproduktion från myeloida celler och uppreglera nischhärledda faktorer , såsom insulinliknande tillväxtfaktor-1 (IGF-1) respektive interleukin (L)-6 (Agliano et al., 2017; Ayob och Ramasamy, 2018; Shiozawa et al. Experimentella och kliniska bevis visar faktiskt att CSCs i primära tumörer sprider och koloniserar distala platser (de Sousae Melo et al., 2017) och att deras placering vid den invasiva fronten korrelerar negativt med patientöverlevnad (Kodamaet al., 2017) Slutligen, med avseende på terapiresistens, förändrar CSC-vägar signalmolekyler som styr läkemedelsmetabolism (t.ex. högt uttryck av ATP-bindande kassetttransportproteiner som ökarläkemedelsutflödehastighet), EMT (t.ex. ökad SOX2, oktamerbindande transkriptionsfaktor 4 [OCT4] och NANOG-uttryck) och metabolisk omprogrammering (t.ex. förbättrad glukostransportör 1, oxidativ fosforylering och reaktiv syreaktivitet; Ayob och Ramasamy, 2018 ). Den fenotypiska plasticiteten hos CSC kan bidra till ytterligare cancerkännetecken via deras förmåga att transdifferentiera till peri-cyter, endotelceller och fibroblaster, vilket bidrar till tumörangiogenes, stamcellsnischutveckling och inflammation (Figur 1; Cheng et al, 2013; Dongre och Weinberg, 2019; Huet al., 2016; Nair et al., 2017; Ricci-Vitiani et al., 2010; Wang et al., 2010a). Denna plasticitet återspeglas också i förmågan hos "differentierade" cancerceller att återadoptera ett omoget CSC-tillstånd, en dedifferentieringsprocess som kan stimuleras av signaler som emanerar från TME, inklusive tumörassocierade makrofager (TAM), myeloidhärledd suppressor celler (MDSC), T-celler, cancerassocierade fibroblaster (CAF) och andra immunceller (Plaks et al., 2015). Mest anmärkningsvärt är att den starka CSC-immuncellskopplingen bevisades av opartiska profileringsstudier, som visade en stark negativ korrelation mellan cancercellers stam- och antitumörimmunitetssignaturer över 21 typer av solida tumörer (Miranda et al, 2019). Specifikt var ökad stam-ness associerad med minskade anti-cancer-immunceller, inklusive CD8 plus T-celler, naturliga mördarceller (NK) och B-celler, och förbättrad polarisering av infiltrerande makrofager (Miranda et al, 2019). På liknande sätt har cancergenomatlasen (TCGA) och vävnadsmikroarray-analyser avslöjat att cancercellers stam-ness korrelerar negativt med aktiverade CD4 plus och CD8 plus T-celler i solida tumörer (Hou et al., 2019; Malta et al, 2018).

Dessa i silico-fynd i human cancer stämmer väl överens med nya experimentella fynd från studier av olika musmodeller av human cancer. Det har visat sig att andelen CSCs i melanom är beroende av den specifika immunkomprometterade musstammen som används, vilket tyder på en viktig roll för immunsystemet i regleringen av CSCs (Quintana et al., 2008). Å andra sidan kan CSCs forma en specifik TME genom deras reglering av immunceller. Till exempel korrelerar uttrycket av CSC-markör och regulator dubbelkortinliknande kinas 1 (Westphalen et al., 2014) positivt med ett överflöd av TAM och regulatoriska T-celler (T-reg-celler) och förhöjt uttryck av faktorer som hämmar CD8 plus Tcell aktivitet (Wu et al, 2020). CKLF-liknande MARVEL transmembrandomän-innehållande 6, som uttrycks på cancercellplasmamembran, kan förbättra CSC stamness via WNT/-catenin pathway, undertrycka antitumörimmunitet via programmerad dödligand 1 (PD-L1) uppreglering, och minska CD8* och CD4* T-celler i många typer av cancer, inklusive skivepitelcancer i huvud och hals (SCCHN) (Chen et al., 2020a), melanom och bröstcancer (Burr et al, 2017; Mezzadraet al. ,2017). Fett-massa- och fetmaassocierat protein (FTO) är am grad A demetylas och överuttryckt i AML. Hämning av FTO försämrar stamceller från leukemi och omprogrammerar immunsvaret genom att undertrycka immunkontrollpunktsgener, såsom LILRB4 (leukocyt-immunoglobulinliknande receptorunderfamilj B-medlem 4), vilket gör att AML-celler sensibiliseras för T-cellsmedierad cytotoxicitet (Suet al, 2020). På liknande sätt avslöjade encelliga RNA-sekvensanalyser (RNA-seq) av AML en subpopulation av stamliknande AML-celler som samuttrycker stamness-relaterade och myeloid-primande gener (van Galen et al, 2019). Dessutom kan CSC-härledda exosomer, som överför last mellan celler (Mathieu et al, 2019), förbättra överlevnaden av suppressiva neutrofiler för att främja tillväxt av tjocktarmscancer (Hwang et al, 2019). Denna delade stam- och immuntranskriptionsprofil överensstämmer med det senaste fyndet att avsaknaden av naturliga mördargrupp 2-medlems-Dligander, som definierar leukemi-stamceller, bidrar till deras selektiva flykt från NK-cellmedierad immunövervakning (Paczulla et al., 2019). Förutom dessa immunceller är CAF och deras interaktioner med CSC också viktiga förtumörbildningochterapiresistens(Chan et al, 2019). Tillsammans belyser dessa fynd en intim koppling mellan molekylerna och mekanismerna som styr CSC-biologi och tumörimmunitet över många tumörtyper.
Sammanfattningsvis understryker ökande translationella och experimentella bevis de otaliga interaktionerna och sammanflätade tumörbiologiska rollerna för CSCs och immunceller, särskilt myeloidceller (TAMs och MDSCs) och T-celler. Denna recension sammanfattar den nuvarande kunskapen om molekylär överhörning och den funktionella inverkan av dessa symbiotiska interaktioner på kännetecknen för cancer. När det gäller myeloidceller lyfter vi fram TAM och MDSC individuellt, även om de delar samma ursprungscell och liknande funktioner för att undertrycka T-cellsmedierad antitumörimmunitet (Engblom et al., 2016). Dessa framväxande insikter ger en färdplan för utvecklingen av nya anti-cancer terapeutiska strategier som stör denna dynamiska krets i specifika tumörtyper.

CSC-TAM Crosstalk
Inverkan av CSCs på makrofagbiologi
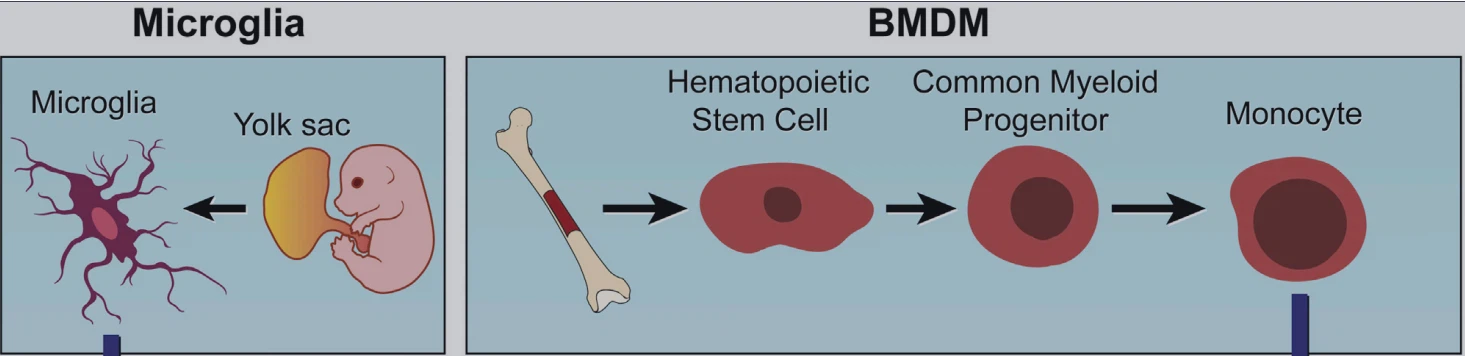
Faktorer som utsöndras av olika celltyper i TME, inklusive CSC, är kända för att rekrytera och polarisera TAM (Chen et al., 2017, 2019a, 2020b; Colegio et al, 2014). Dessa TAM kommer från benmärgshärledda makrofager (BMDM) och lokala vävnadsresidenta makrofager (t.ex. mikroglia i hjärnan, Kupffer-celler i levern och alveolära makrofager i lungan), som härstammar från hematopoetiska stamceller och stamceller sådd i embryonala vävnader (t.ex. gulesäcken för mikroglia och fosterlevern för Kupffer-celler respektive alveolära makrofager) (Figur 2; Pathria et al., 2019). TAM-rekrytering drivs av en mängd olika kemokiner, inklusive CC-motiv kemokin ligand 2(CCL2), CCL3, CXC-motiv kemokinligand 14(CXCL14) och lysyloxidas(LOX), som utsöndras av cancerceller, makrofager och andra stromaceller i TME (Chen et al., 2019a; Pathria et al. al., 2019; Wei et al., 2020. Allt fler bevis visar att CSC också bidrar till infiltrationen av makrofager och mikroglia via distinkta molekyler och mekanismer i olika cancerformer (Figur 2; Tabell 1). Observera att några av dessa kemokiner är specifikt producerat av CSCs, som hög belyser en unik roll för CSC: er i regleringen av TAM-infiltration. Till exempel uttrycks och utsöndras periostin (POSTN) företrädesvis av CSCs i glioblastom (GBM) och kolangiokarcinom (CCA), som i sin tur rekryterar BMDM genom bindning med xvB3-integrin (Zeng et al, 2018; Zhou et al., 2015).

Genetiska och epigenetiska förändringar i CSCs reglerar kemokinproduktionen. Till exempel uppreglerar PTEN-brist eller AKT-överuttryck i GSCs och neurala stamceller LOX och CXCL12B, som rekryterar TAMs genom 1 integrin (Chen et al., 2019a) och CXC-motiv kemokinreceptor 4 (CXCR4) (Chia et al., 2018), respektive. Optiska GSC isolerade från Nf1loxneo; GFAP-Cre låggradig gliommusmodell utsöndrar CX3CL1 och CCL5 för att rekrytera mikroglia, och denna effekt förstärks ytterligare av förlusten av Pten (Guo et al, 2019b). På liknande sätt kan F1-brist i humana GSC främja infiltrationen av makrofager och mikroglia, även om de NF1-reglerade kemokinerna inte är kända (Wang et al, 2017). I många tumörtyper, amplifiering av epidermal tillväxtfaktorreceptor (EGFR) och mutation kan främja CSC-stammighet och makrofagrekrytering (An et al, 2018; McCann et al, 2018; Rutkowska et al, 2019). Vid levercancer aktiverar EGFR/AKT-aktivering det ja-associerade protein(YAP)/TEA-domänfamiljemedlemmen (TEAD) transkriptionsfaktorkomplexet i CSCs, vilket i sin tur uppreglerar makrofagrekryteringsfaktorerna CCL2 och makrofagkolonistimulerande faktor (M-CSF) (Guo et al.2017). Vid icke-småcellig lungcancer (NSCLC), ökar ökat ubiquitin-specifikt proteas 17, ett deubiquitinas som krävs för trafficking och onkogen aktivitet av mutant EGFR (McCann et al., 2018), cancercellers stamness, vilket i sin tur uppreglerar makrofaginfiltration genom att ökad produktion av cytokiner, inklusive tumörnekrosfaktor (TNF)-a, IL-1 och IL-6 (Lu et al., 2018). Vid blåscancer främjar funktionsförlustmutationer av den histonmodifierande genen lysin (K)-specifikt demetylas 6A (KDM6A) CSC stamness och utsöndring av IL-6 och CCL2, vilket i sin tur ökar makrofagrekryteringen (Kobatake et al. al., 2020). I GBM förbättrar cirkadiska rörelsecykler kaput (CLOCK), en epigenetisk och dygnsrytmregulator som förstärks i 5 procent av fallen, GSC stamness och utsöndring av det kemokine olfactomedin-liknande proteinet 3 (OLFML3), som rekryterar mikroglia till TME ( Chen et al., 2020b). Slutligen, caveat emptor, även om många studier har fastställt involveringen av CSC-härledda faktorer i makrofaginfiltration, har det omvända också observerats på grund av den specifika CSC-genotypen och dess unika TME. Till exempel hämmar TP53-muterade och cisplatinresistenta CSC från lungcancer makrofaginfiltration i TME (Xu et al., 2019).

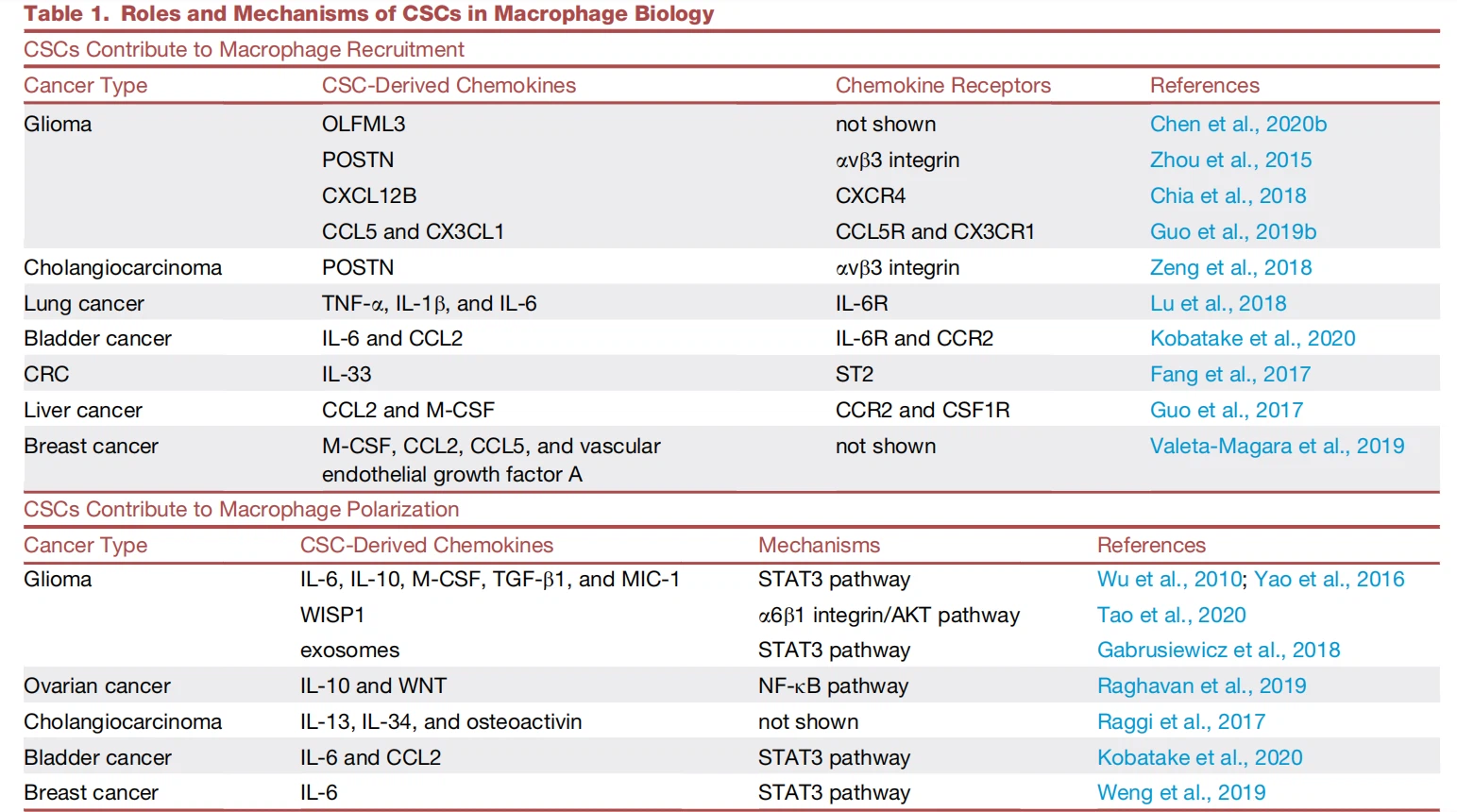
Förutom att stimulera TAM-rekrytering kan CSCs påverka det biologiska tillståndet hos dessa makrofager. Makrofager är kända för att uppvisa ett spektrum av fenotyper, allt från en antitumör till protumörfenotyp (tidigare kallad M1 och M2; Pathria et al., 2019). När väl makrofager infiltrerar in i tumörer genomgår de vanligtvis polarisering mot en protumörfenotyp, en process som drivs av kemokiner (t.ex. IL-4 och IL-13) och metaboliter (t.ex. laktat), som är härledda från både cancerceller och värdceller i TME (Chen et al., 2017; Colegio et al., 2014; Qian och Pollard, 2010). Flera bevis visar att CSC ytterligare kan provocera anti-till protumor polarisering av makrofager. Först, vid samodling med CSCs, uppregleras protumörmakrofagmarkörer (t.ex. CD206, IL-10 och arginas 1), medan antitumörmakrofagmarkörer (t.ex. TNF-, kväveoxidsyntas 2 [ NOS2] och CD86) är nedreglerade (Deng et al, 2015). För det andra kan CSCs utsöndra olika lösliga faktorer som inducerar polarisering mot en protumörfenotyp (Figur 2; Tabell 1). Till exempel är Wnt-inducerat signalprotein 1(WSP1) föredraget utsöndrat av GSCs i GBM, vilket främjar överlevnaden av protumör-TAM genom aktivering av x6 1-integrin/AKT-vägen på makrofager (Tao et al, 2020). På liknande sätt kan CSC-härledda IL-6 och IL-10 förvränga TAMs mot en protumörfenotyp i äggstockscancer (Raghavan et al, 2019), blåscancer (Kobatake et al, 2020), GBM ( Wu et al, 2010; Yao et al., 2016) och bröstcancer (Weng et al, 2019). Förutom utsöndrade faktorer frigör GSC exosomer som innehåller eukaryot initieringsfaktor 2, däggdjursmålet för rapamycin (mTOR) och efrin B-signalvägar som är hem för monocytmembranet och främjar makrofag protumörpolarisering (Gabrusiewiczet al, 2018). Slutligen, i samband med tumörnekros i GBM, kan GSC-härledda partiklar, definierade som "autoschizis-liknande produkter", uppslukas av TAMs, som i sin tur uppreglerar L-12 för att polarisera dessa TAMs mot en antitumör fenotyp (Tabu et al, 2020). Således utsöndrar CSC: er en mängd olika produkter som uppmuntrar makrofagpolarisering.
