Kapitel 1: Njurskydd med SGLT2-hämmare: Effekter vid akuta och kroniska njursjukdomar
Jun 17, 2022
För mer information. Kontakttina.xiang@wecistanche.com
Abstrakt
Syftet med granskningen: Den här recensionen ger en kritisk narrativ utvärdering av nya bevis för att natrium-glukos co-trans-porter-2(SGLT2)-hämmare utövar nefroprotektiva effekter hos personer med typ 2-diabetes.
Nya fynd SGLT2-hämmarklassen av glukossänkande medel har nyligen visat gynnsamma effekter för att minska uppkomsten och progressionen av njurkomplikationer hos personer med och utan diabetes. Randomiserade kliniska prövningar och observationsstudier från den verkliga världen, mest involverade patienter med typ 2-diabetes, har noterat att användningen av en SGLT2-hämmare kan bromsa nedgången i glomerulär filtrationshastighet (GFR), minska uppkomsten av mikroalbuminuri och sakta ner eller vända progression av proteinuri.
Sammanfattning: De nefroprotektiva effekterna av SGLT2-hämmare är klasseffekter som observerats med vart och ett av de godkända medlen hos personer med normal eller nedsatt GFR. Dessa effekter observeras också hos icke-diabetes, magra och normotensiva individer, vilket tyder på att mekanismerna sträcker sig bortom de glukossänkande, viktsänkande och blodtryckssänkande effekterna som åtföljer deras glukosuriska verkan hos diabetespatienter. En nyckelmekanism är en tubuloglomerulär återkoppling där SGLT2-hämmare orsakar att mer natrium passerar längs nefronet: natriumet avkänns av makulaceller som verkar via adenosin för att dra ihop afferenta glomerulära arterioler, och därigenom skydda glomeruli genom att minska det intraglomerulära trycket. Andra effekter av SGLT2-hämmare förbättrar tubulär syresättning och metabolism och minskarnjurinflammationoch fibros. SGLT2-hämmare har inte ökat risken för urinvägsinfektioner eller risken förakut njurskada. Införandet av en SGLT2-hämmare hos patienter med mycket låg GFR uppmuntras dock inte på grund av en initial nedgång i GFR, och det är klokt att avbryta behandlingen om det finns en akut renal händelse, hypovolemi eller hypotoni.
Nyckelord: Natrium-glukos co-transportör-2(SGLT2)-hämmare. Diabetisk njursjukdom. Kronisk njursjukdom. Albuminuri. Akut njursjukdom
Klicka här för att lära dig vad cistanche används till
Introduktion
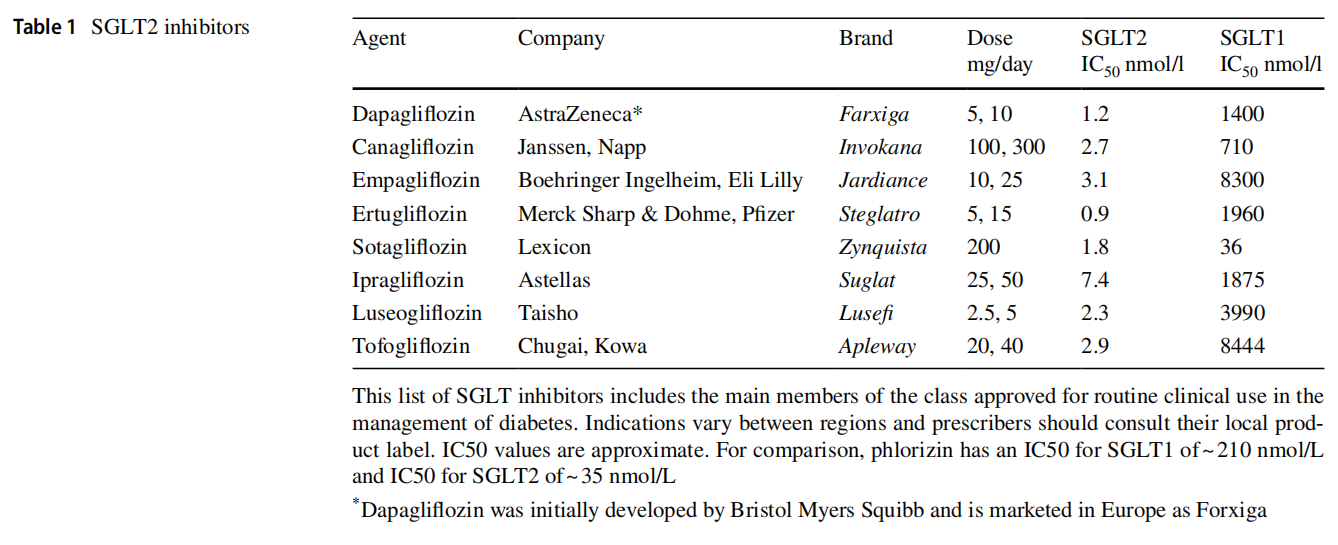
Natrium-glukos co-transporter-2(SGLT2)-hämmare är glukossänkande medel som eliminerar överskott av glukos genom en glukosurisk effekt genom att minska glukosreabsorptionen från njurfiltratet[1,2e]. Sedan introduktionen av den första SGLT2-hämmaren 2012 har klassen vuxit till att omfatta kanagliflozin, dapagliflozin, empagliflozin och ertugliflozin i Europa och Amerika, med ytterligare medlemmar i klassen som har etablerat sig i andra regioner (tabell 1). Även om det är utformat för att minska hyperglykemi och hjälpa kroppsviktskontroll vid typ 2-diabetes, erkänns nu ytterligare terapeutiska möjligheter för SGLT2-hämmare för att åtgärda kardio-renala komplikationer och samsjukligheter av typ 2-diabetes.
Initiala farhågor om SGLT2-hämmare fokuserade på möjliga skadliga effekter på njursystemet, särskilt ökade urinvägsinfektioner, försämrad blåshälsa och förvärrande akut njurskada [3]. Det noterades också med oro att administrering av en SGLT2-hämmare orsakade en tillfällig nedgång i glomerulär filtrationshastighet och orsakade ihållande minskningar i plasmavolym och blodtryck. Dock observationer underkardiovaskuläraresultatförsök och verkliga studier har identifierat potentiellt fördelaktiga effekter av SGLT2-hämmare för att minska risken för uppkomst och progression av flera kardiovaskulära tillstånd och bevaranjurfunktion.
Denna narrativa översikt, som är baserad på en omfattande litteraturöversikt (ruta 1), erbjuder en kritisk bedömning av framväxande bevis för de nefroprotektiva egenskaperna hos SGLT2-hämmare. Ruta 1 Litteratursökningsstrategi och urvalskriterier. MEDLINE, PubMed och Google Scholar söktes efter artiklar publicerade mellan januari 2010 och mars 2021 med termerna "natrium-glukostransportörhämmare, "SGLT2-hämmare och de generiska namnen på individuella SGLT2-hämmare i kombination med termen "njursjukdom", " akut njurskada, 'kronisk njursjukdom', 'njurfunktion', 'diabetes och 'typ 2-diabetes. Studier valdes ut om de utfördes i mänskliga populationer och/eller beskrev kliniskt relevanta mekanismer, publicerade på engelska och gav övertygande information. Fallrapporter, ledare, riktlinjer och prekliniska studier inkluderades när de erbjöd information eller tolkningar som inte var tillgängliga i andra källor.

SGLT2-hämning
Utvecklingen av SGLT2-hämmare kan spåras från 1800-talets observationer att glukosiden florizin orsakade glukosuri [4]. Prekliniska studier på 1980-talet visade att florizinbehandling kunde kontrollera hyperglykemi hos delvis pankreatektomiserade råttor, men klinisk tillämpning väntade på syntetiska analoger som undvek intestinal glukosidasnedbrytning och erbjöd förbättrad styrka och selektivitet för att hämma SGLT2 snarare än SGLT1[5,6.
SGLT2 finns nästan uteslutande i de luminala membranen hos epitelceller som täcker de första och andra segmenten av de proximala tubuli, där det förmedlar återabsorption av det mesta (typiskt mer än eller lika med 90 procent) av filtrerat glukos (Fig. 1). SGLT1 i de luminala membranen hos celler som kantar det tredje (raka) segmentet av de proximala tubuli förmedlar återabsorption av låga koncentrationer av glukos som finns kvar i tubuli. SGLT1 är mest förekommande i de apikala membranen hos enterocyter där det förmedlar glukosupptag från tarmens lumen. För att undvika störning av den intestinala absorptionen av glukos har hög selektivitet för hämning av SGLT2 i allmänhet föredragits (tabell 1). Kanagliflozin utövar dock en viss undertryckning av SGLT1, och sotagliflozin är en SGLT1/2-hämmare: båda dessa medel kan fördröja tarmabsorptionen av glukos innan de absorberas eller bryts ned, vilket underlättar prandial glykemisk kontroll. Mängderna av dessa medel som absorberas och exponeras för njuren, samtidigt som de hämmar SGLT2, är otillräckliga för att ha någon substantiell hämmande effekt på SGLT1 i de proximala tubuli.
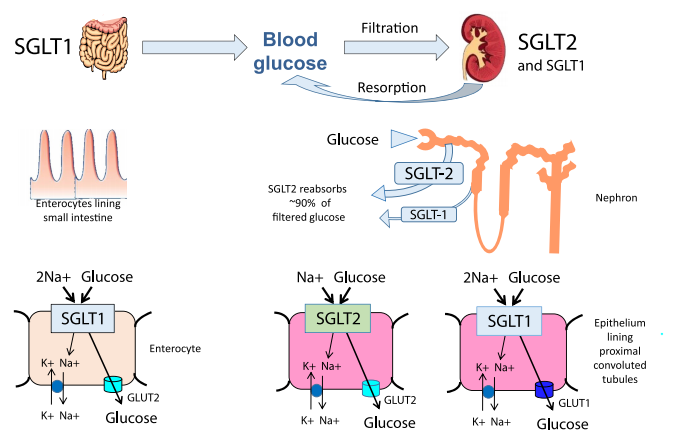
Fig. 1 Nyckelverkningsställen för natrium-glukos co-transportör (SGLT)-hämmare. SGLT2 (kodas av den lösta bärargenen slcSa2) uttrycks nästan uteslutande i det luminala membranet hos epitelceller som täcker de första och andra segmenten av de proximala tubuli. Det är en samtransportör med hög kapacitet som verkar med en natrium-glukosstökiometri på 1:1 för att mediera reabsorptionen av det mesta av den filtrerade glukosen. SGLT1 (kodas av slcSal) uttrycks i det luminala membranet hos celler som kantar det tredje (raka) segmentet av de proximala tubuli. Det verkar med en natrium-glukosstökiometri på 2:1 och har en lägre kapacitet men högre affinitet än SGLT2 för att återvinna låga koncentrationer av glukos som finns kvar i tubuli. SGLT1 uttrycks brett och förekommer mest i de apikala membranen av enterocyter i tunntarmen där det förmedlar glukosupptag från tarmens lumen. Båda transportörerna är sekundära aktiva symportörer som är beroende av natriumgradienten som skapas av Na plus -K十-ATPas-pumpar i de basolaterala membranen som sänker den intracellulära natriumkoncentrationen. Glukos som tas upp av natrium-glukos-samtransportörer in i proximala tubuliceller och enterocyter elimineras över de basolaterala membranen och in i interstitium via underlättande glukostransportörer (t.ex. GLUT1 och GLUT2)
Hyperglykemi av diabetes innebär att större än normala mängder glukos filtreras från glomeruli in i de proximala tubuli, och ökade mängder reabsorberas, i samband med en kompensatorisk uppreglering av SGLT2 och SGLT1 uttryck [9]. Ändå överskrids ofta njurtröskeln för glukos, och glukosurin förstärks av SGLT2-hämmare som verkar genom reversibel kompetitiv hämning utan att själva transporteras [2e]. De binder till co-transportörerna vid den luminala ytan med större affinitet än glukos och med en uppehållstid på flera minuter. Således kan en trivial (terapeutisk) koncentration av en SGLT-hämmare i filtratet förhindra återabsorption av en stor (upp till cirka 100 g/dag) mängd filtrerat glukos. Även om SGLT2-hämmare sänker njurtröskeln för glukos, är deras glukosuriska effekt självbegränsande så att de inte medför risken för kliniskt signifikant hypoglykemi. Detta beror på att, eftersom hämmaren ökar glukosurin, sänker detta blodsockret så att mindre glukos filtreras, och tillräckligt med aktiva (ohämmade) transportörer kan sedan reabsorbera (nästan all denna mindre mängd glukos, vilket förhindrar blodsockret från att sjunka under euglykemi).
Glukossänkning och viktsänkning Aktiviteten hos SGLT2-hämmare är oberoende av insulinstatus, dvs oförminskad av insulinresistens eller absolut insulinbrist, vilket möjliggör glukossänkning vid typ 2- och typ 1-diabetes. Beroende på omfattningen av hyperglykemi innebär att glukossänkande effekt är större hos individer med högre blodglukoskoncentrationer och är särskilt användbar för att minska prandiala glukosexkursioner. Metaanalyser av minskningen av HbAlc med SGLT2-hämmare vid typ 2-diabetes har konsekvent noterat minskningar på cirka 0,5 till 1 procent (6-11 mmol/mol) från en baslinje på cirka 8 procent (64 mmol/ mol)[10-12]. Eftersom SGLT2-hämmare har en annan verkningsmekanism än andra glukossänkande medel kan de användas i kombination med andra medel inklusive insulin, och kan ofta minska mängden insulin som krävs vid typ 2 och typ 1 diabetes [13,14]. SGLT2-hämmare kan dock inte ersätta behovet av tillräckligt med insulin för att upprätthålla grundläggande metaboliska krav. Överreduktion av (eller fördröjning av att starta) insulin är vanligtvis orsaken till atypisk (euglykemisk) diabetisk ketoacidos (DKA) där DKA uppträder utan hyperglykemi och ibland avslöjar att en diagnos av typ 2-diabetes är typ 1[15].
In clinical trials with type 2 diabetes patients, the weight-reducing effect of SGLT2 inhibitors has typically been around 3 kg, leveling out by 6-12 months, although 'real-world observational studies have often noted reduc-tions>6 kg som fortsätter längre än ett år. Sjunkande vikt tillskrivs generellt kaloriförlust genom glukosuri. Tabell 2 Stora randomiserade kontrollerade kardiovaskulära resultatstudier (CVOT) där njurhändelser mättes under behandling av typ 2-diabetespatienter med en SGLT2-hämmare. BMI body mass index, CVD kardiovaskulär sjukdom, eGFR uppskattad glomerulär filtrationshastighet, GLD-glukossänkande läkemedel, MACE allvarlig kardiovaskulär händelse (kardiovaskulär död, icke-fatal hjärtinfarkt eller stroke), hjärtinfarkt med hjärtinfarkt, UACR-urinalbumin-kreatininförhållande. Värden för MACE, CV-död, MI, stroke, hjärtsvikt, alla dödsfall och njurkomposit är riskkvoter med 95 procents konfidensintervall.*Njurkompositer varierade mellan försöken: EMPA-REG minskar fettmassan, även om minskad plasmavolym också kan bidra [16, 17].
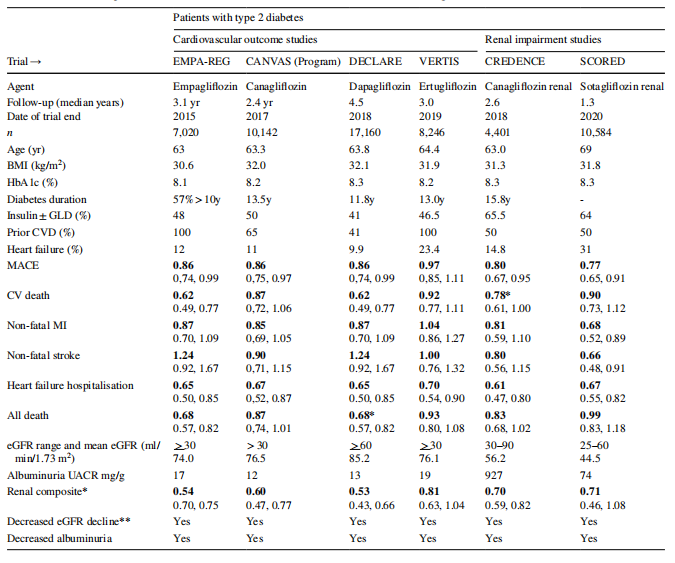
Table2 Large randomized controlled cardiovascular outcome trials(CVOTs)in which renal events were measured during treatment of type 2 diabetes patients with an SGLT2 inhibitor.BM7 body mass index, CVD cardiovascular disease,eGFR estimated glomerular filtration rate, GLD glucose-lowering drug, MACE major adverse cardiovascular event(cardiovascular death, non-fatal myocardial infarction or stroke), MI/ myocardial infarction, UACR urine albumin-creatinine ratio. Values for MACE, CV death, MI, stroke, heart failure, all deaths, and renal composite are hazard ratios with 95% confidence intervals.*Renal composites varied between trials: EMPA-REG OUTCOMES.doubling of serum creatinine,eGFR≤45 ml/min/1.73 m², start renal replacement, renal death; CANVAS PROGRAM,>40% decrease in eGFR, start renal replacement, renal death: DECLARE,>40% decrease in eGFR,end-stage kidney disease, renal or CV death; VERTIS, doubling of serum creatinine, start renal replacement, renal death; CREDENCE, double serum creatinine,end-stage kidney disease, renal death or CV death: SCORED, sustained (>30 days)decrease of≥50%in eGFR, dialysis, and renal transplantation or sustained (>30 dagar)eGFR av<15 ml/min/1.73="" m².**decline="" in="" the="" long-term="" rate="" of="">

Kardiovaskulära effekter
Beyond glucose-lowering and weight lowering, SGLT2 inhibitors have consistently reduced blood pressure (systolic by 3-5 mmHg and diastolic by 2-3 mmHg)during clinical trials without causing hypotension [18]. SGLT2 inhibitors have also OUTCOMES, doubling of serum creatinine, eGFR≤45 ml/min/1.73 m², start renal replacement, renal death; CANVAS PROGRAM,>40% decrease in eGFR, start renal replacement, renal death: DECLARE,>40% decrease in eGFR, end-stage kidney disease, renal or CV death; VERTIS, doubling of serum creatinine, start renal replacement, renal death; CREDENCE, double serum creatinine,end-stage kidney disease, renal death or CV death; SCORED, sustained(>30 days)decrease of≥50% in eGFR, dialysis, and renal transplantation or sustained(>30 dagar)eGFR av<15 ml/min/1.73="" m².**declinein="" long-term="" rate="" of="" egfr="" consistently="" reduced="" the="" risk="" of="" new="" heart="" failure="" and="" worsening="" of="" existing="" heart="" failure="" during="" clinical="" trials="" (table2).="" the="" benefit="" is="" evident="" within="" a="" few="" weeks="" of="" starting="" an="" sglt2="" inhibitor,="" occurs="" in="" people="" with="" and="" without="" diabetes,="" and="" is="" independent="" of="" the="" extent="" of="" effects="" on="" glucose,="" weight,="" or="" blood="" pressure[19-21].="" the="" improved="" prognosis="" for="" heart="" failure="" is="" also="" independent="" of="" age="" and="" is="" not="" significantly="" affected="" by="" the="" presence="" of="" ckd,="" albuminuria,="" or="" concomitant="" use="" of="" antihypertensive="" therapies.="" studies="" in="" which="" ejection="" fraction="" was="" quantified="" have="" mostly="" involved="" patients="" with="" reduced="" ejection="" fraction(hfref),="" but="" there="" is="" emerging="" evidence="" that="" sglt2="" inhibitors="" can="" also="" benefit="" those="" with="" preserved="" and="" mid-range="" ejection="" fraction.[22-25].measures="" of="" atherosclerotic="" cardiovascular="" disease(cardiovascular="" deaths,="" non-fatal="" myocardial="" infarction,="" and="" stroke)="" have="" also="" been="" reduced="" in="" some="" studies="" with="" sglt2="" inhibitors:="" these="" are="" reviewed="" in="" detail="" elsewhere="" in="" the="" context="" of="" the="" reciprocating="" interrelationships="" of="" heart="" and="" kidney="">
Diabetes njursjukdom
Alla typer av diabetes är förknippade med en ökad risk för nedsatt njurfunktion (kallas diabetisk nefropati eller diabetisk njursjukdom (DKD)). Detta känns vanligtvis igen av en progressiv kronisk njursjukdom (CKD) med en uppskattad glomerulär filtrationshastighet (eGFR)<60 ml/min/1.73m²that="" can="" be="" attributed="" to="" diabetes="" [28].="" the="" condition="" may="" be="" accompanied="" by="" micro-(uacr="" 30-300="" mg/g)or="" macro-(="">300 mg/g) albuminuria, often with an underlying glomerulopathy of thickened capillary basement membranes, diffuse mesangial sclerosis, and nodular sclerosis. The normal age-related rate of decline in eGFR(~1 ml/min/l.73m²per year wheneGFR>60 ml/min/1,73 m²) fördubblas vanligtvis vid typ 2-diabetes med CKD och kan överstiga 3 ml/min/1,73 m² per år hos individer med makroalbuminuri [29]. Observationsstudier tyder på att 20-40 procent av personer med typ 2-diabetes drabbas av en eGFR<60 ml/min/1.73m²,="" mostly="" amongst="" older="" patients="" and="" those="" with="" poor="" glycaemic="" control.="" type="" 2="" diabetes="" is="" also="" a="" major="" cause="" of="" end-stage="" kidney="" disease(eskd)="" requiring="" renal="" replacement="" therapy="">
Konventionella behandlingar (främst sträng kontroll av blodtrycket med ACE-hämmare eller ARB och intensiv blodsockerkontroll) minskar utvecklingen av DKD, men de har inte kunnat stoppa sjukdomsprogression. En framväxande mängd bevis tyder nu på att SGLT2-hämmare kan skydda mot uppkomsten av DKD och bromsa sjukdomsprogression oberoende av och additivt till blockad av renin-angiotensin-aldosteronsystemet (RAAS).

Njursjukdom och användning av SGLT2-hämmare
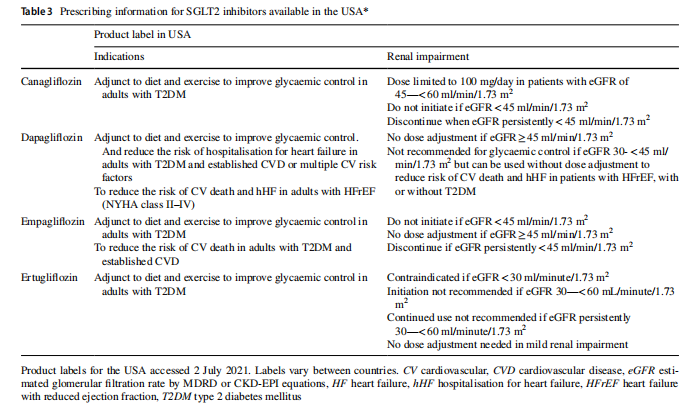
Eftersom en minskning av GFR minskar mängden glukos som levereras till de proximala tubuli, minskar den glukosuriska effekten (och därmed den antihyperglykemiska effekten) av SGLT2-hämmare ungefär i linje med en minskning av GFR. Följaktligen definierar produktetiketterna för SGLT2-hämmare GFR-värden under vilken det rekommenderas att inte påbörja eller fortsätta behandlingen [35-38]. Med ökande insikt om att SGLT2-hämmare inte äventyrar njursäkerheten och erbjuder kardio-njurfördelar, har indikationerna och tillåtna eGFR-intervall utökats (tabell 3) och varierar mellan länderna.
Renala ändpunkter
Insikten om att SGLT2-hämmare kunde förändra förloppet av diabetisk njursjukdom grumlades initialt av korttidsobservationer fokuserade på den initiala nedgången i eGFR. Denna sänkning är vanligtvis cirka 5 ml/min/1,73 m², den når en nadir inom 1-2 veckor och går långsamt tillbaka mot förbehandlingsvärdena under de kommande 3-9 månaderna(Fig.2). Bevis från långtidsstudier av typ 2-diabetes, särskilt de kardiovaskulära utfallsprövningarna (CVOT) som beskrivs nedan, visade att eGFR därefter minskade långsammare med användning av en SGLT2-hämmare än hos placebobehandlade patienter och att albuminuri var mindre allvarlig.

Fördefinierade sekundära effektmått i CVOT:erna utvärderade olika individuella och sammansatta mått på njurfunktionen som inkluderade progression av albuminuri (indikerat med UACR), fördubbling av serumkreatinin, minskning av eGFR (till antingen<45><60 ml/min/1.73m²),="" end-stage="" kidney="" disease,="" kidney-related="" death="" or="" renal="" replacement="" therapy="" (dialysis="" or="" transplantation).="" because="" the="" composites="" and="" the="" patient="" populations="" differed="" between="" the="" trials,="" direct="" comparisons="" are="" necessarily="" cautious.="" however,="" each="" of="" the="" composites="" that="" included="" a="" measure="" of="" the="" rate="" of="" decline="" in="" egfr="" noted="" a="" significant="" benefit="" of="" treatment="" with="" an="" sglt2="" inhibitor:="" for="" example,="" a="" decrease="" in="" adverse="" events="" by≥30%(table="" 2).="" also,="" the="" individual="" renal="" parameters="" assessed="" in="" the="" cvots="" showed="" either="" significant="" reductions="" or="" non-significant="" numerical="" reductions="" in="" the="" occurrence="" of="" adverse="" renal="" events,="" bearing="" in="" mind="" that="" the="" studies="" were="" not="" powered="" for="" renal="">
Large Randomised Trials in Type 2 Diabetes In the EMPA-REG OUTCOME trial, the renal composite (doubling of serum creatinine,eGFR≤45 ml/min/1.73 m², initiation of renal replacement therapy or death from kidney disease) was reduced by 46% in the groups receiving empagliflozin [39,40]. After the initial dip in eGFR, there was a slight annual decline in eGFR with the use of empagliflozin (0.19±0.11 ml/min/1.73 m²/year; mean±standard error)compared with a more rapid decline in the placebo group (1.67±0.13 mL/min/1.73 m²/year). Progression to macroalbuminuria (UACR>300 mg/g) minskade med 38 procent med användning av empagliflozin, och det fanns också signifikanta minskningar av antalet patienter med en fördubbling av serumkreatinin, minskning av eGFR till mindre än eller lika med 45 ml/min/1,73 m², och påbörja njurersättningsterapi.
DECLARE-TIMI 58-studien fann att användningen av dapagliflozin var associerad med en 47 procents minskning av en njurkomposit av en ihållande minskning av eGFR med mer än eller lika med 40 procent till<60 ml/min/1.73="" m²,="" new="" eskd="" or="" death="" from="" a="" renal="" cause.="" the="" decline="" in=""><60 ml/min/1.73="" m²)="" was="" 46%="" less="" with="" dapagliflozin,="" and="" there="" were="" also="" significant="" reductions="" in="" eskd="" and="" renal="" death.="" additionally,="" dapagliflozin="" decreased="" new-onset="" albuminuria="" by="" 21%="" and="" new-onset="" macroalbuminuria="" by="">
En kombinerad analys av CANVAS- och CANVAS-R-studierna (CANVAS-programmet) noterade att användningen av canagliflozin minskade med 40 procent en njurkomposit av ihållande (22 på varandra följande åtgärder) minskning (med mer än eller lika med 40 procent) i eGFR-behov för njurersättningsterapi eller dödsfall på grund av njurorsaker [43]. Progression av albuminuri (förändring från normal till mikro- eller mikro- till makro-albuminuri eller mer än eller lika med 30 procent ökning av mikroalbuminuri) minskade med kanagliflozin med 27 procent, och många av patienterna som fick kanagliflozin visade en minskning av mikro- eller makroalbuminuri.
I VERTIS CV-studien reducerades njurkompositen, som inte inkluderade ett mått på eGFR (fördubbling av serumkreatinin, påbörjad njurersättningsterapi eller död av en njurorsak), numeriskt med 19 procent (inte statistiskt signifikant) med användning av ertugliflozin [44]. En separat analys av en njurkomposit som omfattar en varaktig minskning av eGFR med mer än eller lika med 40 procent, njurdialys/transplantation eller njurdöd noterade dock en minskning med 34 procent med ertugliflozin, och med 5 år, minskningen av eGFR var signifikant mindre (med 2,6 ml/min/1,73 m²) än med placebo. Med 5 år minskade ertugliflozin också progressionen från normal till mikroalbuminuri med 21 procent och ökade regression från makro- till mikro- och från makro- eller mikro- till normoalbuminuri med 23 procent.
Flera metaanalyser av njurdata från ovanstående CVOT och andra studier har bekräftat att SGLT2-hämmare minskade en sammansättning av försämrad eGFR, ESKD eller njurdöd med cirka 33 procent [46-48].
Försök på personer med nedsatt njurstatus I de fyra CVOT som beskrivs ovan var fördelaktiga effekter av SGLT2-hämmaren på de olika njurparametrarna uppenbara (i större eller mindre utsträckning) oavsett kön, etnicitet, ålder, vikt, varaktighet eller svårighetsgrad av diabetes; närvaro eller frånvaro av kardiovaskulär sjukdom; och baslinje-eGFR eller baslinjealbuminuri. Men i dessa studier hade få patienter framskriden CKD (egeGFR<45 ml/min/1.73="" m²)or="" advanced="" macroalbuminuria.="" this="" was="" addressed="" in="" the="" credence="" study="" in="" which="" type="" 2="" diabetes="" patients="" were="" recruited="" with="" an="" egfr="" range="" of="" 30-90="" ml/min/1.73="" m²,="" macroalbuminuria(uacr="">300 till<5,000 mg/g),="" and="" raas="" blockade="">
I CREDENCE hade 60 procent av patienterna en eGFR på<60 ml/min/1.73="" m²,and="" 30%="" had="" anegfr=""><45ml in/1.73="" m²(mean="" baseline="" egfr="" of="" 56="" ml/min/1.73="" m2),while="" 88%="" had="" a="" uacr="">{{0}} mg/g (median UACR 927 mg/g). Njurkompositen (fördubbling av serumkreatinin, ESKD, njurdöd eller CV-död) var 30 procent lägre med användning av kanagliflozin, och det fanns en signifikant minskning av minskningen av eGFR för dem som fick kanagliflozin jämfört med placebo (-1.85±0.13 mot -4.59±0.14 ml/min/1.73 m² /år). Om dessa olika minskningshastigheter av eGFR fortsatte för en sådan population (63 år, eGFR 56 ml/min/1,73 m²), beräknas det ta mer än 10 år längre för kanagliflozinpatienterna att utvecklas till ESKD [49]. I CREDENCE fanns det faktiskt 32 procent färre fall av ESKD(eGFR av<15 ml/min/1.73="" and/or="" renal="" replacement)="" and="" 34%="" fewer="" renal="" deaths="" with="" the="" use="" of="" canagliflozin.="" also,="" canagliflozin="" lowered="" uacr="" by="" 31%="" at="" 6="" months="" and="" increased="" by="" 30%="" the="" number="" of="" patients="" with="" a="" reduction="" in="" uacr[50].="" of="" particular="" note,="" the="" effectiveness="" of="" the="" sglt2="" inhibitor="" to="" slow="" the="" decline="" in="" egfr="" and="" reduce="" the="" progression="" of="" albuminuria="" was="" similar="" for="" patients="" with="" a="" baseline="" egfr="">eller<45 ml/min/1.73="" m²and="" a="" uacr="">eller<1,000 mg/g,="" and="" the="" sglt2="" inhibitor="" also="" slowed="" the="" decline="" in="" egfr="" for="" patients="" with="" a="" baseline=""><30 ml/min/1.73m².="" the="" effectiveness="" of="" the="" sglt2="" inhibitor="" on="" these="" parameters="" was="" independent="" of="" glycaemic="" status,="" type="" of="" raas="" blockade,="" and="" atherosclerotic="" cardiovascular="" disease,="" suggesting="" that="" the="" benefits="" of="" sglt2="" inhibitors="" on="" renal="" function="" can="" be="" gained="" irrespective="" of="" cardio-renal="" or="" metabolic="" status="" in="" type="" 2="">
Similar findings emerged from the SCORED trial in type 2 diabetes patients with CKD (eGFR 25-60 ml/min/1.73 m²). Treatment with the SGLT1/2 inhibitor sotagliflozin was associated with a 29% reduction in the renal composite of sustained (>30 days) decrease of≥50% in eGFR,dial-ysis, renal transplantation or sustained(>30 dagar)eGFR av<15 ml/min/1.73="">
Because the CVOTs and similar studies in type 2 diabetes indicated that the cardio-renal benefits of SGLT2 inhibitors were not contingent on their glucose-lowering efficacy, studies were undertaken in populations that included people without diabetes(Table 4).The DAPA-CKD trial examined the effect of dapagliflozin in people with(67%)and with-out(33%)type 2 diabetes who had renal impairment (eGFR 25-75ml/min/1.73 m²,mean 43.1 ml/min/1.73 m²; and UACR 200-5000 mg/g,median~950 mg/g with 48.3% of patients having a UACR>1000 mg/g)[51].Standard care for all patients included RAAS blockade. Similar reductions in the renal composite endpoint(decline in eGFR>50%, ESKD, renal death, or CV death) were observed with the use of dapagliflozin in those with (by 36%)and without(by 50%)diabetes. Dapagliflozin also reduced each of the component measures of the composite, and the findings were generally consistent for patients with an eGFR>eller<45 ml/min/1.73="" m²or="" uacr="">eller<1,000 mg/g.="" the="" average="" annual="" decline="" in="" egfr="" was="" also="" slower="" with="" dapagliflozin="" than="" with="" placebo="" (-1.67="" versus-3.59="" ml/min/1.73="">
