Effekten av högt saltintag på ett naturligt tarm-ekosystem hos vilda möss
Oct 30, 2023
Abstrakt: Däggdjursholobionten hyser en komplex och ömsesidigt beroende mutualistisk tarmbakteriegemenskap. Förändringar i sammansättningen av detta bakteriekonsortium är kända för att vara en nyckelfaktor i värdhälsan, immunitet och sjukdom. Bland många andra är kostvanor avgörande drivkrafter för en potentiell störning av den ömsesidiga interaktionen mellan bakterier och värd. I detta sammanhang har vi tidigare visat att en högsaltdiet (HSD) leder till ett dysbiotiskt tillstånd av murin tarmmikrobiota, kännetecknad av en minskning eller utarmning av välkända hälsofrämjande tarmbakterier. Men på grund av en kontrollerad och sanerad miljö har konventionella laboratoriemöss (CLM) en mindre mångfaldig tarmmikrobiota jämfört med vilda möss, vilket leder till dåliga translationsresultat för tarmmikrobiomstudier, eftersom en minskad tarmmikrobiota-diversitet skulle kunna misslyckas med att skildra komplexet beroende av varandra. mikrobiomets nätverk. Här utvärderade vi HSD-effekten på tarmmikrobiota i CLM i jämförelse med vilda möss, som har ett naturligt tarm-ekosystem som närmare efterliknar situationen hos människor. Möss behandlades med antingen kontrollfoder eller HSD och tarmmikrobiota profilerades med användning av amplikonbaserade metoder riktade mot 16S ribosomalgenen. I linje med tidigare fynd avslöjade våra resultat att HSD inducerade betydande förlust av alfa-diversitet och omfattande modulering av tarmmikrobiotasammansättningen i CLM, kännetecknad av minskningen av potentiellt nyttiga bakterier från Firmicutes phylum såsom släktena Lactobacillus, Roseburia, Tuzzerella, Anaerovorax och ökning av Akkermansia och Parasutterella. HSD-behandlade vilda möss visade dock inte samma förändringar i termer av alfa-diversitet och förlust av Firmicutes-bakterier som CLM, och mer generellt uppvisade vilddjur endast mindre förändringar i tarmmikrobiotans sammansättning efter HSD. I linje med detta föreslog den 16S-baserade funktionella analysen endast stora förändringar av tarmmikrobiota ekologiska funktioner i CLM jämfört med vilda möss på HSD. Våra fynd tyder på att rikare och vildhärledd tarmmikrobiota är mer resistent mot kostinterventioner som HSD, jämfört med tarmmikrobiota av CLM, vilket kan ha viktiga konsekvenser för framtida translationell mikrobiomforskning.

cistanche tubulosa-förbättra immunförsvaret
Nyckelord: mikrobiom; kost med hög salthalt; immunitet; vildling
1. Introduktion
Däggdjurens tarm koloniseras av ett komplext och mångsidigt bakteriesamhälle, som tillsammans med värden skapar en delikat symbiotisk relation [1,2]. Denna bakteriella gemenskap utövar många funktioner användbara för värden, inklusive metaboliska, immunmodulerande och trofiska funktioner [3–7] och tarmmikrobiotans sammansättning kan förändras under livet, i linje med värdens specifika behov och fysiologi [1,8, 9]. Många fördelaktiga funktioner hos tarmhälsofrämjande bakterier förmedlas av anaeroba jäsningshärledda metaboliter [10-13] och dysbiotiska tillstånd kan signifikant påverka värdens hälsa [2,11,14,15]. Den växande oron för livsstilens påverkan på hälsan har lett till ett ökat vetenskapligt intresse för tarmmikrobiota och dess translationella implikationer [16,17]. Faktum är att tarmmikrobiotan formas av både yttre (t.ex. livsstil, diet och medicinska behandlingar) och inneboende (t.ex. värdgenetik, immun- och metaboliska regler) faktorer [8,18–20]. Det är allmänt erkänt att yttre element kan framkalla effektfulla effekter, med kosten som en av de främsta bidragande faktorerna för att påverka tarmmikrobiotans sammansättning och funktion [1,2,21]. Västerländska kostkomponenter, såsom högt saltintag, är kända för att skada värdhomeostas genom att påverka immunsystemet och förändra tarmmikrobiotan och sjukdomar [18,22–37]. I murin tarmmikrobiota är en högsaltdiet (HSD) associerad med minskningen av hälsofrämjande bakterier som är notoriskt kända som producenter av kortkedjiga fettsyror (SCFA) såsom Lactobacillus spp., Bifidobacterium, Blautia och Faecalibaculum [28, 29,38–41], tillsammans med en ökning av förekomsten av Akkermansia, en annan opportunistisk SCFA-producent som har visat sig påverka värdimmunitet och sjukdom i olika modellsystem [42,43]. Murina djurmodeller används ofta för att studera hur kostfaktorer kan forma tarmens mikrobiota, immunförsvar och sjukdomar [29,44–46]. Även om användningen av konventionella laboratoriemöss (CLM) fortfarande är ett giltigt alternativ för många studier, misslyckas det ibland med att korrekt översätta tarmmikrobiota-fokuserade applikationer [47–49]. Till exempel visade sig immunologisk och metabolomisk forskning i murina modeller av inflammatorisk tarmsjukdom (IBD) och fetma dåligt förutsäga translationella resultat av studier av tarmmikrobiota [50]. Detta kan bero på många inneboende skillnader i dessa modellsystem, såsom olika tarmens anatomi, genetik och fysiologi [16,50]. Ett annat problem med att använda CLM för att studera mikrobiota-immuninteraktioner är dock domesticeringen av tarmbakteriesammansättningen i CLM, vilket återspeglas i minskningen av komplexiteten och motståndskraften hos CLM-tarmmikrobiotan jämfört med vilda möss [51]. Behovet av sanerade och kontrollerade miljöer står inför en minskad närvaro av potentiella patogener och parasiter, vilket antas följaktligen leda till ett mindre "utbildat" immunsystem i CLM jämfört med vilda möss [51-53]. För att ta itu med detta problem utvecklades den vilda murina modellen genom C57BL/6-möss-härledda embryoöverföring till vilda möss för att erhålla en vild-härledd tarmmikrobiota, för att övervinna translationsproblemet med immunologiska tarmmikrobiotastudier [54]. Nyligen genomförda studier som involverade denna musmodell visade överlägsna resultat för att förutsäga translationsvärdet av experimentella immunterapier jämfört med CLM [54,55]. Dessutom var mikrobiota från vilda tarmar mer resistenta och motståndskraftiga mot antibiotikabehandling och fettrik kost jämfört med CLM, jämförbar med den mer komplexa situationen hos människor [54,55]. Men trots de etablerade effekterna av HSD på tarmmikrobiota, immunförsvar och olika sjukdomsmodeller i CLM, är effekterna av högt saltintag på naturlig, vildhärledd tarmmikrobiota okända. I denna studie utvärderade vi effekten av HSD på olika tarmbakterieekosystemsammansättningar och prediktiva funktioner hos CLM i jämförelse med vilda möss.
2. Material och metoder
2.1. Djur och kost
Vildtyp C57BL/6-möss (7–8 veckor gamla honor, n=20) köptes från Charles River och hölls i djuranläggningen vid University of Hasselt under standardiserade förhållanden. Vilda möss (C57BL/6 genetisk bakgrund, hanar n=12 och honor n=11) [54] hölls i djuranläggningen i UHasselt under standardiserade förhållanden. Djurstudier godkändes av Ethical Committee on Animal Experiment (ECAE) vid Hasselt University (ID201618A4V1, ID202235). Möss inhystes (4 möss/bur) i ett temperaturkontrollerat rum (21–23 ◦C) med en 12:12 h ljus/mörk ljuscykel. Följande renade dieter köptes från Ssniff (Soest, Tyskland): 0,5 % NaCl/kontrolldiet (E15430-04) och 4% NaCl/HSD (E15431-34). För HSD matades djuren med 1 % NaCl i dricksvattnet förutom E15431-34, som beskrivs i [28]. CLM-möss var jämnt fördelade mellan kontrollgruppen (n=10) och HSD (n=10). För de vilda mössen, var han- och honindivider också lika fördelade i kontroll- och HSD-dietgrupper (6 hanar för kontroll, 6 hanar för HSD, 5 honor för kontroll och 6 honor för HSD).

cistanche växthöjande immunförsvar
2.2. DNA-extraktion
Mikrobiell DNA-extraktion utfördes enligt beskrivning i [28], genom att använda ett modifierat protokoll av QIAmp Fast DNA Stool Mini Kit (Qiagen, Hilden, Tyskland). I korthet sattes fekala pellets till en 2-mL Eppendorf innehållande 0,5 mm glaspärlor och 1,5 ml lysbuffert (ASL) (Qiagen, Hilden, Tyskland). Pärlslagning användes för att utföra mekanisk homogenisering av pelletsen. Fullständig extraktion utfördes enligt tillverkarens protokoll med mindre modifieringar (förlängning av proteinas K-inkubationstiden till 2 timmar vid 70 ◦C). DNA-koncentrationer utvärderades med hjälp av en NanoDrop ND-1000-spektrofotometer (NanoDrop Technologies, Wilmington, DE, USA) och lagrades vid -20 ◦C före 16S rRNA-genamplifiering.
2.3. 16S rRNA-genamplifiering och sekvensering
16S rRNA-gensekvens amplifierades genom att använda en primer specifik för V4-regionen (F515/R806), som tidigare beskrivits [56]. Kortfattat användes 25 ng DNA per PCR-reaktion (30 µL) (KAPA HiFi HotStart ReadyMix, Roche, Basel, CH, USA) av initial denaturering i 30 s vid 98 ◦C, följt av 25 cykler (10 s vid 98 ◦ C, 20 s vid 55 ◦C och 20 s vid 72 ◦C). Reaktioner utfördes i tre exemplar, slogs samman per prov och renades med ett magnetiskt pärlbaserat rengöringssystem (Agencourt AMPure XP, Beckman Coulter, Brea, CA, USA). Biblioteksberedning utfördes med en PCR med begränsad cykel för att erhålla det indexerade biblioteket med hjälp av Nextera-teknologi (Nextera XT Index Kit, Illumina, San Diego, CA, USA), följt av ett andra AMPure XP-reningssteg för magnetiska pärlor. Indexerade prover normaliserades sedan till samma koncentration av 4 nM, slogs samman och sekvenserades på en Illumina MiSeq-plattform PE300 med ett 2 × 300 bp protokoll med parad ände enligt företagets protokoll (Illumina, Inc., San Diego, CA, USA).

cistanche tubulosa-förbättra immunförsvaret
Klicka här för att se produkter från Cistanche Enhance Immunity
【Be om mer】 E-post:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
2.4. Bearbetning och statistisk analys av 16S rRNA-gensekvenseringsdata
Råsekvenser bearbetades med en QIIME 2 [57] pipeline. Efter längd- och kvalitetsfiltrering (standardparametrar) filtrerades läsningar och tilldelades operationella taxonomiska enheter (OTU) med DADA2 [58]. Taxonomisk tilldelning utfördes av VSEARCH-algoritmen (https://github.com/torognes/vsearch; åtkoms den 9 november 2022) och Silva-databasen v128 (https://www.arb-silva.de /; åtkoms den 9 november 2{{40}}22). ASV-tabellen normaliserades sedan genom sällsynthet vid 6,147 djup så att varje prov nådde platån i slutet av sällsynthetskurvan. Alfa-diversitet utvärderades med hjälp av två olika mått: OTUs richness (Observed), Chao1, Shannon, Simpson, Inverse Simpson (InvSimpson) ekologiska index. För beta-diversitet beräknades och plottades Bray−Curtis-skillnad, Jaccard-likhet och viktade och oviktade UniFrac-mått [59] med Principle Coordinates Analysis (PCoA) för att visualisera det verkliga avståndet mellan proverna. För att normalisera OTU-räkningstabellen utfördes sällsynthet på ett djup av 6305 sekvenser per prov 100 gånger. Utdata som erhölls från OTU-taxonomitilldelningen, som en taxonomitabell, användes för att kollapsa den normaliserade OTU-tabellen till tabeller för taxonominivåerna L2 (Phylum), L5 (Familj) och L6 (Genus). Statistiska analyser utfördes med hjälp av R (https://www.R-project.org/; tillgänglig den 25 november 2022; version 4.2.0). R-paketet "vegan" (Version 2.6-4) [60] användes för att generera beta-diversitetsmått för att jämföra sammansättningsskillnader mellan grupper med PCoA eller genom principal component analysis (PCA). Paket och dataseparation testades genom permutationstest med pseudo-F-förhållanden (funktion "Adonis" i "vegan"). Separation i termer av beta-diversitet mellan grupper testades med Permutational Multivariate Analysis of Variance Using Distance Matrices (PERMANOVA, funktion "Adonis" i "vegan"), medan skillnader för spridning inom grupper testades med Multivariate homogeneity of groups dispersions test (PERMDISP) , funktion "betadisper" i "vegan"). Taxa som inte fanns i minst 4 prover exkluderades från analysen. Skillnader i form av relativa taxaförekomster utvärderades först med det preliminära Kruskal-Wallis-testet mellan 4 grupper och utvärderades sedan ytterligare med Wilcoxon-testet mellan följande jämförelsepar: CLM Control vs. CLM HSD, Wildling Control vs. Wildling HSD, CLM Control vs. wildling Control, CLM HSD vs. wildling HSD. För utvärdering av taxonomiska skillnader mellan wildling och CLM användes Linear Discriminant Analysis Effect Size (LEfSe: https://huttenhower.sph.harvard.edu/galaxy/; tillgänglig den 25 november 2022) för att särskilja huvuddragen på släktnivå [ 61]. LEfSe-resultaten visades sedan som ett stapeldiagram, med en Linjär Diskrimineringsanalys (LDA) poängtröskel högre än 1,0. När det var nödvändigt justerades p-värden för flera jämförelser med Benjamini-Hochberg-metoden. En falsk upptäcktsfrekvens (FDR) Mindre än eller lika med 0,05 ansågs vara statistiskt signifikant: * p Mindre än eller lika med 0,05; ** p Mindre än eller lika med 0,01; *** p Mindre än eller lika med 0,001. Funktionella skillnader mellan mikrobiomer med olika NaCl-innehåll i maten (0,5% och 4% NaCl-matinnehåll) analyserades av PICRUST2, ett bioinformatikprogram för att förutsäga metagenomfunktionellt innehåll från 16s rDNA-gensekvenseringsdata (https://huttenhower.sph. harvard.edu/picrust/; åtkoms den 29 november 2022; PICRUST2 2.4.1) [62]. PICRUST2-pipeline applicerades på representativa sekvenser och deras överflödstabell från DADA2 med hjälp av standardparametrar (https://github.com/picrust/picrust2/wiki/Full-pipeline-script; åtkoms den 29 november 2022). Från den fullständiga pipeline-utgången byggdes metagenomisk förutsägelse för KEGG Orthology och MetaCyc-vägar som tabeller, med prediktiva funktioner som rader och prover som kolumner, och användes för att jämföra tarmmikrobiotafunktioner i wildling och CLM på HSD-regim. Mikrobiella gemenskapsprediktiva funktioner som bidrog mest till variationen mellan vilddjur och CLM efter första (PC1), andra (PC2) och tredje huvudkomponent (PC3) valdes ut för ytterligare analys av HSD-konsumtion i de två modellerna. Matrisen med de prediktiva funktionsöverflöden normaliserades sedan, transformerades i centrerad loggförhållande (CLR)-värden och log2mean-förhållandet beräknades (HSD/kontroll) för både vilddjur och CLM. Slutligen jämfördes log2mean-förhållandena mellan grupper med Wilcoxon-test och plottades som en kilskrift. Skillnader mellan grupper jämfördes statistiskt i R-programvara med Wilcoxon-test- och Kruskal-Wallis-testfunktioner och p-värden justerade med Holm- eller Benjamini-Hochberg-metoden.
3. Resultat
3.1. HSD påverkar mångfald och sammansättning av CLM och Wildling Gut Microbiota
För att undersöka effekten av HSD på ett vildhärlett mikrobiellt ekosystem i tarmen hos möss, matade vi HSD eller kontrolldieter till vilddjursmöss och CLM. Möss hölls på dietregimer i två veckor och sammansättningen av fekal tarmmikrobiota undersöktes därefter genom 16S RNA-gensekvensering från fekala pellets insamlade vid dag 14 (Figur 1A). I linje med en tidigare rapport upptäcktes inga starka skillnader i termer av kroppsvikter mellan kontroll- och HSD-grupper av CLM och vilda möss [29]. För att bedöma den olika tarmmikrobiotan mellan de två modellerna CLM och vilda möss vid baslinjen, uppskattade vi alfa-diversitet (Observed eller Richness, Chao1, Shannon, Simpson och Inverse Simpson-index), beta-diversitet (Bray−Curtis-skillnad) och de viktigaste taxonomiska skillnader. I linje med tidigare studier [54] kännetecknades vilddjurens tarmmikrobiota av större mikrobiell rikedom (Figur 1B, alla alfa-diversitetsindex), såväl som en distinkt och mer heterogen mikrobiell sammansättning än CLM (Figur 1C, PERMANOVA p {{9} }.001 & PERMDISP p=0.0009, wildling vs. CLM; och figur S1). När det gäller mikrobiella signaturer, kännetecknades CLM och vilda möss tarmmikrobiota av olika bakteriella taxa (Figur S1). I linje med Rosshart et al. [54], bakteriella taxa från vilda möss tillhör Intestinomonas, Desulfovibrio, Tuzzerella, Oscillobacter, Orodibacter och det patogena släktet Helicobacter, som karakteriserade den vildhärledda icke-domesticerade profilen för denna modell (Figur S1).

Figur 1. HSD-påverkan på bakteriesammansättningen av CLM (n=10/grupp) och vilda möss (n=11 för vilda Ctrl och n=12 för vilda HSD). (A) Experimentell design. C57BL/6 CLM eller vilda möss matades med 0,5 % NaCl (kontroll, Ctrl) eller högsalt 4 % NaCl (HSD) och tarmbakteriesamhällets tarm kännetecknad av 16S rRNA-genamplikonsekvensering. (B) Index för alfa-diversitet av fekal tarmmikrobiota av CLM och vilddjur; från vänster till höger visas följande index: Observed (OUT richness), Chao1, Shannon, Simpson, Simpson (Inverse Simpson). Skillnader mellan grupper utvärderas statistiskt med Wilcoxon-testet. (C) Huvudkoordinatanalysplot av beta-diversitetsordination från Bray−Curtis-skillnadsmått mellan CLM vs. wildling (överst), CLM-kontroll vs. CLM HSD (nederst till vänster) och wildling-kontroll vs. wildling HSD (nedre höger); separation och homogenitet mellan grupperna beräknades med PERMANOVA- respektive PERMDISP-tester. * p Mindre än eller lika med 0.05; ** p Mindre än eller lika med 0.01; **** p Mindre än eller lika med 0.0001. Figur 1. HSD-påverkan på bakteriesammansättningen av CLM (n=10/grupp) och vilda möss (n=11 för vilda Ctrl och n=12 för vilda HSD). (A) Experimentell design. C57BL/6 CLM eller vilda möss matades med 0,5% NaCl (kontroll, Ctrl) eller högsalt 4% NaCl (HSD) och tarmbakteriesamhällets tarm kännetecknad av 16S rRNA-genamplikonsekvensering. (B) Index för alfa-diversitet av fekal tarmmikrobiota av CLM och vilddjur; från vänster till höger visas följande index: Observed (OUT richness), Chao1, Shannon, Simpson, Simpson (Inverse Simpson). Skillnader mellan grupper utvärderas statistiskt med Wilcoxon-testet. (C) Huvudkoordinatanalysplot av beta-diversitetsordination från Bray−Curtis-skillnadsmått mellan CLM vs. wildling (överst), CLM-kontroll vs. CLM HSD (nederst till vänster) och wildling-kontroll vs. wildling HSD (nedre höger); separation och homogenitet mellan grupperna beräknades med PERMANOVA- respektive PERMDISP-tester. * p Mindre än eller lika med 0,05; ** p Mindre än eller lika med 0,01; **** p Mindre än eller lika med 0,0001.
HSD inducerade en signifikant minskning av bakteriell mångfald (Figur 1B, alla alfa-diversitetsindex) såväl som en signifikant mikrobiell förändring i sammansättningen av CLM (Figur 1C, PERMANOVA p=0.001, PERMDISP p=0 .1, CLM Ctrl vs. CLM HSD). Däremot kännetecknades tarmmikrobiotan hos vilda möss av högre mångfald vid HSD (Figur 1B, Observed & Chao1 index), avvikande från CLM, och de kännetecknades också av mindre uttalad mikrobiell sammansättningsförskjutning på HSD jämfört med CLM (Figur 1C, PERMANOVA p=0.001, PERMDISP p=0.5, wildling Ctrl vs. wildling HSD).
3.2. Tarmmikrobiell sammansättning av vilda möss är mer resistent mot HSD än CLM
Bakteriesammansättningsskillnader mellan wildling och CLM karakteriserades ytterligare taxonomiskt. På fylumnivå var de vanligaste fylerna när det gäller relativ förekomst: Firmicutes (CLM: 52 ± 12%, vildling: 32 ± 34%), Bacteroidota (CLM: 24 ± 23%, vildling: 57 ± 19%), Actinobacteriota (CLM: 1{{10}} ± 7%, vildling: 0,7 ± 1,3%) och Verrucomicrobiota (CLM: 24 ± 23%, vildling: 0%/ej upptäckt) (Figur 2). Tarmmikrobiella profilen visade ytterligare olika förekomster för alla phyla detekterade i fekala prover mellan vilda möss och CLM (Figur 2). Speciellt var kärnmikrobiota phyla Firmicutes, Bacteroidota och Verrucomicrobiota signifikant olika mellan de två modellerna (Figur 2). Mer specifikt, på familjenivå, observerades ett annat bidrag i vilddjur kontra CLM tarmmikrobiota för de flesta av de bakterier som tidigare rapporterats som HSD-känsliga [28], inklusive Lactobacillaceae, Clostridiaceae, Peptostreptococcaceae och Akkermansiaceae (Figur 3). I linje med detta bekräftades liknande trender på släktnivå mellan vilddjurs- och CLM-prover för huvudmedlemmarna i de tidigare nämnda familjerna; bland dessa var de mest representativa Lactobacillus, Roseburia, Tuzzerella, Faecalibaculum och Akkermansia (figur S1 och 4). För att ytterligare karakterisera effekten av HSD på CLM och vilda tarmmikrobiotakompositioner, analyserade vi också effekten av dietregimen på olika klassificeringsnivåer. På filumnivå kännetecknades HSD-behandlad CLM-tarmmikrobiota av betydande utarmning av Firmicutes och anrikning av Verrucomicrobiota (Figur 2), men ingen av de större filorna påverkades av HSD i vilddjursprover (Figur 2). På familjenivå kännetecknades CLM-tarmmikrobiota av betydande utarmning av mjölksyraproducerande bakterier som Lactobacillaceae, såväl som SCFA-producenter som Peptostreptococcaceae och Clostridiaceae (Figur 3). Dessutom, i HSD-matad CLM, observerade vi ökningar i Akkermansiaceae, Sutterellaceae, Defluvitaleaceae och Eggerthellaceae (Figur 3). Däremot påverkade HSD olika bakteriefamiljer i vilddjurs-tarmmikrobiota, bland dem de två mycket rikliga Muribaculaceae och Prevotellaceae, som båda ökade vid HSD (Figur 3). Bakteriemodulering som mest bidrog till HSD-effekten i CLM inkluderade ökningen av släktena Akkermansia, Parasutterella och Enterorhabdus, såväl som minskningen av Lactobacillus, Roseburia, Tuzzerella, (Eubacterium) oxidoreducens group, Muribaculum och Anaerovorax (Figur 4). Förutom Roseburia påverkades inga av de tidigare nämnda släktena av HSD i vilddjursmikrobiota, medan släktet Anaerovorax visade en motsatt tendens från CLM (Figur 4).

Figur 2. HSD-effekt på bakteriefila från tarmmikrobiota av CLM (n=10/grupp) och vilda möss (n=11 för vilda Ctrl och n=12 för vilda HSD). Den totala sammansättningen i form av phyla relativ förekomst visas av stapeldiagram per varje individ (överst) och boxplot för specifik phyla (nederst); statistiska jämförelser utfördes mellan grupper med Wilcoxon-test. * p Mindre än eller lika med 0.05; ** p Mindre än eller lika med {{10}}.01; *** p Mindre än eller lika med 0,001; **** p Mindre än eller lika med 0,0001.

Figur 3. Effekten av högsaltmatkonsumtion på bakteriefamiljer av CLM (n=10/grupp) och vilda möss (n=11 för vilda Ctrl och n=12 för vilda HSD). Total sammansättning på familjenivå representeras av stapeldiagram per individ (överst) och boxplot för specifika familjer (nederst); statistiska jämförelser utfördes mellan grupper med Wilcoxon-test. * p Mindre än eller lika med 0.05; ** p Mindre än eller lika med {{10}}.01; *** p Mindre än eller lika med 0,001; **** p Mindre än eller lika med 0,0001.
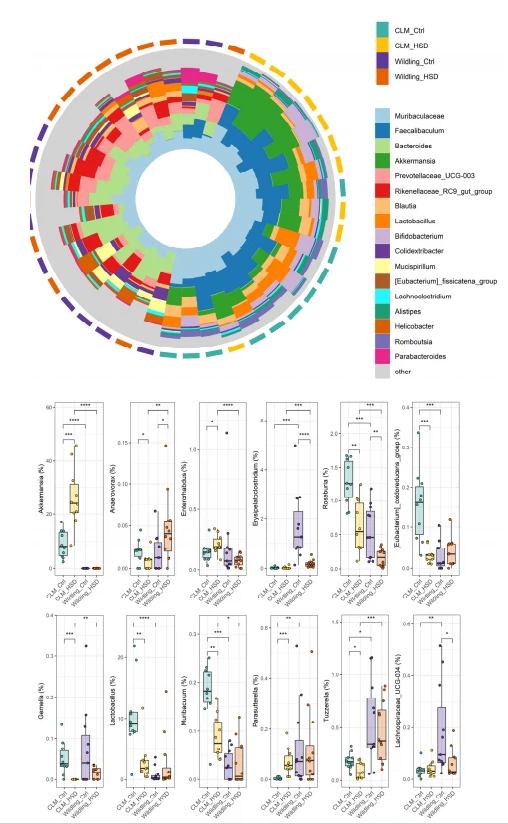
Figur 4. Förändringar i bakteriesläkten i CLM (n=10/grupp) och vilda möss (n=11 för vilda Ctrl och n=12 för vilda HSD). Det totala relativa överflödsbidraget på släktnivå plottas som ett cirkulärt stapeldiagram per varje individ (överst) och en boxplot för specifika släkten (nederst); statistiska jämförelser utfördes mellan grupper med Wilcoxon-test. * p Mindre än eller lika med 0.05; ** p Mindre än eller lika med 0.01; *** p Mindre än eller lika med 0,001; **** p Mindre än eller lika med 0,0001.
3.3. HSD påverkar prediktiva mikrobiella funktioner i CLM men inte i vilda möss
PICRUST 2-utdata detekterade inte någon signifikant skillnad mellan mikrobiella samhällsfunktioner hos vilda HSD kontra obehandlade vilda möss för både KEGG Orthology och MetaCyc-vägkommentarer, med det enda undantaget av HSD-inducerad ökad funktion på recG-genen för en ATP-beroende helikas från KEGG-ortologin (Figur 5A). HSD-påverkan på CLM kännetecknades av en signifikant minskning av prediktiva funktioner för KEGG Orthology, bland dem genen spp (sackaros-6-fosfatas) och pfkA (fosfofruktokinas 1), båda involverade i stärkelse- och sackarosmetabolism, vilket är i linje med med tidigare fynd [28] (Figur 5A). Dessutom kännetecknades tarmmikrobiotan av HSD-matad CLM av minskade prediktiva funktioner hos gener involverade i membrantransport (feoB för järntransport, AB 2P AB 2 permeasprotein, AB 2A AB 2 ATP-bindande protein), glutaminbiosyntes (glnA) transkriptionell regulator av Lacl-familjen (lacI, galR) och transketolas (tktA, tktB) (Figur 5A). För MetaCyc-vägar berikade HSD signifikant CLM-tarmmikrobiotan av prediktiva funktioner associerade med nitratreduktion (denitrifikationsväg), galaktosnedbrytning (D-galaktaratnedbrytning, superväg för nedbrytning av D-glukarat och D-galaktarat), nedbrytning av fenylpropanot, fetthalt. syraräddning, succinatnedbrytning till butansyra och aminosyranedbrytning (aromatisk aminnedbrytning, L-leucinnedbrytning) (Figur 5B). Dessutom, i linje med tidigare fynd [28], förlorade HSD-tarmmikrobiota i CLM prediktiva funktioner för amminosyrabiosyntes (superväg för L-alaninbiosyntes, L-lysinbiosyntes), blandad syrafermentering, med ytterligare ny signatur förlorad som N- nedbrytning av acetylglukosamin/N-acetylmannosamin/N-acetylneuraminat och nedbrytning av deoxiribonukleosider (pyrimidin- och purinnedbrytning, inosin5fosfatbiosyntes III) (Figur 5B).

Figur 5. Forts.

Figur 5. Effekt av HSD på tarmprediktiva metagenomiska funktioner i CLM (n=10/grupp) och vildling (n=11 för vildling Ctrl och n=12 för vildling HSD) tarmmikrobiota. PICRUST2-utdata plottad som kilskrift för KEGG Orthology-annotering (A) och MetaCyc-vägar (B) uttryckt som log2-medelförhållandet mellan antalet prediktiva funktioner mellan HSD vs Ctrl-prover. Alla statistiska jämförelser utfördes mellan Ctrl- och HSD-grupper genom Wilcoxon-test.
4. Diskussion
Komplex och mångsidig tarmmikrobiota är känd för att vara mer motståndskraftig mot vissa sjukdomsmodeller [51] och kostregimer, såsom högt fettintag [54,55]. Men ingen tidigare studie har utvärderat effekterna av högt natriumintag på murin vildhärledd tarmmikrobiota. Här undersökte vi för första gången hur HSD påverkar vilddjurs tarmmikrobiota jämfört med CLM. Intressant nog visade våra resultat att jämfört med CLM är vilddjursmikrobiomet mer resistent mot HSD-störningar på både sammansättnings- och prediktiv funktionsnivå. Det är välkänt att högt saltintag kan förvärra risken för olika sjukdomar, såsom kardiovaskulära eller autoimmuna sjukdomar, genom att förändra tarmmikrobiomsammansättningen och immunhomeostas [25,29,31,34,63–65]. I linje med tidigare rapporter kännetecknades HSD-inducerade förändringar i tarmmikrobiota i CLM av betydande förändringar i mikrobiell mångfald, sammansättning och prediktiva funktioner [28]. Hälsofrämjande bakterier som familjen Peptostreptococcaceae och släktena Lactobacillus, Roseburia och Tuzzerella minskade i form av relativ förekomst i CLM, medan Akkermansia ökade signifikant i HSD-matade grupper. Vi upptäckte också högre relativa förekomster av HSD i Defluvitaleaceae, Enterorhabdus och Parasutterella. Intressant nog är släktet Parasutterella en kärnkomponent i tarmmikrobiotan hos både CLM och människor, där det beter sig som en asackarolytikum och producent av succinat [66]. Både Enterorhabdus från familjen Eggerthellaceae och Parasutterella från familjen Sutterellaceae är kända för att vara berikade hos patienter med IBD [67,68], vilket ytterligare indikerar hur HSD kan påverka sjukdomsutvecklingen. Men intressant nog visade vilddjursmöss inte en liknande enhet av HSD-inducerade mikrobiella skift, såsom CLM. Trots detta ökade mångfalden av vilddjur avsevärt på HSD för observerade OTU:er och Chao1-mått, och endast ett fåtal taxa var involverade i HSD-störningen av vilddjurs tarmmikrobiota, bland dem en ökning av Anaerovorax, tillsammans med en minskning av Erysipelatoclostridium, Roseburia och Lachnospiraceae UCG-004 släkte. Roseburia var den enda bakteriesignaturen som vanligtvis delades mellan HSD-grupper jämfört med motsvarande kontroller, trots att HSD-matad CLM fortfarande kännetecknas av ett högre överflöd av denna bakterie jämfört med HSD-matade vilda möss. Att notera, butyratproducerande bakterier som Roseburia visades ha lägre relativ förekomst hos patienter med ulcerös kolit [69] och denna minskning observerades också vara korrelerad med IBD genetisk risk hos människor [70]. Detta är i linje med tidigare fynd, där förändringar i bakteriesläkten som Roseburia eller Lactobacillus visade sig vara associerade med en risk för högt blodtryck, möjligen främjat av en västerländsk diet [71]. Den bakteriella sammansättningen av tarmen är också associerad med tarmens motilitet och fysiologi [72].

cistanche fördelar för män stärker immunförsvaret
Släktet Anaerovorax har tidigare observerats hos möss med onormal tarmfysiologi och nedsatt rörlighet [73]; dock kan anrikningen av Anaerovorax i HSD för vilda möss leda till en annan roll för denna taxa i samband med tarmhomeostas och korrekt funktion. I linje med tidigare fynd observerade vi en ökning av släktet Akkermansia i HSD-gruppen av CLM [28], medan tarmmikrobiotan av vilda möss var utarmad på detta släkte, vilket också överensstämmer med tidigare studier på denna modell [51, 53–55]. Även om släktet Akkermansia är ett potentiellt probiotikum på grund av dess positiva effekt på att förbättra värdens immunologiska och metaboliska profiler (t.ex. vid fetma och typ 2-diabetes) [42,74–77], är rollen för detta släkte fortfarande oklar på grund av dess negativa korrelation med kliniska resultat i kolorektal cancer [78], Parkinsons sjukdom [79,80] och multipel sklerospatienter [81]. I enlighet med våra tidigare resultat som erhållits med MetaCyc-vägar [28], visade CLM vid HSD minskade prediktiva mikrobiella funktioner associerade med stärkelse- och sackarosmetabolism för KEGG-ortologi. De mindre förändringarna i tarmbakteriesammansättningen hos HSD-matade vilda möss lyckades dock inte inducera några signifikanta variationer i prediktiva bakteriefunktioner, vilket indikerar att tarmmikrobiota och metaboliska/ekologiska nätverk från vilddjur är mycket mer stabila och kan anpassa sig mycket lättare till HSD-inducerade kostvariationer jämfört med CLM tarm-ekosystem, vilket motiverar ytterligare undersökning. Värt att nämna är också det möjliga inflytandet från tarmsvampsamhället på tarmbakteriernas nätverk på differentiella kostregimer. Tidigare studier har redan föreslagit hur potentiella interaktioner mellan bakterier och svampar är inblandade i värdimmunsystemets homeostas och sjukdomsutveckling [82-85]. I detta sammanhang är CLM ytterligare begränsad av deras lägre bakteriella komplexitet jämfört med vilda möss, vilket kan hindra etableringen av en mångsidig tarmmykobiota [54]. Framtida studier kommer att kunna fastställa bidraget från tarmsvampsamhällen i miljöer av tarmmikrobiota och värdimmunitet genom att använda vilddjursmodellen. Sammanfattningsvis ger vår studie data om hur högt natriumintag påverkar ett naturligt, vildhärdat tarmmikrobiellt ekosystem i jämförelse med ett domesticerat tarmbakteriesamhälle av CLM. Vår studie visade att HSD inte påverkar bakteriell taxa och tarmmikrobiota hos vilda möss på samma sätt som det gör för en domesticerad tarmmikrobiota från CLM. Denna avvikelse, som tidigare nämnts för andra dietregimer eller tillstånd som dieter med hög fetthalt [54,55], indikerar att framtida forskning behövs i naturliga murina modellsystem för att rekapitulera och uppskatta effekten av kostinterventioner på mer komplexa tarm-ekosystem, som hos människor.

cistanche tubulosa-förbättra immunförsvaret
Referenser
1. Candela, M.; Biagi, E.; Turroni, S.; Maccaferri, S.; Figini, P.; Brigidi, P. Dynamisk effektivitet hos människans tarmmikrobiota. Crit. Rev. Microbiol. 2015, 41, 165–171. [CrossRef] [PubMed]
2. Candela, M.; Biagi, E.; Maccaferri, S.; Turroni, S.; Brigidi, P. Intestinal mikrobiota är en plastisk faktor som svarar på miljöförändringar. Trender Microbiol. 2012, 20, 385–391. [CrossRef] [PubMed]
3. Boets, E.; Gomand, SV; Deroover, L.; Preston, T.; Vermeulen, K.; De Preter, V.; Hamer, HM; Van den Mooter, G.; De Vuyst, L.; Courtin, CM Systemisk tillgänglighet och metabolism av kolon-härledda kortkedjiga fettsyror hos friska försökspersoner: En stabil isotopstudie. J. Physiol. 2017, 595, 541–555. [CrossRef] [PubMed] 4. Tan, J.; McKenzie, C.; Potamitis, M.; Thorburn, AN; Mackay, CR; Macia, L. Kortkedjiga fettsyrors roll i hälsa och sjukdom. Adv. Immunol. 2014, 121, 91–119. [PubMed]
5. Kumar, J.; Rani, K.; Datt, C. Molekylär koppling mellan kostfiber, tarmmikrobiota och hälsa. Mol. Biol. Rep. 2020, 47, 6229–6237. [CrossRef] [PubMed]
6. Bilotta, AJ; Cong, Y. Gut mikrobiota metabolitreglering av värdförsvar vid slemhinneytor: Implikation i precisionsmedicin. Precis. Clin. Med. 2019, 2, 110–119. [CrossRef]
7. Rooks, MG; Garrett, WS Tarmmikrobiota, metaboliter och värdimmunitet. Nat. Rev. Immunol. 2016, 16, 341–352. [CrossRef]
8. Rodríguez, JM; Murphy, K.; Stanton, C.; Ross, RP; Kober, OI; Juge, N.; Avershina, E.; Rudi, K.; Narbad, A.; Jenmalm, MC Sammansättningen av tarmmikrobiotan under hela livet, med tonvikt på tidigt liv. Microb. Ecol. Hälsa Dis. 2015, 26, 26050. [CrossRef]
9. Arrieta, M.-C.; Stiemsma, LT; Amenyogbe, N.; Brown, EM; Finlay, B. Tarmmikrobiomet i tidigt liv: hälsa och sjukdom. Främre. Immunol. 2014, 5, 427. [CrossRef]
10. Chung, WSF; Walker, AW; Louis, P.; Parkhill, J.; Vermeiren, J.; Bosscher, D.; Duncan, SH; Flint, HJ Modulering av den mänskliga tarmens mikrobiota av kostfibrer sker på artnivå. BMC Biol. 2016, 14, 3. [CrossRef]
11. Danneskiold-Samsøe, NB; Barros, HDdFQ; Santos, R.; Bicas, JL; Cazarin, CBB; Madsen, L.; Kristiansen, K.; Pastore, GM; Brix, S.; Júnior, MRM Samspel mellan mat och tarmmikrobiota i hälsa och sjukdom. Food Res. Int. 2019, 115, 23–31. [CrossRef] 12. Scott, KP; Duncan, SH; Flint, HJ Kostfiber och tarmens mikrobiota. Nutr. Tjur. 2008, 33, 201–211. [CrossRef]
13. Donohoe, DR; Garge, N.; Zhang, X.; Sun, W.; O'Connell, TM; Bunger, MK; Bultman, SJ Mikrobiomet och butyrat reglerar energimetabolism och autofagi i däggdjurets kolon. Cell Metab. 2011, 13, 517–526. [CrossRef]
14. Gomaa, EZ Mänsklig tarmmikrobiota/mikrobiom i hälsa och sjukdomar: En översyn. Antonie Van Leeuwenhoek 2020, 113, 2019–2040. [CrossRef]
15. Requena, T.; Martínez-Cuesta, MC; Peláez, C. Diet och mikrobiota kopplade till hälsa och sjukdom. Matfunktion. 2018, 9, 688–704. [CrossRef] [PubMed]
16. Ericsson, AC; Franklin, CL Tarmmikrobiomet hos laboratoriemöss: Överväganden och bästa praxis för translationell forskning. Mamma. Genom 2021, 32, 239–250. [CrossRef] [PubMed]
17. Beresford-Jones, BS; Forster, SC; Stares, MD; Notley, G.; Viciani, E.; Browne, HP; Boehmler, DJ; Söderholm, AT; Kumar, N.; Vervier, K. Mus Gastrointestinal Bacteria Catalog möjliggör översättning mellan musens och mänskliga tarmmikrobiotas via funktionell kartläggning. Cell Host Microbe 2022, 30, 124–138.e8. [CrossRef]
18. Fava, F.; Rizzetto, L.; Tuohy, K. Tarmmikrobiota och hälsa: Förbinder aktörer över det metabola systemet. Proc. Nutr. Soc. 2019, 78, 177–188. [CrossRef]
19. David, LA; Materna, AC; Friedman, J.; Campos-Baptista, MI; Blackburn, MC; Perrotta, A.; Erdman, SE; Alm, EJ Värdens livsstil påverkar människans mikrobiota på dagliga tidsskalor. Genome Biol. 2014, 15, 89 kr. [CrossRef]
20. Tanaka, M.; Nakayama, J. Utveckling av tarmmikrobiotan i spädbarnsåldern och dess inverkan på hälsan senare i livet. Allergol. Int. 2017, 66, 515–522. [CrossRef]
21. David, LA; Maurice, CF; Carmody, RN; Gootenberg, DB; Knapp, JE; Wolfe, BE; Ling, AV; Devlin, AS; Varma, Y.; Fischbach, MA Dieten förändrar snabbt och reproducerbart den mänskliga tarmens mikrobiomet. Naturen 2014, 505, 559–563. [CrossRef] [PubMed]
22. García-Montero, C.; Fraile-Martínez, O.; Gómez-Lahoz, AM; Pekarek, L.; Castellanos, AJ; Noguerales-Fraguas, F.; Coca, S.; Guijarro, LG; García-Honduvilla, N.; Asúnsolo, A. Näringskomponenter i västerländsk kost kontra medelhavskost vid samspelet mellan tarmmikrobiota och immunsystem. Konsekvenser för hälsa och sjukdom. Nutrients 2021, 13, 699. [CrossRef] [PubMed]
23. Soverini, M.; Rampelli, S.; Turroni, S.; Schnorr, SL; Quercia, S.; Castagnetti, A.; Biagi, E.; Brigidi, P.; Candela, M. Variationer i den mänskliga tarmmetagenomprofilen efter avvänjning som ett resultat av förvärv av Bifidobacterium i den västra mikrobiomen. Främre. Microbiol. 2016, 7, 1058. [CrossRef] [PubMed]
24. Manzel, A.; Muller, DN; Hafler, DA; Erdman, SE; Linker, RA; Kleinewietfeld, M. Roll av "västerländsk kost" i inflammatoriska autoimmuna sjukdomar. Curr. Allergy Asthma Rep. 2014, 14, 404. [CrossRef] [PubMed]
25. Kleinewietfeld, M.; Manzel, A.; Titze, J.; Kvakan, H.; Josef, N.; Linker, RA; Muller, DN; Hafler, DA Natriumklorid driver autoimmun sjukdom genom induktion av patogena TH17-celler. Naturen 2013, 496, 518–522. [CrossRef] [PubMed]
26. Haase, S.; Wilck, N.; Kleinewietfeld, M.; Müller, DN; Linker, RA Natriumklorid utlöser Th17-medierad autoimmunitet. J. Neuroimmunol. 2019, 329, 9–13. [CrossRef] [PubMed]
27. Hernandez, AL; Kitz, A.; Wu, C.; Lowther, DE; Rodriguez, DM; Vudattu, N.; Deng, S.; Herold, KC; Kuchroo, VK; Kleinewietfeld, M. Sodium chloride hämmar den undertryckande funktionen hos FOXP3+ regulatoriska T-celler. J. Clin. Undersök. 2015, 125, 4212–4222. [CrossRef]
28. Hamad, I.; Cardilli, A.; Corte-Real, BF; Dyczko, A.; Vangronsveld, J.; Kleinewietfeld, M. Diet med hög salthalt inducerar utarmning av mjölksyraproducerande bakterier i murin tarm. Näringsämnen 2022, 14, 1171. [CrossRef]
29. Wilck, N.; Matus, MG; Kearney, SM; Olesen, SW; Forslund, K.; Bartolomaeus, H.; Haase, S.; Mähler, A.; Balogh, A.; Markó, L. Salt-responsiv tarmkommensal modulerar TH 17-axeln och sjukdom. Naturen 2017, 551, 585–589. [CrossRef]
30. Wei, Y.; Lu, C.; Chen, J.; Cui, G.; Wang, L.; Yu, T.; Yang, Y.; Wu, W.; Ding, Y.; Li, L. Diet med hög salthalt stimulerar tarmens Th17-svar och förvärrar TNBS-inducerad kolit hos möss. Oncotarget 2017, 8, 70. [CrossRef]
31. Han, FJ; Li, J.; MacGregor, GA Effekt av måttlig saltminskning på längre sikt på blodtrycket. Cochrane Database Syst. Rev. 2013, 346, f1325. [CrossRef] [PubMed]
32. Hu, L.; Zhu, S.; Peng, X.; Li, K.; Peng, W.; Zhong, Y.; Kang, C.; Cao, X.; Liu, Z.; Zhao, B. Högt salt framkallar hjärninflammation och kognitiv dysfunktion, åtföljd av växlingar i tarmmikrobiotan och minskad produktion av SCFA. J. Alzheimers Dis. 2020, 77, 629–640. [CrossRef]
33. Tubbs, AL; Liu, B.; Rogers, TD; Sartor, RB; Miao, EA Dietsalt förvärrar experimentell kolit. J. Immunol. 2017, 199, 1051–1059. [CrossRef]
34. Muller, DN; Wilck, N.; Haase, S.; Kleinewietfeld, M.; Linker, RA Natrium i mikromiljön reglerar immunsvar och vävnadshomeostas. Nat. Rev. Immunol. 2019, 19, 243–254. [CrossRef] [PubMed]
35. Burr, AH; Bhattacharjee, A.; Hand, TW Näringsmodulering av mikrobiomet och immunsvar. J. Immunol. 2020, 205, 1479–1487. [CrossRef] [PubMed]
36. Roca-Saavedra, P.; Mendez-Vilabrille, V.; Miranda, JM; Nebot, C.; Cardelle-Cobas, A.; Franco, CM; Cepeda, A. Livsmedelstillsatser, föroreningar och andra mindre komponenter: Effekter på mänsklig tarmmikrobiota — En översikt. J. Physiol. Biochem. 2018, 74, 69–83. [CrossRef]
37. Côrte-Real, BF; Hamad, I.; Hornero, RA; Geisberger, S.; Roels, J.; Van Zeebroeck, L.; Dyczko, A.; van Gisbergen, MW; Kurniawan, H.; Wagner, A. Natrium stör mitokondriell andning och inducerar dysfunktionella tregs. Cell Metab. 2023, 35, 299–315.e298. [CrossRef] [PubMed]
38. Zagato, E.; Pozzi, C.; Bertocchi, A.; Schioppa, T.; Saccheri, F.; Guglietta, S.; Fosso, B.; Melocchi, L.; Nizzoli, G.; Troisi, J. Endogen murin mikrobiotamedlem Faecalibaculum rodentium och dess humana homolog skyddar från intestinal tumörtillväxt. Nat. Microbiol. 2020, 5, 511–524. [CrossRef] [PubMed]
39. Mao, G.; Li, S.; Orfila, C.; Shen, X.; Zhou, S.; Linhardt, RJ; Ja, X.; Chen, S. Depolymeriserat RG-I-berikat pektin från citrussegmentmembran modulerar tarmmikrobiota, ökar SCFA-produktionen och främjar tillväxten av Bifidobacterium spp., Lactobacillus spp. och Faecalibaculum spp. Matfunktion. 2019, 10, 7828–7843. [CrossRef]
40. Miranda, PM; De Palma, G.; Serkis, V.; Lu, J.; Louis-Auguste, MP; McCarville, JL; Verdu, EF; Collins, SM; Bercik, P. Hög saltdiet förvärrar kolit hos möss genom att minska Lactobacillus-nivåer och butyratproduktion. Microbiome 2018, 6, 57. [CrossRef]
41. Chen, L.; Han, FJ; Dong, Y.; Huang, Y.; Wang, C.; Harshfield, GA; Zhu, H. Modest natriumreduktion ökar cirkulerande kortkedjiga fettsyror hos obehandlade hypertensiva: En randomiserad, dubbelblind, placebokontrollerad studie. Hypertoni 2020, 76, 73–79. [CrossRef] [PubMed]
42. Lukovac, S.; Belzer, C.; Pellis, L.; Keijser, BJ; de Vos, WM; Montijn, RC; Roeselers, G. Differentiell modulering av Akkermansia muciniphila och Faecalibacterium prausnitzii av värd perifer lipidmetabolism och histonacetylering i mustarmorganoider. MBio 2014, 5, e01438-14. [CrossRef] [PubMed]
43. Dao, MC; Everard, A.; Aron-Wisnewsky, J.; Sokolovska, N.; Prifti, E.; Verger, EO; Kayser, BD; Levenez, F.; Chilloux, J.; Hoyles, L. Akkermansia muciniphila och förbättrad metabol hälsa under en kostintervention vid fetma: Förhållande med tarmmikrobiomrikedom och ekologi. Gut 2016, 65, 426–436. [CrossRef] [PubMed]
44. Llewellyn, SR; Britton, GJ; Contijoch, EJ; Vennaro, OH; Mortha, A.; Colombel, J.-F.; Grinspan, A.; Clemente, JC; Merad, M.; Faith, JJ Interaktioner mellan kosten och tarmmikrobiotan förändrar tarmpermeabiliteten och svårighetsgraden av kolit hos möss. Gastroenterology 2018, 154, 1037–1046.e1032. [CrossRef]
45. Berber, K.; Gerdes, LA; Cekanaviciute, E.; Jia, X.; Xiao, L.; Xia, Z.; Liu, C.; Klotz, L.; Stauffer, U.; Baranzini, SE Tarmmikrobiota från patienter med multipel skleros möjliggör spontan autoimmun encefalomyelit hos möss. Proc. Natl. Acad. Sci. USA 2017, 114, 10719–10724. [CrossRef]
46. Sanchez, JMS; DePaula-Silva, AB; Libbey, JE; Fujinami, RS Dietens roll för att reglera tarmens mikrobiota och multipel skleros. Clin. Immunol. 2022, 235, 108379. [CrossRef]
47. Mak, IW; Evaniew, N.; Ghert, M. Lost in translation: Djurmodeller och kliniska prövningar i cancerbehandling. Am. J. Transl. Res. 2014, 6, 114.
48. Payne, KJ; Crooks, GM Engagemang för immuncellslinje: Översättning från möss till människor. Immunity 2007, 26, 674–677. [CrossRef]
49. Seok, J.; Warren, HS; Cuenca, AG; Mindrinos, MN; Bagare, HV; Xu, W.; Richards, DR; McDonald-Smith, GP; Gao, H.; Hennessy, L. Genomiska svar i musmodeller härmar dåligt mänskliga inflammatoriska sjukdomar. Proc. Natl. Acad. Sci. USA 2013, 110, 3507–3512. [CrossRef] [PubMed]
50. Nguyen, TLA; Vieira-Silva, S.; Liston, A.; Raes, J. Hur informativ är musen för forskning om mänsklig tarmmikrobiota? Dis. Modell. Mech. 2015, 8, 1–16. [CrossRef]
51. Rosshart, SP; Vassallo, BG; Angeletti, D.; Hutchinson, DS; Morgan, AP; Takeda, K.; Hickman, HD; McCulloch, JA; Badger, JH; Ajami, NJ Tarmmikrobiota från vild mus främjar värdkondition och förbättrar sjukdomsresistens. Cell 2017, 171, 1015–1028.e1013. [CrossRef] [PubMed]
52. Suzuki, TA; Phifer-Rixey, M.; Mack, KL; Sheehan, MJ; Lin, D.; Bi, K.; Nachman, MW Värd för genetiska bestämningsfaktorer för tarmmikrobiotan hos vilda möss. Mol. Ecol. 2019, 28, 3197–3207. [CrossRef] [PubMed]
53. Maurice, CF; CL Knowles, S.; Ladau, J.; Pollard, KS; Fenton, A.; Pedersen, AB; Turnbaugh, PJ Markerad säsongsvariation i tarmmikrobiotan av vilda mus. ISME J. 2015, 9, 2423–2434. [CrossRef] [PubMed]
54. Rosshart, SP; Herz, J.; Vassallo, BG; Hunter, A.; Wall, MK; Badger, JH; McCulloch, JA; Anastasakis, DG; Sarshad, AA; Leonardi, I. Laboratoriemöss födda av vilda möss har naturlig mikrobiota och modellerar mänskliga immunsvar. Science 2019, 365, eaaw4361. [CrossRef] [PubMed]
55. Hild, B.; Dreier, MS; Åh, JH; McCulloch, JA; Badger, JH; Guo, J.; Thefaine, CE; Umarova, R.; Hall, KD; Gavrilova, O. Neonatal exponering för en vildhärledd mikrobiom skyddar möss mot dietinducerad fetma. Nat. Metab. 2021, 3, 1042–1057. [CrossRef] [PubMed]
56. Caporaso, JG; Lauber, CL; Walters, WA; Berg-Lyons, D.; Lozupone, CA; Turnbaugh, PJ; Fierer, N.; Knight, R. Globala mönster av 16S rRNA-diversitet på ett djup av miljontals sekvenser per prov. Proc. Natl. Acad. Sci. USA 2011, 108, 4516–4522. [CrossRef] [PubMed]
57. Bolyen, E.; Rideout, JR; Dillon, MR; Bokulich, NA; Abnet, CC; Al-Ghalith, GA; Alexander, H.; Alm, EJ; Arumugam, M.; Asnicar, F. Reproducerbar, interaktiv, skalbar och utbyggbar mikrobiomdatavetenskap med QIIME 2. Nat. Biotechnol. 2019, 37, 852–857. [CrossRef]
58. Callahan, BJ; McMurdie, PJ; Rosen, MJ; Han, AW; Johnson, AJA; Holmes, SP DADA2: Högupplöst provinferens från Illumina amplikondata. Nat. Metoder 2016, 13, 581–583. [CrossRef]
59. Lozupone, C.; Lladser, ME; Knights, D.; Stombaugh, J.; Knight, R. UniFrac: Ett effektivt avståndsmått för jämförelse av mikrobiell gemenskap. ISME J. 2011, 5, 169–172. [CrossRef]
60. Oksanen, J.; Simpson, G.; Blanchet, F.; Kindt, R.; Legendre, P.; Minchin, P.; O'Hara, R.; Solymos, P.; Stevens, M.; Szoecs, E.; et al. Vegan: Community Ecology Package. Version 2.6-4. 11 oktober 2022. Tillgänglig online: https://CRAN.R-project.org/package= vegan (tillgänglig den 26 november 2022).
61. Segata, N.; Izard, J.; Waldron, L.; Gevers, D.; Miropolsky, L.; Garrett, WS; Huttenhower, C. Metagenomisk biomarkör upptäckt och förklaring. Genome Biol. 2011, 12, 60 kr. [CrossRef]
62. Douglas, GM; Maffei, VJ; Zaneveld, JR; Yurgel, SN; Brown, JR; Taylor, CM; Huttenhower, C.; Langille, MG PICRUST2 för förutsägelse av metagenomfunktioner. Nat. Biotechnol. 2020, 38, 685–688. [CrossRef]
63. Neal, B.; Wu, Y.; Feng, X.; Zhang, R.; Zhang, Y.; Shi, J.; Zhang, J.; Tian, M.; Huang, L.; Li, Z. Effekt av saltsubstitution på kardiovaskulära händelser och död. N. Engl. J. Med. 2021, 385, 1067–1077. [CrossRef]
64. Arroyo Hornero, R.; Hamad, I.; Côrte-Real, B.; Kleinewietfeld, M. Effekten av kostkomponenter på regulatoriska T-celler och sjukdomar. Främre. Immunol. 2020, 11, 253. [CrossRef] [PubMed]
65. Wu, GD; Chen, J.; Hoffmann, C.; Bittinger, K.; Chen, YY; Keilbaugh, SA; Bewtra, M.; Knights, D.; Walters, WA; Knight, R.; et al. Koppla samman långsiktiga kostmönster med tarmmikrobiella enterotyper. Vetenskap 2011, 334, 105–108. [CrossRef] [PubMed]
66. Ju, T.; Kong, JY; Stothard, P.; Willing, BP Definierar rollen av Parasutterella, en tidigare okarakteriserad medlem av tarmmikrobiotan. ISME J. 2019, 13, 1520–1534. [CrossRef] [PubMed]
