Inriktning på katepsin B med cykloastragenol förbättrar antitumörimmuniteten hos CD8 T-celler via hämmande av MHC-I-nedbrytning Del 1
Aug 03, 2023
ABSTRAKT
BakgrundFörlusten av tumörantigener och utarmning av CD8 T-celler orsakad av PD-1/PD-L1-vägen är viktiga faktorer för tumörimmunflykt. Under senare år har det skett en ökande forskning om traditionell kinesisk medicin inom tumörbehandling. Cykloastragenol (CAG), en effektiv aktiv molekyl i Astragalus membranaceus, har visat sig ha antivirala, antiaging, antiinflammatoriska och andra funktioner. Dess antitumöreffekt och mekanism är dock inte klarlagda.
Glykosid av cistanche kan också öka aktiviteten av SOD i hjärt- och levervävnader och avsevärt minska innehållet av lipofuscin och MDA i varje vävnad, effektivt rensa upp olika reaktiva syreradikaler (OH-, H₂O₂, etc.) och skydda mot DNA-skador orsakade av OH-radikaler. Cistanche-fenyletanoidglykosider har en stark rensande förmåga av fria radikaler, en högre reducerande förmåga än vitamin C, förbättrar aktiviteten av SOD i spermiesuspension, minskar innehållet av MDA och har en viss skyddande effekt på spermiemembranets funktion. Cistanche-polysackarider kan öka aktiviteten av SOD och GSH-Px i erytrocyter och lungvävnader hos experimentellt åldrande möss orsakade av D-galaktos, samt minska innehållet av MDA och kollagen i lungor och plasma, och öka innehållet av elastin, har en god renande effekt på DPPH, förlänger hypoxitiden hos åldrande möss, förbättrar aktiviteten av SOD i serum och fördröjer den fysiologiska degenerationen av lungor hos experimentellt åldrande möss. Med cellulär morfologisk degeneration har experiment visat att Cistanche har den goda antioxidantförmågan och har potential att vara ett läkemedel för att förebygga och behandla åldrande hudsjukdomar. Samtidigt har echinacoside i Cistanche en betydande förmåga att avlägsna DPPH-fria radikaler och har förmågan att avlägsna reaktiva syrearter och förhindra friradikal-inducerad kollagennedbrytning, och har även en god reparationseffekt på anjonskada av tymin-fria radikaler.

Klicka på cistanche för- och nackdelar
【För mer information:george.deng@wecistanche.com / WhatApp:8613632399501】
MetoderAntitumöreffekten av CAG undersöktes i MC38- och CT26-mustransplanterade tumörmodeller. Antitumöreffekten av CAG analyserades ytterligare via encells multi-omics-sekvensering. Målresponsiv tillgänglighetsprofileringsteknik användes för att hitta målproteinet för CAG. Därefter undersöktes antitumörmekanismen för CAG med användning av konfokal mikroskopi, immunoutfällning och transfektion av mutanta plasmider. Slutligen undersöktes den kombinerade antitumöreffekten av CAG- och PD-1-antikroppar i möss eller organoider.
ResultatVi fann att CAG effektivt hämmade tumörtillväxt in vivo. Vår encelliga multi-omics-atlas visade att CAG främjade presentationen av tumörcellsytantigener och kännetecknades av den förbättrade dödande funktionen hos CD8 plus T-celler. Mekanistiskt band CAG till sitt målprotein cathepsin B, vilket sedan hämmade den lysosomala nedbrytningen av huvudhistokompatibilitetskomplex I (MHC-I) och främjade aggregatet n av MHC-I till cellmembranet, vilket ökade förstationen av tumörantigenet . Samtidigt förbättrade kombinationen av CAG med PD-1-antikropp effektivt tumördödande tumördödande CD8 plus T-celler i xenograftmöss och organoider av kolorektal cancer. Slutsats Våra data rapporterade för första gången att cathepsin B-nedreglering ger antitumörimmunitet och exp daterar antitumörmekanismen för naturlig produkt CAG.
INTRODUKTION
Kolorektal cancer är en av de vanligaste cancerformerna i världen. Dess incidens och dödlighet rankas bland de tre bästa, vilket allvarligt hotar människors liv och hälsa.1 Vanliga behandlingsmetoder inkluderar kirurgiska kemoterapi och strålbehandling, riktade läkemedel och immunterapi.2–4 Men cancerceller uppvisar vanligtvis förlust av ytantigener och uttrycker höga nivåer av hämmande molekyler för att undkomma övervakningen av immunceller. Därför, för att lösa problemet med tumörimmunflykt, har forskare utvecklat immunkontrollpunktshämmare och neoantigenterapi för att blockera maskeringen av cancerceller till immunceller.5–8 Även om immunkontrollpunktshämmare kan återställa de utarmade immuncellerna, cancerns ytantigen. celler har inte påverkats nämnvärt. Därför är det särskilt viktigt att hitta läkemedel som kan främja presentationen av tumörytantigen. Igenkännandet av cancerceller av cytotoxiska CD8 plus T-celler beror på TCR/CD3/major histocompatibility complex (MHC-I)-vägen. TCR tar emot antigenet som finns i dendritiska cellen/cancercellsmembranproteinet CI och sänder signalen för att tätt koppla CD3, som sedan sträcker sig djupare in i cytoplasman.9 10 Samtidigt, med aktiveringen av CD28/B7-signalen , CD8 plus T-celler kan samaktiveras för att känna igen och döda cancerceller.11 Nyligen genomförda studier har funnit att lysosomer i processen med tumörprogression resulterar i en minskning av MHC-I-aggregation på ytan av cancerceller, vilket inte fungerar effektivt närvarande antigener.12 13 Liu et al rapporterade att hämning av PCSK9 kan förhindra nedbrytning av MHC-I i lysosomer och göra det möjligt för MHC-I att återvända till cellmembranet för att presentera antigener.12 Därför återställer den antigenpresenterande funktionen MHC-I är särskilt viktigt för att blockera tumörimmunflykt.
Ett ökande antal studier har visat att tillämpningen av aktiva molekyler från traditionell kinesisk medicin och antitumörintervention har stora möjligheter.14 15 Cykloastragenol (CAG) är en effektiv aktiv molekyl n Astragalus membranaceus, som har antivirala, antibakteriella, anti- inflammatoriska och andra farmakologiska effekter, men dess antitumöreffekt rapporteras sällan.16–19 I denna studie fann vi att CAG hämmade tillväxten av transanterade tumörer av tjocktarmscancertumörer. Mekanismen innebar främst att hämma nedbrytningen av MHC-I, förmedlad av cathepsin B (CTSB), som främjar antigenpresentationen av cancerceller och förbättrar sedan avdödningsförmågan hos CD8 plus T-celler.
MATERIAL OCH METODER
Antikroppar och reagens
CAG was obtained from Yongjian Pharmaceutical Technology (Jiangsu, China, purity >99 procent). Antikroppar av CTSB (Cat#12216-1-AP, PRID: AB_2086929), HLA (Cat#15240-1-AP, PRID: AB_1557426 ), Actin (Cat#{{ 5}}Ig, PRID: AB_2782959 ), Tubulin (Cat#10094-1-AP, PRID: AB_2210695 ), och Anti-mus/kanin Immunohistochemistry Detection Kit (Cat#PK10006) köptes från Proteintech. Antikroppar av H2-Kd (Cat#sc-53852, PRID: AB_784514), LAMP1 (Cat#sc- 20011, PRID: AB_626853), och CTSB (Cat#sc-365558, PRID: AB_10842446) köptes från Santa Cruz Biotechnology. Antibody of Ki-67 (Cat#12202, PRID: AB_2620142) köptes från Cell Signaling Technology. Antikropp av Na/K ATPas (Cat# ab3528, RRID: AB_303877) köptes från Abcam. Flödescytometriantikroppar av CD45-V500 (Cat#561487, RRID: AB_1069704 6), CD3-APC (Cat#345767, RRID: AB_2833003) och CD{ {31}}PerCP (Cat#345774, RRID: AB_2868802 ) köptes från BD Bioscience. Flödescytometriantikropp av Gzmb-FITC (Katnummer 515403, RRID: AB_2114575) köptes från BioLegend. Flödescytometriantikroppar av NK1.1-PE-Cy7 (Cat#25-5941-81, RRID:AB_469664) och IFN- -PE (Cat#12-7311-81, RRID :AB_466192) köptes från Thermo Fisher Scientific. DMEM-medium (Cat#01-052-1ACS), PenicilinStreptomycin (Cat#15140122) och fetalt bovint serum (Cat#C04001-500) köptes från Biological Industries. Getserum (Cat#88RNG001) och Pierce BCA proteinanalyskit (Cat#23225) köptes från Thermo Fisher Scientific. Antikropparna av anti-human PD-1 (Cat#BE0188, RRID: AB_1095031 8) och anti-mus PD-1 (Cat#BE0146, RRID: AB_1094905 3) köptes från Bio X cell. MACS Tumor Tissue Dissociation Kit (Cat#130-095-929) köptes från Miltenyi Biotec.
Cell kultur
Koloncancercellinjer från mus MC38 och CT26 bibehölls i vårt laboratorium.20 De humana tjocktarmscancer-l-linjerna HCT-116 erhölls från Type Culture Collection av Chinese Academy of Sciences (Shanghai, Kina). MC38-, CT26- och HCT-116-cellerna odlades i ett DMEM-medium innehållande 10 procent fetalt bovint serum och 1 procent penicillin/streptomycin vid 37 grader i en 5 procent CO2-inkubator.
Transplantationstumörexperiment
Sex-åtta veckor gamla C57BL/6JGpt honmöss, BALB/c möss och BALB/,c nakna möss köptes från GemPharmatech (Nanjing, Kina). MC38 eller CT26 cancerceller (1×106) ympades subkutant i varje mus. När tumören växer till 100 mm3 delades mikrofonen slumpmässigt in i fosfatbuffrad saltlösning (PBS) grupp (t.ex. en gång om dagen) och CAG-gruppen (t.ex. 50 mg/kg en gång om dagen). Tumörvolymer bestämdes genom tjockleksmätning med formeln V=längd×bredd2/2. När tumörvolymen hos möss i PBS-gruppen nådde 1000 mm3 togs tumören från möss ut, fotograferades och vägdes.

Encellsdissociation från musen för encellig RNA/ATACseq
Fasta tumörer från möss spjälkades med användning av Tumor Dissociation Kit för att erhålla encelliga enkelceller. Enkla celler Encelliga celler med en koncentration av 1000 celler/1000 celler laddade på 10×genomics kromkontrollern encelliga enkelceller enligt 10×genomics tillverkarens protokoll. Omvänd transkriptionsreagens, streckkodade gelkulor och partitioneringsolja blandades med cellerna för gen för att generera gelkulor i emulsioner (GEM) för omvänd transkription. scRNA-seq data förbearbetning och qua y kontroll.
Baserat på musreferensgenomet GRCm38 (mm10), CellRanger V.4.0.0 pipeline (10×Genomics) för att bearbeta encellig RNA sekvensdata för varje experiment (GSE197229). Digitala genuttrycksmatriser sattes in i R (V.4.0.4) med Seurat-paketet (V.4.0.0).21 Innan dBeforem-analys filtrerades cellerna med UMI-nummer (<100,000 UMIs), gene number (<6500 genes), and mitochondrial gene percentage ('percentage. MT'less than 10%). Normalization was performed with the SCTransform function with regression of percentage the of mitochondrial genes.22 For integration, 2000 shared highly variable genes were identified using the t SelectIntegrationFeatures function.23 Integration anchors were identified based on these genes using the FindIntegrationAnchors34 function with an'SCT'normalization method. The data were then integrated using the IntegrateData function. Principal component analysis (PCA) and t-distributed stochastic neighbor embedding (t-SNE) dimension reduction with the top 30 principal components were performed. A nearest-neighbor graph using the 30 dimensions of the PCA reduction was calculated using FindNeighbors, followed by clustering using FindClusters with a resolution of 0.8. Candidate Marker genes for each cell cluster were identified by the FindAllMarkers function. For each cluster of cells, up-specific differentially expressed genes were identified using the Wilcoxon Rank Sum test as implemented in FindAllMarkers.
SeaTac-seq dataförbehandling och kvalitetskontroll
Encells ATAC-seq-data (GSE197229) förbehandlades av cell ranger-at (V.2.0.0) med count-kommandoraden. För den efterföljande scATAC-seq databearbetningen och analysen använde vi ArchR (V.1.0.1)-paketet.24 Sedan använde vi funktionen addArchRGethe nome ('mm10') för genomannotering och skapade en pilfil med funktionen cre ArrowFiles med standardparametrarna. Därefter använde vi filterDoublets-funktionen för att ta bort potentiella dubbletter och skapade ett ArchR-projekt med ArchRProject-funktionen med standardparametrar. Vi använde sedan Harmony-paketet för att ta bort batcheffekten av addHarmony-funktionen.25 För dimensionsreduktion använder vi funktionen addIterativeLSI i ArchR för att köra med def t-parametrarna. För encellsinbäddning valde vi reduceradDims-objektet med harmoni och använde addTSNE-funktionen med parametern 'perplexity=30' för visualisering.
Integrerad analys av siRNA-seq och scATAC-seq data
To integrate scATAC-seq data with matched scRNA-seq data, we first used the FindTransferAnchors function from the Seurat package and aligned the data with the addGeneIntegrationMatrix function in ArchR with 'unconstrained integration' mode. From the result, we found that most of the predicted scores were>0.5. För att förbättra noggrannheten i förutsägelserna för att bättre integrera de två datamängderna, integrerade vi återigen scATAC-seq och scRNA-seq-data med hjälp av "begränsad integration"-läget. Kortfattat kommenterade vi scATAC-seq-data med celltyper baserat på genpoängen för scATAC-seq. Sedan skapade vi en begränsad lista så att genuttryckslikhet endast beräknades i samma celltyp för både scATAC-seq och scRNA-seq. Oövervakad klustring med t-SNE avslöjade 13 subcellkluster, som kommenterades av kända eller förmodade markörer i tilläggstabell 1 online.
Pseudotidslinjebana
Cellhärkomstbanan för cancerceller härleddes genom att använda Monocle2 (V.2.18.0) R-paket.26 Monocyter lär sig den explicita huvudgrafen från encellig genomikdata genom Reversed Graph Embedding för att sortera celler och på så sätt lösa komplexa biologiska processer robust och exakt.27 Vi använde funktionen ''differentialGeneTest'' för att härleda DEG från varje kluster, och efter att ha konstruerat cellbanan upptäckte vi de differentiellt uttryckta generna under pseudotiden. Alla pseudotidsberoende gener visualiserades av plott_pseudotime_heatmap-funktionen som tog ett CellDataSet-objekt. Linjebana plots och jämna uttryckskurvor baserade på CellDataSet genererades av plott_cell_trajectory och plot_gener_i_pseudotime, respektive.28
Encellskopieringsnummervariantsamtal
För att identifiera maligna celler med klonala storskaliga kromosomala kopietalsvariationer (CNV), använde vi inferCNV R-paketet för att härleda de genetiska profilerna för varje cell baserat på det genomsnittliga uttrycket av stora genuppsättningar i varje kromosomal region av tumörgenomet jämfört med normala celler.29 På prov för prov användes immuncellerna som referens för att uppskatta CNV i de cancerrelaterade cellerna.
Anrikningsanalys
KEGG-väg- och GO-anteckningsanalyser utfördes med R-paketet clusterProfiler (V.3.11.1) med parametrarna PValueCutoff=0.05, PAdjustMethod=BH, QValueCutoff{{6} }.05, MingsSize=10 och MaxGSSize=500.20Genuppsättningsanrikningsanalys (GSEA) användes med hjälp av 50 känneteckengenuppsättningar (h.all.V.7.4.symbols. gmt) för att identifiera signifikant berikade funktionella vägar via GSEA-mjukvara (V.4.1.0), med screeningkriterier med nominellt P-värde<0.05and false discovery rate q<0.250.30
Kvantitativ PCR-analys i realtid
MC38- och HCT-116-celler såddes i plattor med sex brunnar under 6 timmar och behandlades sedan med CAG i ytterligare 24 timmar. Cellerna tvättades tre gånger med kall PBS och centrifugerades vid 18 0g i 5 minuter vid 4 grader. Samtidigt, efter slipning av tumörvävnaden. Totalt RNA extraherades från MC38, HCT-116-celler och tumörvävnad med hjälp av TRIzol-reagenset, enligt tillverkarens instruktioner. Reaktionsvolymen var 20 µL innehållande: 1 µg RNA, 5 µL 5×Hiscript III qRT SuperMix och RNase Free dH2 O. cDNA:t utsattes för kvantitativ PCR, med en reaktionsvolym på 10 µL med 1 µL cDNA, 5 µL qPCR5 mixer, 5 µL qPCR5 mixers. (Framåt och bakåt), och 3,25 µL RNas-fri dH2O. Primerna syntetiserades av GenScript Biotech Corporation (Nanjing, Kina) enligt följande sekvenser (online tilläggstabell 2).
Målupptäckt via en målkänslig tillgänglighetsprofilering
Screeningen av CAG-bindande proteiner utfördes som beskrivits tidigare.31 32 Kortfattat användes den målkänsliga tillgänglighetsprofileringsmetoden (TRAP) för att upptäcka bindningsproteinerna för CAG i cellmiljön genom att övervaka lysininducerad ligandengagemang tillgänglighetsförändringar på proteomnivå. Kortfattat behandlades två skålar med celler med 10µM CAG respektive dimetylsulfoxid (DMSO). Efter 1-timmes inkubation permeabiliserades cellerna av M-PER-buffert (Thermo Scientific) och de resulterande lysaten märktes kovalent genom tillsats av formaldehyd och boran-pyridinkomplex som tillsammans specifikt märker proteinhaltiga lysinrester vid rumstemperatur för tillgänglighetsprofilering . Sedan fälldes lysaten ut med organiskt lösningsmedel och de uppsamlade pelletarna återupplöstes i 8 mol/L urea, reducerat med ditiotreitol (DTT) vid 56 grader i 30 minuter, följt av alkylering med användning av jodacetamid (IAA) i mörker under 30 minuter. En lämplig mängd DTT-lösning tillsattes igen för att reagera med överskott av IAA. Därefter späddes proteomet med ammoniumbikarbonatlösning tills den slutliga koncentrationen av urea når 1 mol/L. De uppsamlade proteinspjälkningarna avsaltades på C18 HLB-kolonner (Waters, Milford, Massachusetts, USA), och de anrikade peptiderna torkades och rekonstituerades i 0,1 procent myrsyra (FA) vattenlösning. AnanoLCSYNAPT G2 Si Q-TOF-system (Waters) användes för att analysera proverna för kvantitativ profilering av lysintillgänglighetsförändringarna som svar på CAG-bindning för målupptäckt. Databeroendeinsamling i det positiva läget användes för datainsamling. Dataanalys utfördes med användning av PEAKS Studio V.8.5 (BSI Solutions, Waterloo, Kanada). Specifikt valdes cys-alkylering som en fast modifikation, och metioninoxidation och lysindimetylering, uppnådd genom TRAP-märkning, sattes som variabla modifieringar. Kortfattat tillskrevs peptider som innehåller TRAP-inducerad dimetylering och uppvisade signifikanta överflödsförändringar med och utan CAG-inkubation som målkänsliga peptider. Förhållandet mellan mängden av varje TRAP-märkt peptid indikerar graden av tillgänglighetsförändring och är intimt associerad med ligandbindande affinitet. Students t-test utfördes för att bedöma om de detekterade tillgänglighetsförändringarna för märkta peptider är statistiskt signifikanta. Ett intergrupps p-värde (s<0.001) and R-value (TRAP ratio > 2 or <0.5) were set as the cut-off to screen the target responsive peptides belonging to the CAG binding proteins from the whole quantified proteome.

Organoid kultur
De mänskliga organoiderna av kolorektal cancer konstruerades och odlades av Chongqing Kingbiotech.33 Patientvävnadsprover som förvärvats genom den kirurgiska operationen maldes i så små bitar som möjligt med steril sax. Vävnadsbitarna blandades noggrant med Matrigel (Corning, Cat#356231) i det ungefärliga förhållandet 1:4 på is. Den efterföljande behandlingen avsåg publicerade protokoll. Kortfattat såddes bitarna-Matrigel-suspensionerna snabbt i flerbrunnsplattan för att bilda halvsfäriska droppar och överfördes till 37 grader i 15–20 minuter, vilket gjorde att dropparna kunde stelna. Tillsatte lämplig mängd odlingsmedium (KingcultureTM Organoid Growth Medium, Cat#KCW-2) till varje brunn och bytte medium varannan till var fjärde dag.
Isolering och odling av humana CD8 T-celler
Tillsätt samma volym normal saltlösning till det perifera blodet hos friska personer som innehåller antikoagulantia för att späda ut helblodet. Tillsätt en viss volym separationslösning till ett 15 ml centrifugrör, tillsätt långsamt det utspädda helblodet längs rörväggen till toppen av separationslösningen och centrifugera vid 750 g i 20 minuter. Efter centrifugering, använd en pipett för att försiktigt suga in monocyterna i det mellersta vita lagret i ett 15 ml centrifugrör, tillsätt en viss volym PBS för att återsuspendera, centrifugera 250 g i 5 minuter och kassera supernatanten. Efter tillsats av humana CD8 magnetiska pärlor till cellfällningarna, sorterades CD8 T-celler genom LS-sorteringskolonn. CD8 T-celler sattes till den perforerade plattan förbelagd med 5 µg/mL CD3 (Thermo Fisher Scientific Cat# 16-0032-38, RRID: AB_2865578) antikropp och sedan 10 ng/ml IL{{15} } (Peprotech Cat# 212-12) och 5 µg/mL CD28 (Thermo Fisher Scientific Cat# 16-0281-81, RRID: AB_468920) funktionella antikroppar tillsattes odlade i 24 timmar.
Samkultur
Efter att organoiderna inkuberats med CAG i 24 timmar, ersattes det färska odlingsmediet, och sedan suspenderades organoiderna och aktiverade CD8 T-celler i matrisgelen, sedan sattes suspensionen till sex-brunnars plattan och placerades i 37 graders inkubator i 15 minuter, och sedan tillsattes 2 ml serumfritt komplett odlingsmedium under 24 timmar.
Väst blot
MC38- och HCT-116-celler såddes i plattor med sex brunnar under 6 timmar och behandlades sedan med CAG i ytterligare 24 timmar. Cellerna tvättades tre gånger med kall PBS och centrifugerades vid 180 g under 5 minuter vid 4 grader. Det totala proteinet lyserades med WB-IP-lys innehållande 1 procent proteashämmare under 30 minuter på is. Totalt protein utvärderades med användning av ett BCA-proteinkvantifieringskit. Proteinprover separerades med 10 procent –12 procent SDS polyakrylamidgelelektrofores och överfördes till PVDF (polyvinylidenfluorid) membran vid 350 mA under 90 minuter. PVDF-membranen blockerades med 5 procent BSA under 1 timme, remsorna med den angivna primära antikroppen över natten och med den sekundära antikroppen inkuberad i 90 minuter vid rumstemperatur. Slutligen detekterades remsorna med användning av ett LumiGLO kemiluminescerande substratsystem (KPL, Gaithersburg, Maryland, USA).
Flödescytometri
Efter digestion av tumörvävnad och encellsuspensionen framställdes. Ytfärgning utfördes med ytantigenantikroppar i FCM (Flow Cytometry)-bufferten (PBS innehållande 1 procent FBS) och färgades på is med lämpliga antikroppar i 30 minuter. Reaktiva färgämnen (eBioscience) användes för att eliminera döda celler. Intracellulär cytokinfärgning utfördes med BD-cellfixativ lösning/extracellulär membranlösning, och cellerna fixerades och genomträngdes och färgades sedan med antikroppar mot cytokiner i Perm/Wash-buffert (BD Biosciences).
CTSB mutantplasmider transfekterade
HCT-116-celler såddes i 6-brunnsplattor i 12 timmar och transfekterades sedan med CTSB-WT-EGFP- eller CTSB-mutantplasmider (Y75A, A77V och G198A) under 36 timmar.
Transfektionsinterferens eller överuttrycksplasmid av CTSB till MC38-celler eller HCT-116-celler
MC38-celler (1×106/brunn) inokulerades i 6-brunnsplattor i 6 timmar, transfekterades sedan med CTSB-störande RNA (sekvens: Forward-GGACAUAGAUCUACCUGAATT och Reverse-UUCAGGUAGAUCUAUGUCCTT) i 48 timmar, och mRNA- eller proteinuttrycksnivåerna av Ctsb och H2-k1 upptäcktes. HCT-116-celler (1×106/brunn) inokulerades i 6-brunnsplattor i 6 timmar, transfekterades sedan med CTSB-interferens (sekvens: GCTGGTCA ACTATGTCAACAA) eller överuttrycksplasmid i 48 timmar, och mRNA:t eller proteinuttrycksnivåer av CTSB och HLA-A detekterades.
Dockningsteknik
3D-strukturen för CTSB laddades ner från proteindatabasen (PDB ID: 2iPP), och strukturerna för CAG laddades ner från PubChem. Dockningsprocessen utfördes i Autodock 2 med grov dockning med hjälp av en simulerad glödgningsalgoritm och en efterföljande förfining med en genetisk algoritm.
Cellulär termisk skiftanalys
MC38-cellerna såddes i 10cm plattor över natten och behandlades sedan med CAG eller 0,1 procent DMSO i ytterligare 2 timmar. Cellerna uppsamlades, tvättades med kall PBS och centrifugerades vid 180 g under 5 min. Cellerna delades sedan jämnt upp i centrifugeringsrör (70 µL varje rör) och värmdes i 3 minuter vid följande temperatur: 46, 49, 52, 55, 58, 61, 64 och 67 grader, proverna kyldes i 3 minuter vid temperaturer och höll sedan på is. Därefter placerades proverna i ett kylskåp vid -80 grader över natten. Proverna tinades vid rumstemperatur i 30 minuter och kyldes sedan vid -80 grader i 4 timmar. Slutligen centrifugerades proverna vid 12, 000 g i 25 minuter, supernatanten sattes till laddningsbufferten och analyserades med Western blotting.
Immunhistokemisk färgning
Paraffinsnitt av tumörvävnad nedsänktes i xylen i 20 minuter för att avvaxa och sedan i 100 procent, 75 procent och 50 procent etanol i 10 minuter. Efter att skivorna utsatts för antigenreparation med natriumcitratantigenreparationslösning, inaktiverades den endogena väteperoxiden med 3 % väteperoxid. Efter blockering med 5 procent getserum under 1 timme tillsattes anti-Ki67-antikroppen (1:200) och inkuberades över natten vid 4 grader. Den antimus/kanin-HRP-märkta polymeren (100 µL) tillsattes och prover inkuberades vid 37 grader i 30 minuter, följt av 100 µL DAB-arbetslösning och inkubering vid rumstemperatur i 5 minuter. Efter 1 minuts färgning med hematoxylin tvättades proverna i 50 procent, 75 procent och 100 procent etanol och xylen i 5 minuter, och neutralt gummi användes för att försegla filmen. Filmen observerades och fotograferades under ett mikroskop.
Statistiskanalys
Statistisk analys utfördes med programvaran GraphPad Prism (V.8.0). Alla resultat uttrycks som medel ±SEM för tre oberoende experiment. En enkelriktad variansanalys följt av Dunnetts post hoc-test användes för att utvärdera skillnaderna när det fanns fler än två grupper. Students t-test användes för att utvärdera den signifikanta skillnaden mellan de två grupperna. En statistisk signifikans sattes till sid<0.05.
RESULTAT
Encellig multi-omics-analys av CAG som hämmar tillväxten av transplanterad tjocktarmscancer hos möss
För att undersöka om CAG har en antitumöreffekt transplanterade vi först MC38-cancerceller till C57BL/6-möss. Vi noterade att CAG signifikant hämmade tillväxten av tumörer (online kompletterande figur S1A, B). Därefter transplanterade vi CT26-celler till BALB/c-möss och fann att CAG också hämmade tillväxten av tumörer (online tilläggsfigur S1C, D).

För att ytterligare avslöja den specifika mekanismen genom vilken CAG hämmar tumörtillväxt, analyserade vi den med hjälp av scRNA-seq och scATAC-seq-teknikerna (figur 1A). Vi delade upp cellpopulationen i fyra grupper: cancerceller, fibroblaster, myeloidceller och lymfocyter (figur 1B, online kompletterande figur S2A, B). Vi fann att cancerceller (52 procent) och fibroblaster (41 procent) huvudsakligen infiltrerades i tumörvävnader, medan immunceller endast stod för 7 procent. Vi delade sedan upp cancerceller i åtta undergrupper och fibroblaster i tre undergrupper (figur 1C–E). Därefter visade anrikningsanalysen av starkt uttryckta gener i varje cellpopulation att MHC-I molekylära vägar i cancerceller berikades, liksom antitumörsignalerna från T-celler och NK-celler (online tilläggsfigur S2C). Sedan hittades också fyra grupper av celler med användning av scATAC-seq och scRNA-seq integrationsanalys (figur 2D-G). Efter jämförelsen fann vi att cancerceller (C01-, C03-celler), CD8 plus T-celler, Spp1 plus TAM-celler och fibroblaster (F01- och F02-celler) uppträdde i ATAC-sekvensering (figur 1F, G) och uttrycktes vidare i hög grad transkriptionsfaktorer anrikades i dessa celler (figur IH). Genom dessa analyser spekulerar vi att hämningen av tumörtillväxt av CAG är nära relaterad till förändringar i dessa celler.
Cag främjar tumörcellantigenpresentation
För att analysera antitumörmekanismen för CAG analyserade vi först tumörcellpopulationen och delade upp cancercellerna i åtta undergrupper (figur 2A, B, kompletterande figur S3A online). Resultaten visade att, jämfört med PBS-gruppen, minskade C05-gruppcellerna signifikant medan C07-gruppcellerna ökade (figur 2C). Under tiden, för att verifiera noggrannheten i vår tumörcellklustring, jämförde vi CNV för lymfocyter och myeloidceller som referensceller. Resultaten visade att CNV för cancerceller var signifikant högre än för immunceller (online tilläggsfigur S3B). När vi analyserade undergrupperna av cancerceller fann vi att interferonsvarsgenerna Isg15, Irf7, Ifit3 och Ifi47 uttrycktes starkt i C07- och C08-cellpopulationerna i CAG-gruppen jämfört med PBS-gruppen (online tilläggsfigur S3C). Analysen av tumörcellpopulationen fann att antigenpresentationsrelaterade vägar var signifikant berikade i multipla cellpopulationer. Därför spekulerar vi att CAG kan främja antigenpresentationen av cancerceller för att spela en antitumörroll (figur 2D). Sedan valde vi de antigenpresentationsrelaterade generna och fann att uttrycksnivån i CAG-gruppen var signifikant högre än den i PBS-gruppen (figur 2E, tilläggsfigur S3D online). Vi fann också att CAG främjade antigenpresentation i tumörvävnader (figur 2F, G).

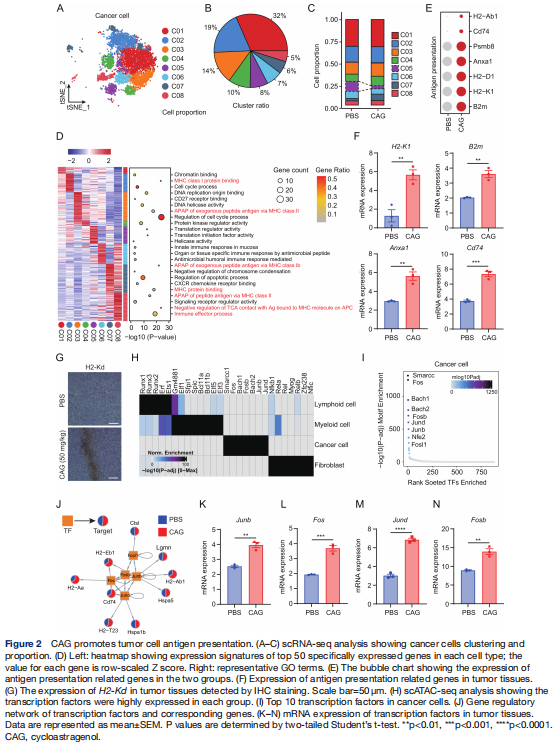
Därefter använde vi scATAC-seq för att analysera de specifika orsakerna bakom CAG-främjande presentation av tumörcellantigen. Vi fann att tumörcellpopulationen i hög grad uttryckte transkriptionsfaktorerna Fos, Junb, Jund, Fosb och Fosl1 (figur 2H, I). Därefter konstruerade vi en karta över interaktionen mellan transkriptionsfaktorer och motsvarande gener för att förklara att CAG främjade uttrycket av tumörcellantigenpresenterande relaterade gener (figur 2J). I tumörvävnader fann vi också att transkriptionsfaktorerna Junb, Fos, Jund och Fosb var signifikant överuttryckta i PBS-gruppen under CAG-behandling (figur 2K-N, online-tilläggsfigur S3E-I). Hittills har vi funnit att CAG kan främja uttrycket av transkriptionsfaktorer av antigenpresenterande relaterade gener, och därigenom förbättra den antigenpresenterande funktionen hos cancerceller. Hur dessa cancerceller svarar på immuncellssvar är dock oklart.
För att avslöja fenomenet genom vilket CAG främjar antigenpresentationen av cancerceller, utförde vi banaanalys för att undersöka hur cancerceller förändrar varandra som svar på immuncellssvar. Vi fann att C07-cancerceller över tiden transformerades till C05-, C06- och C08-celler, och genberikning visade också att cancerceller skulle omvandlas till antigenpresentation (figur 3A–E).
CAG förbättrar immuncellers dödande funktion
Dessa resultat visar att CAG kan presentera tumörcellsantigener, så kommer en förbättring av tumörcellantigenpresentationen att leda till förbättring av immuncellsfunktionen? För att ta reda på detta analyserade vi lymfocyter respektive myeloidceller. Resultaten visade att CAG främjade infiltrationen av CD8 plus T-celler i tumörvävnader, och infiltrationen av CD8 plus T-celler och NK-celler ökades också, detekterade med flödescytometri (online kompletterande figur S4A-F). Vi observerade också att CAG förbättrade uttrycket av Ifitm2-, Cxcr6- och S100a6-gener i CD8 plus T-celler,
Fcer1g-, Gzmb-, AW112010- och Zfp36i2-gener i NK-celler och Nfkbia- och Junb-gener i CD4 plus T-celler (online tilläggsfigur S4G). Uttrycket av Ifng och Gzmb i CD8 plus T-celler förbättrades också signifikant, vilket detekterades med flödescytometri (online tilläggsfigur S4H, I). Vidare fann vi att efter CAG-behandling minskade uttrycket av de hämmande receptorerna Lag3, Tigit och Havcr2 på ytan av CD8 plus T-celler och uttrycket av generna Cd28, Cd69, Gzmk, Ccl5 och Pdcd1, som karakteriserar aktivering av CD8 plus T-celler, ökade signifikant (online tilläggsfigur S4J). För att ytterligare verifiera att CAG förbättrade dödandefunktionen hos CD8 plus T-celler genom att främja förbättrad tumörantigenpresentation, transplanterade vi CT26-celler till transplanterade tumörer i nakna möss och observerade att CAG inte effektivt kunde hämma tillväxten av tumörer (online tilläggsfigur S4K-M ).
Efter detta analyserade vi myeloidceller och fann att Spp1 plus TAM-celler ökade efter CAG-behandling, medan antalet C1qc plus TAM-celler minskade och antalet Il1b plus monocyter ökade (online kompletterande figur S5A-D). Efter CAG-behandling var Spp1 plus TAM- och C1qc plus TAM-celler mer mottagliga för pro-inflammatorisk TAM-transformation. Anrikningsanalys fann att den huvudsakligen fokuserade på Tnf-, Ifn-g och signalvägen för inflammatorisk respons (online tilläggsfigur S5E-H). Baserat på de ovan nämnda resultaten drar vi slutsatsen att CAG förbättrar immuncellers igenkänning och dödande funktion genom att främja antigenpresentation i cancerceller. Hur CAG regleras är dock inte klart.
Upptäckt av CAG-målproteinet CTSB genom fälla
Därefter kommer vi att undersöka det specifika CAG-målproteinet som spelar en antitumörroll. Vi valde cancerceller som forskningsobjekt eftersom vi fann att CAG kan förbättra antigenpresentationen av cancerceller och därigenom förbättra immuncellers dödande funktion. Vi syntetiserade först biotinderivatet av CAG och fann att endast 3-OH kunde reagera (online tilläggsfigur S6A). Vi undersökte sedan om CAG-biotin också främjar uttrycket av antigenpresentationsrelaterade gener i mus-MC38-tumörcellinjen. Resultaten visar att CAG-biotin inte påverkade uttrycket av H2-K1-, Cd74- och Anxa1-gener (online tilläggsfigur S6B-D).
Därför använde vi den tidigare TRAP-målsökningsmetoden i laboratoriet.32 CAG och DMSO inkuberades båda med MC38-cellinjen (figur 4A). Vi valde proteinet med FC större än eller lika med 2 och ap Mindre än eller lika med 0.05 som kandidatmålprotein för CAG. Efter principen att bindningen av små molekyler till proteiner kommer att leda till den låga märkningseffektiviteten av lysin, valde vi CTSB för studien (figur 4B). Därefter använde vi cellulär termisk skiftanalys (figur 4C) och mikroskala termofores (MST) (figur 4D) för att verifiera bindningen mellan CAG och CTSB, och fann att affiniteten mellan CAG och CTSB var 26,6 nM (figur 4D). Därefter förutspådde vi bindningsställena mellan CAG och CTSB enligt proteinkristallstrukturen för CTSB i PDB-biblioteket. Vi fann att hydroxylgrupperna i båda ändarna av CAG och ALA77- och GLY198-ställena i CTSB var bundna av en vätebindning, medan TYR75-, PR076- och ALA173-ställena i CAG och CTSB var bundna av van der Waals-kraft (figur 4E) . För att verifiera bindningsstället mellan CAG och CTSB transfekterade vi den muterade plasmiden av CTSB i HCT-116-celler. Resultaten visar att affiniteten mellan mutantplasmiden vid A77V och G198A och CAG var hundratals gånger högre än den för WT-plasmiden (figur 4F, G). I nästa avsnitt utforskar vi den specifika mekanismen genom vilken CAG spelar en antitumörroll genom CTSB.
【För mer information:george.deng@wecistanche.com / WhatApp:8613632399501】
