Beta Vulgaris Rubra L. (rödbeta) Peel Metanolextrakt minskar oxidativ stress och stimulerar cellproliferation via ökat VEGF-uttryck i H2O2-inducerad oxidativ stressad human navelvens endotelceller
Jun 09, 2022
Vänligen kontaktaoscar.xiao@wecistanche.comför mer information
Abstrakt:Antioxidantkapaciteten hos polyfenoler och flavonoider som finns i kostmedel hjälper till att stoppa utvecklingen av reaktiva syrearter (ROS) och skydda endotelceller från oxidativ stress/inducerad nekros. Rödbetor (Beta vulgaris var. Rubra L.; BVr) är en allmänt konsumerad grönsak som representerar en rik källa till antioxidanter. Rödbetors bioaktiva föreningar och deras roll i mänskliga navelvenendotelceller (HUVEC) är fortfarande underforskade. I den aktuella studien framställdes rödbetsskalmetanolextrakt (BPME) och dess effekt på bioeffektiviteten, kärnintegriteten, mitokondriell membranpotential, vaskulär celltillväxt och immunregleringsrelaterade genuttrycksnivåer i HUVECs med inducerad oxidativ stress analyserades . Resultaten från gaskromatografi-masspektroskopi (GC-MS) bekräftade att BPME innehåller 5-hydroximetylfurfural (32,6 procent), metylpyruvat (15,13 procent), furfural (9,98 procent) och 2,3-dihydro{{ 14}},5-dihydroxi-6-metyl-4H-Pyran-4-on (12,4 procent). BPM-extrakt förbättrade effektivt cellproliferation och bekräftades genom MTT-analys; den nukleära integriteten bekräftades med propidiumjodid (PI) färgningsanalys; den mitokondriella membranpotentialen (Aψm) bekräftades med JC-1-färgningsanalys. Annexin V-analys bekräftade att BPME-behandlade HUVEC visade 99 procent livsdugliga celler, men endast 39,8 procent viabilitet visades i HUVEC behandlade med enbart H2O2. Dessutom reducerade BPME-behandling av HUVEC under 48 timmar mRNA-uttryck av lipidperoxid(LPO) och ökade NOS-3, Nrf-2, GSK-3, GPX, endotelkväveoxidsyntas (eNOS) ) och vaskulär celltillväxtfaktor (VEGF)mRNA-expressionsnivåer. Vi fann att BPME-behandling minskade proinflammatorisk (nukleär faktor-k (Fk), vävnadsnekrosfaktor- (TNF-), tollliknande receptor-4(TLR-4), interleukin-1 ( IL-1 )) och vaskulär inflammation (intracellulär adhesionsmolekyl (ICAM), vaskulär celladhesionsmolekyl (VCAM), EDN, IL-1 )-relaterade mRNA-uttryck. Sammanfattningsvis ökade behandling med rödbetsskal effektivt vaskulära glatta celltillväxtfaktorer och utveckling av mikrotubuli, medan den minskade vaskulära inflammatoriska regulatorer. BPM kan vara fördelaktigt för vaskulär glattcellsregenerering, vävnadsreparation och anti-aging potential.
Nyckelord:rödbeta; oxidativ stress; mitokondrier; angiogenes; inflammation
1. Introduktion
Angiogenes är den fysiologiska processen för vaskulogenes från kroppens befintliga kärlsystem [1. Det är viktigt inte bara för embryonal utveckling och reproduktion utan också för cellcykel och vävnadsreparation[2,3]. Det är dock associerat med patogenesen av olika sjukdomar, såsom tumörtillväxt, reumatoid artrit och olika ischemiska och inflammatoriska sjukdomar [3-5]. Det vaskulära endotelet spelar en viktig roll för att upprätthålla vaskulär hemostas genom att reglera blodkärlstonen och immun- och inflammatoriska reaktioner [6,7].puritaner c-vitaminEndotelceller (EC) är tunna monocellulära skikt som kantar alla inre ytor av blodkärlen och producerar en mängd olika molekyler som verkar lokalt eller på avlägsna platser [7]. Endotelet är grundläggande för kroppens homeostas, och varje förändring i endotelets cellrespons leder till de primära händelserna av inflammatoriska och vaskulära sjukdomsprocesser, såsom ateroskleros och hypertoni [6,8,9]. Dessa sjukdomar orsakar oxidativ stress, vilket förändrar EC-strukturen och funktionsintegriteten och leder till endotelial dysfunktion [9]. Human navelven ECs (HUVECs) har använts i stor utsträckning som en modell för mänskliga vaskulära endotel-relaterade studier. Dessutom representerar de en användbar modell för att studera de viktigaste biologiska vägarna som är involverade i endotelets funktion [10].

Bioaktiva föreningar och fytokemikalier finns rikligt i frukt, grönsaker, gröna örter och många växter, som uppvisar många hälsofördelar, såsom antiinflammatoriska, antioxidant, anticarcinogena och angiogena egenskaper [11-13]. I detta avseende tillhör rödbetor (Beta vulgaris var. Rubra L.; BVr) familjen Amaranthaceae och klassificeras som en av de bästa källorna till höga halter av antioxidanter [14,15. Specifikt innehåller den flera fytokemikalier som är biologiskt aktiva, inklusive betalainer, flavonoider, polyfenoler, terapeutiska enzymer, askorbinsyra, dehydroaskorbinsyra (DHAA) och oorganiskt nitrat (NO3)[16-18]. Dessutom ger det värdefulla essentiella näringsämnen, såsom kalium, kalcium, magnesium, natrium, järn, zink, fosfor, koppar och mangan [19]. Flera studier har rapporterat att extrakt av rödbeta (rot) har många fördelaktiga effekter på grund av dess hypoglykemiska, lipidsänkande, antiinflammatoriska, antihypertensiva och antiproliferativa egenskaper [20-22].sistancheDessa fördelaktiga egenskaper kan alla kopplas till de bioaktiva föreningarnas förmåga att avlägsna fria radikaler. Således har konsumtionen av rödbetor kopplats till många närings- och hälsofördelar. På grund av dess näringsvärde kan den användas som en funktionell matkälla mot oxidativ stress som inducerar kroniska metabola sjukdomar, såsom typ 2-diabetes och hjärt-kärlsjukdom [23].
Baserat på litteraturöversikten har Beta vulgaris potenta antioxidanter, immunreglerande och angiogena egenskaper. Apigenin har hittats i betblad; det har antiproliferativa effekter i lever- och tarmceller, och det kan förbättra fettrik kostinducerad fetmakomorbiditet via AMPK-aktivering [24,25]. De Silva et al., (2020) [26] identifierade att Beta vulgaris skyddar vaskulära EC från externt inducerad oxidativ stress, vilket kan bero på den kombinerade effekten av flera bioaktiva föreningar som finns i denna växt. Fram till nu har den mekanistiska verkan för EG-proliferation och angiogeneseffekt av Beta vulgaris rotskal undersökts. Därför syftade vi till att genomföra den aktuella studien för att undersöka vaskulär cellproliferation, mikrotubuliutveckling, oxidativ stress och angiogeneskapacitet relaterad till Beta vulgaris rotskal med hjälp av cellulär morfologi och genuttrycksanalys i HUVECs. De angiogena effekterna av metanolextrakt av rödbetsskal associerat med nukleär integritet, utveckling av mikrotubuli, mitokondriell effektivitet och cellcykelstimulering i mänskliga vaskulära ECs utforskas.
2. Material och metoder
2.1.Beredning av rödbeta (Beta vulgaris rubra L.) metanolextrakt
Prover av färska rödbetor (Beta Vulgaris var. Rubra L.; BVr.) erhölls ursprungligen från grönsaksbutiker i Riyadh, Saudiarabien (KSA). De färska rödbetorna tvättades med destillerat vatten för att eliminera stjälkar och föroreningar. Det yttre skalet skalades för att avlägsnas och skars i små bitar. Proverna torkades i en varmluftsugn vid 40 grader och maldes sedan till pulver med användning av en elektronisk mixer. Därefter extraherades 500 g av pulvret i en steril flaska innehållande 1 L metanol (Sigma, St. Louis, MO, USA) under 24 timmar vid rumstemperatur på en shaker och upprepades tre gånger. Efteråt användes ett Whatman-filter (Whatman, Clifton, NJ, USA) för att filtrera extraktet. Slutligen, genom att reducera trycket, separerades lösningsmedlet från extraktet och extraktet uppsamlades som en fast torr substans efter indunstning av metanol. Det extraherade provet förvarades i ett kylskåp vid 4C tills vidare användning.
2.2. Gaskromatografi och masspektroskopianalys
Metanolextraktet (BPME) av rödbetsskal injicerades i en kiseldioxidkapillärkolonn (30 m×0,25 mm ID×0,25 um filmtjocklek) av GC-MS-instrumentet (Agilent 6890N/5973I) , Kalifornien, CA, USA) med en massselektiv detektor för att detektera de kemiska sammansättningarna. Instrumentets temperatur ställdes in som en initial 70 grader, höll 2 min, till 305 grader vid 20 grader/min, följt av hållning i 1 min. Den totala GC-körtiden sattes till 45 minuter med heliumgasen (99,999 procent) som en bärargas (en konstant flödeshastighet på 1,2 ml/min), 250 grader som injektortemperatur och 230 grader som en jonkällas temperatur. Baserat på GC-MS-spektrumet beräknades den relativa procentandelen av motsvarande komponent, och masspektra för den okända komponenten identifierades genom jämförelse med de kända 62,000 mönstren tillgängliga i National Institute of Standard and Technology datorbibliotek (NIST08).

Cistanche kan anti-aging
2.3. Cellkulturmaterial och kemikalier
HUVECs köptes från American Type Culture Collection (ATCC, Manassas, VA, USA). Cellodlingsmaterial såsom Dulbecco's Modified Eagle Medium (DMEM), EDTA, trypsin och andra erhölls från Gibco (Paisley, UK). Penicillin-streptomycin (PS) och fetalt bovint serum (FBS) köptes från Hyclone Laboratories, USA.vad är cistancheKemikalier som användes i det molekylärbiologiska experimentet erhölls från Sigma-Aldrich, särskilt MTT [3-(4,5-dimetyltiazol-2-yl)-2,5- difenyltetrazoliumbromid], PI och JC-1-färgning. SYBR Green PCR Master Mix och cDNA-syntessatsen erhölls från Qiagen (Hilden, Tyskland).
2.4.HUVEC
HUVECs odlades i DMEM och kompletterades med 1 procent PS och 10 procent FBS-komplex. Celler inkuberades i en fuktad atmosfär vid 37°C, 5 procent CO, och sub-odlades ungefär var tredje dag.
2.5. Cellviabilitet och cellproliferation med MTT-analys
HUVECs (1×104 celler/brunn) odlades med ett underhållsmedium och fick vidhäfta över natten i en 96-brunnsodlingsplatta. Sedan ersattes mediet med ett nytt odlingsmedium innehållande ökande koncentrationer av BPME(0,0.05,{{10}}.1,0.2 ,0,4,0,8,1,6 och 3,2 ug/ml) enligt MTT-analysplattkartan och inkuberades i 24 och 48 timmar; obehandlade celler användes som kontroller. Efter inkubationsperioden behandlades de experimentella cellerna med 20 μL/brunn av 5 mg/mL MTT (3-【4,5-dimetyltiazol-2-yl】-2, 5-difenyltetrazoliumbromid som löstes i dimetylsulfoxid (DMSO)) och inkuberades ytterligare i 4 timmar vid 37 grader. Sedan kasserades mediet och den producerade lila formazanen löstes i 100 μL 100 procent DMSO. Absorbansen av lösningen mättes med användning av en mikroplattläsare (Thermo Scientific, Waltham, MA, USA) vid 570 nm våglängd. Procentandelen (procent) av cellproliferation beräknades med följande ekvation: (absorbans av provet/medelabsorbans för kontrollen) × 100.
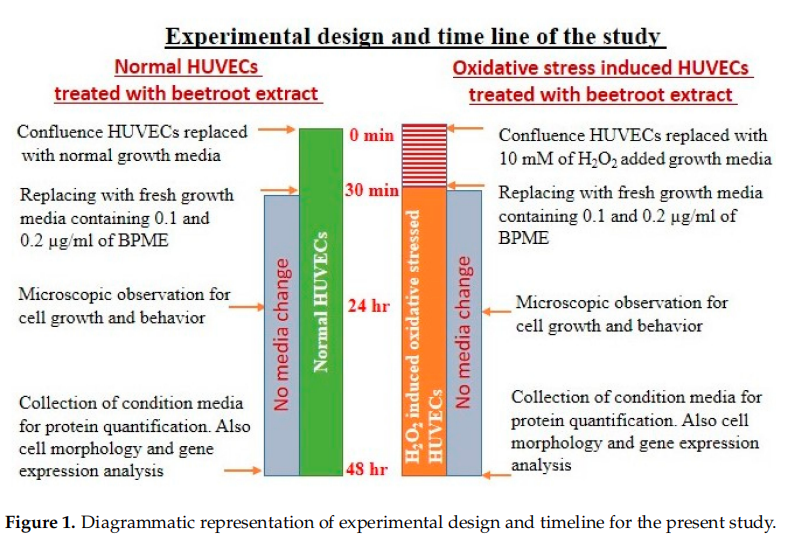
2.6. Experimentell design
Den aktuella cellproliferationsanalysen testade en lägre koncentration av BPME ({{0}}.1 och 0.2 ug/ml) och visade prolifererande HUVEC och mikrotubulimorfologi utan toxicitet. Volymer av 0,1 och 0,2 ug/mL dos av BPME valdes ut och behandlades med normala HUVEC och 10 mM H, O,-inducerade oxidativt stressade HUVECs under 48 timmar för att bestämma cellproliferationen, antiinflammatorisk angiogena och apoptotiska potentialer (Figur 1). Vehikelkontroll upprätthölls också i 48 timmar i båda grupperna. Quercetin (10 μM) användes som referenskontroll i båda experimentgrupperna.Anti-aging cistancheEfter inkubation analyserades de obehandlade och experimentella cellerna med avseende på cell- och kärnmorfologi och mitokondriell membranpotential med hjälp av ett BDM MitoScreen (C-1) Kit; apoptos bestämdes med Annexin V/apoptos-baserad cellsorteringsmetod i flödescytometri. Den oxidativa stressen och proinflammatoriska och angiogenesrelaterade genuttrycksnivåerna undersöktes.
2.7. Propidiumjodidfärgningsanalys för kärnskada
Cellulära morfologier för karakteristisk kärnskada, pyknos eller apoptotiska morfologiska förändringar efter behandling med {{0}}.1 och 0,2 ug/mL BPME (med eller utan H, O2) i HUVECs bestämdes med hjälp av PI-färgningsanalys under inverterad fluorescensmikroskopi, såsom beskrivits av Leite et al. [27].
2.8. Analys av mitokondriell membranpotential (△中m) av JC-1 Dye Staining
Potentialen för det mitokondriella membranet (△!m) bestämdes med JC{{0}}-analys för att bedöma mitokondriell effektivitet i vehikelkontroll och 0.1 och 0.2 ug/mL BPME-behandlade HUVECs (med och utan H2O2). Kortfattat blandades JC-1-färgningslösningen med en liknande volym odlingsmedium och sattes sedan till de experimentella HUVEC:erna och inkuberades i mörker i 20 minuter vid 37 grader. Sedan tvättades det obundna JC-1-färgämnet försiktigt två gånger med 200 μL JC-1-färgningstvättbuffert vid 4 grader. Efteråt observerades ackumuleringen av j-aggregerad mot JC-1-färgning under fluorescensmikroskopi med ett fluorescensmikroskop, och bilder togs. Dessutom mättes det mitokondriella membranets potential i flödescytometri med hjälp av BDIM MitoScreen (JC-1) Kit.
2.9. Annexin Vlapoptos-analys med flödescytometri
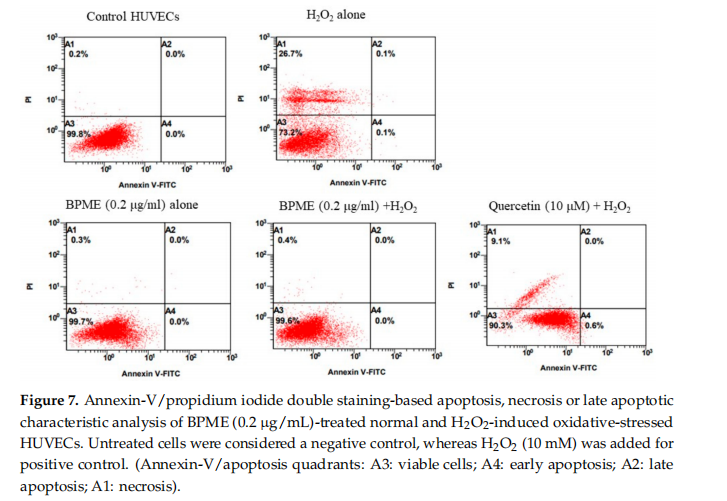
Den flödescytometribaserade Annexin V/PI-detektionsmetoden (Sigma Chemicals, USA) användes för att kvantifiera livskraftiga, proapoptotiska, tidiga apoptotiska och nekrotiska celler. Oxidativ stress-inducerad HUVEC (1×10 grad/brunn) pläterades i 24-brunnsplattor och inkuberades med BPME(0.1 och 0,2 ug/mL) eller vehikelkontroll för 48 h. Efter inkubation inkuberades celler i 400 μL 5 μL Annexin V-fluorescein isothiocyanat (FITC) och 5 μL PI-innehållande bindningsbuffert; efter detta hölls cellerna i 15 minuter vid rumstemperatur (RT) i mörker. Cellerna analyserades med flödescytometri (BD Biosciences, San Jose, CA, USA) för att identifiera apoptotiska (PInegativa och Annexin V-positiva) och sena apoptotiska (PI-positiva och Annexin V-positiva) celler [28].

2.10. Kvantitativ realtids-PCR-analys
Fastlane@ Cell till cDNA-kit (Qiagen, Hilden, Tyskland) användes för att extrahera totalt RNA och syntetisera cDNA från vehikelkontroll, BPME-behandlade HUVECs (med och utan H-O2) med hjälp av ett kvantitativt PCR (qPCR) halvautomatiskt instrument (Applied Biosystems) , Foster City, CA, USA). Uttrycksnivåer av oxidativ stress inkluderar (lipidperoxid, NOS-3), antioxidant (Nrf-2, GSK-3 och GPx), proinflammatorisk (nukleär faktor-k (NF-k), tumörnekrosfaktor- (TNF-), interleukin-1 (IL-1), vaskulär celltillväxtfaktor (VEGF), tollliknande receptor-4(TLR-4), och vaskulär inflammation (intracellulär adhesionsmolekyl (ICAM), vaskulär celladhesionsmolekyl (VCAM), EDN1 och endotelial kväveoxidsyntas (eNOS))-relaterade gener och referensgenen, -aktin, analyserades i HUVEC och kvantifierades med metoden för Yuan et al. [29]. Amplifieringsvärdena (ACt) beräknades av skillnaden mellan Ct (behandlad) och Ct (kontroll). Genuttryck plottades med användning av uttrycket av 2-AACt-värdet.
2.11.Statistisk analys
Alla experimenten replikerades och de resulterande data uttrycktes som medelvärden ± standardavvikelse (SD). Den statistiska analysen av skillnader mellan grupperna utfördes genom envägsanalys av varians (ANOVA) med SPSS-mjukvara (version 28.5, SAS Institute Inc., Cary, NC, USA).cistanche benefíciosSedan genomfördes Tukeys multipla jämförelsetest om signifikanta skillnader hittades. Alla resultat presenterades som medelvärde ± SD för sex replikationer i varje grupp. Ett p-värde < 0.05="" ansågs="" signifikant="">
3. Resultat
3.1.Bioaktiva molekyler i BPME
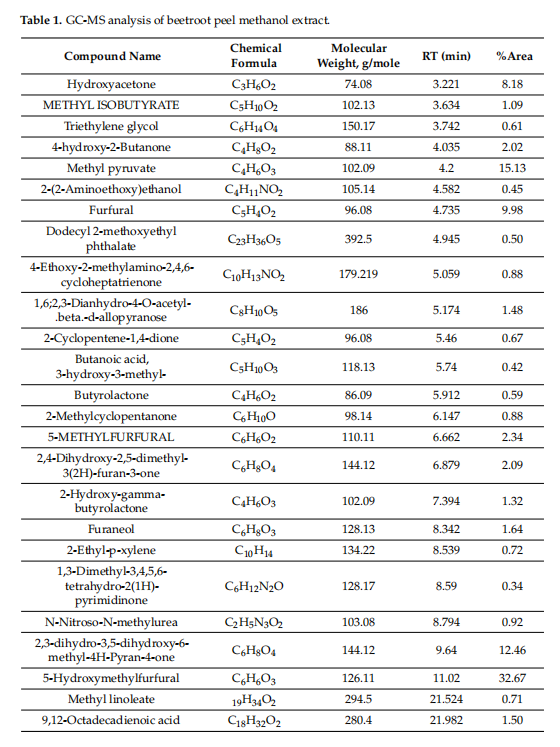
De kemiska beståndsdelarna i BPME bekräftades med GC-MS (Turbomass, PerkinElmer) Den kemiska sammansättningen av rödbetsskalextrakt bestämdes genom att jämföra de tillgängliga masspektra med National Institute of Standard and Technology (NIST) Spectral databas. GC-MS-resultaten bekräftade att BPME innehöll hydroxiaceton (8,18), 5-hydroximetylfurfural (32,6 procent), metylpyruvat (15,13 procent), beta-d-allopyranos (1,48 procent), furfural (9,98 procent),{ {15}}hydroxi-gamma-butyrolakton (1,32 procent) och 2,3-dihydro-3.5-dihydroxi-6-metyl-4H-Pyran{ {27}}ett (12,4 procent ;Figur 2a, Tabell 1).
3.2.Cellproliferation
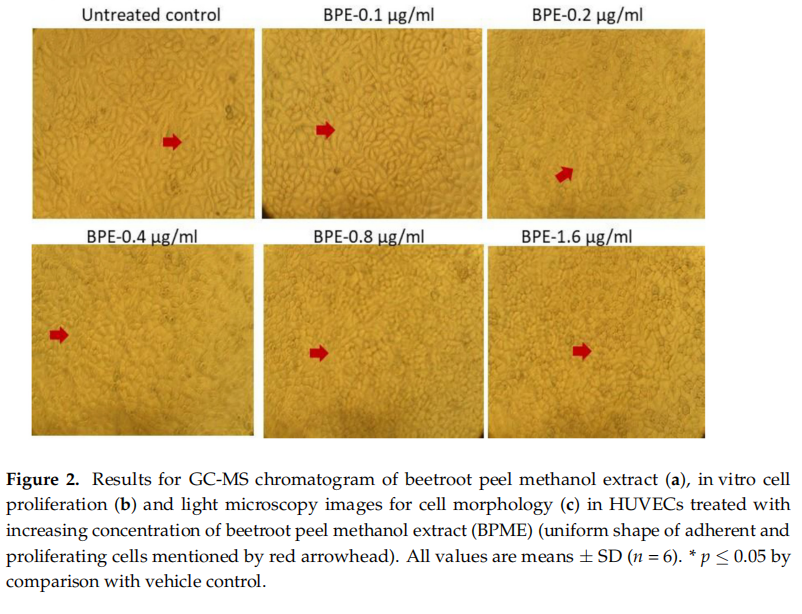
In vitro-cellproliferationspotentialen för BPME mot HUVEC presenteras i figur 2b. Ingen signifikant celltillväxthämning observerades i experimentgrupperna jämfört med vehikelkontrollen. Det bekräftades av den aktuella studien att en ökning av koncentrationen av BPME behandlad med HUVEC resulterade i ökad cellproliferation och livsduglighet efter 48 timmar (112 procent) jämfört med 24 timmar (103 procent) av behandlingen. Dessutom bekräftade de ljusmikroskopiska bilderna av BPME-behandlade HUVEC efter 48 timmar de normala cellerna med den enhetliga formen av adherent cellmorfologi, ökat antal prolifererande (replikations) celler utan någon skada var uppenbar (Figur 2c).
3.3. Analys av cell- och kärnmorfologi, mikrotubulibildning och JC-1 vistelse i HUVECS
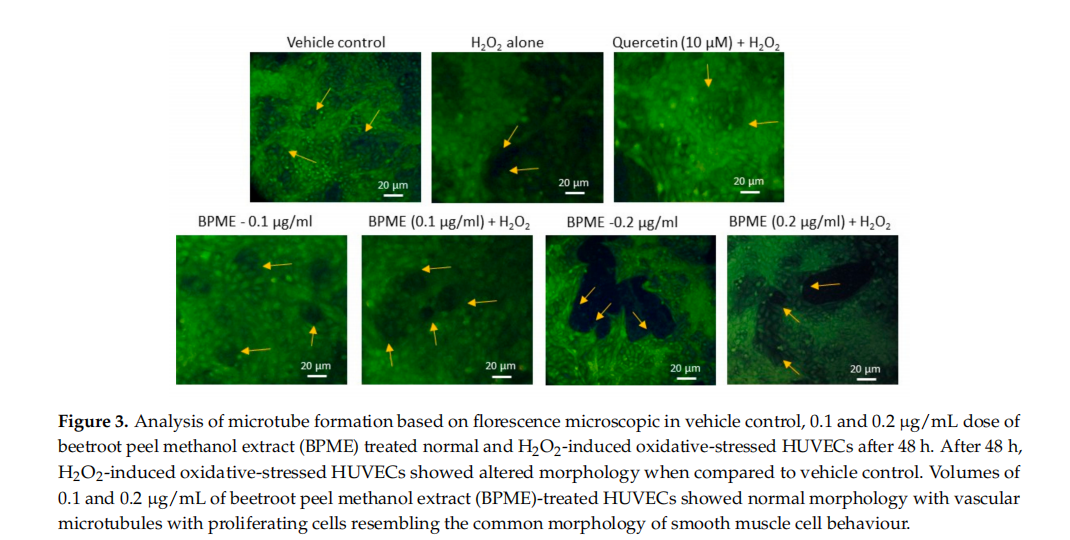
Figur 3 visar morfologin för mikrotubuliutveckling i fluorescensmikroskopiska bilder. H2O2-inducerade oxidativt stressade HUVEC:er visade dålig proliferation och oregelbunden morfologi av adherenta celler jämfört med kontroll HUVEC. Normala HUVECs behandlade med 0,2 ug/mL BPME visade prolifererande celler via replikation eller neogenes med mikrotubulimorfologi. Samtidigt visade 0.1 ug/mL dos av BPME-behandlade celler 1{{10}}0 procent vidhäftande celler med tidiga stadier av mikrotubuli. Oxidativt belastade HUVECs behandlade med 0,2 ug/mL BPME identifierade prolifererande nya celler med mikrotubulimorfologi och minskad oxidativ cellulär skada. Dessutom ökade 0,1 ug/ml BPME också den normala vaskulära cellmorfologin med prolifererande celler.
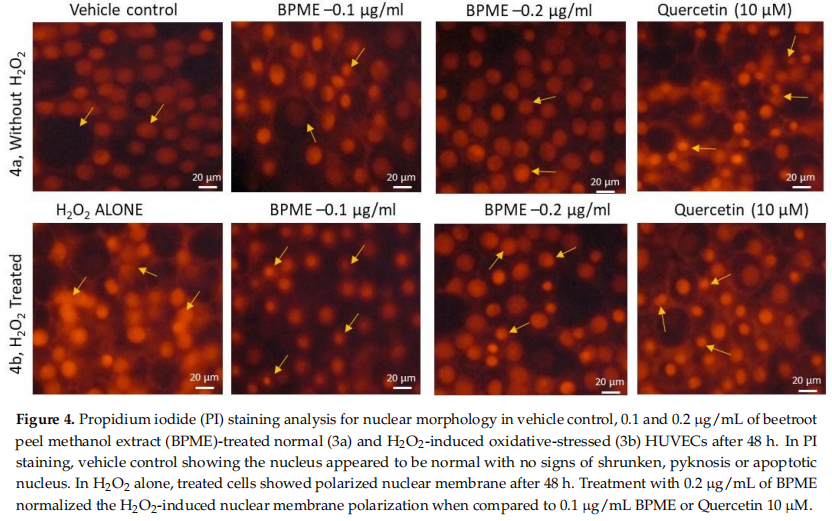
Figur 4a visar den normala morfologin för kärnstrukturen, med en sfärisk form, i kontrollen och BPME(0.1 eller 0.2 ug/mL)-behandlade HUVEC. Figur 4b visar bilderna för PI-färgning av normala och HUVECs med oxidativ stress inducerad av H, O. H2O2-behandlade HUVECs visar kärnor med oregelbundna former, som uppvisar kondensation och pyknos efter 3{{10} } min. Men 0.2 ug/ml BPME-behandling för HUVECs under oxidativ stress visade cirkulära kärnor med normal morfologi. Jämfört med 0,2 ug/mL BPME-extrakt hade 0,1 ug/ml BPME en mindre skyddande effekt mot H2O2-inducerad oxidativ stress i HUVEC.

Figur 5a visar JC-1-färgningsresultaten för HUVEC, inklusive kontroll- och BPME-behandlade celler; figuren illustrerar friska celler med aktiva mitokondrier, vilket bekräftas av det negativt laddade mitokondriernas upptag av den extramitokondriella lipofila katjoniska JC-1(grön färg) och J-aggregat omvandlade med röd färg intramitokon-verkligen. Figur 5b visar JC-1-färgningsresultaten för 0.2 ug/mL BPME administrerat till HUVECs med oxidativ stress inducerad av H2O2; resultaten bekräftade att nästan 94 procent av negativt laddade mitokondrier omvandlade den lipofila katjoniska JC-1(grön färg) till röda färg J-aggregat jämfört med 0.1 ug/mL BPME (61,4 procent) behandling eller
HO,-inducerad oxidativ stress i HUVECs (2 procent). Den mitokondriella membranpotentialen (MMP) observerades vara högre i BPME-behandlade celler jämfört med referensläkemedlet quercetin.
3.4. FACS-assisterad mitokondriell membranpotential (△pm; BD MitoScan) och Annexin V/apoptosanalys i HUVECs
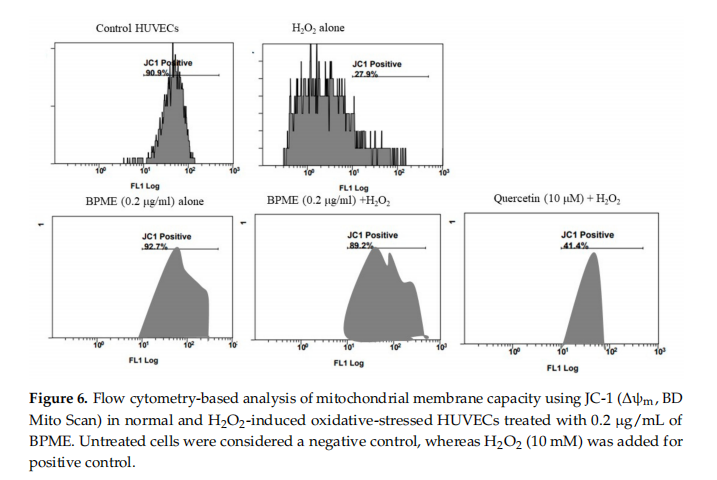
Figure 6 shows the mitochondrial membrane potential capacity in BD MitoScan analysis after 0.2 ug/mL of BPME treatment of normal HUVECs and HUVECs with oxidative stress induced by H>O, vi fann att 0,2 ug/mL BPME-behandling ökade MMP(Aum) till 92,7 procent ± 3,7 procent jämfört med HUVECs behandlade med enbart HO2 (27,9 procent ±7,2 procent). Däremot visade quercetinbehandlade celler en 41,4 procent ±1,6 procent av ökad MMP (Aum) jämfört med HUVECs behandlade med BPME och H2O2 eller H2O2 enbart.
3.5. Kvantifiering av genuttrycksnivåer i HUVEC
Oxidativ stress (LPO3), antioxidant (NOS-3, Nrf-2, GSK-3 och GPX), proinflammatorisk (IL-1, TNF-, NF-band TLR{ {7}}), och vaskulär inflammation (VCAM, ICAM, EDN, eNOS)-relaterade och VEGF-mRNA-expressionsnivåer kvantifierades i vehikelkontroll, 0.1 och 0.2 ug/mL av BPME och quercetin (10 μM)-behandlade HUVEC efter 48 timmar (Figur 8). Vi hittade betydligt (s<0.001) increased="" levels="" of="" lpo,="" nos-3,="" and="" nf-kb.il-1.tnf-α,="" vcam,="" icam,="" edn,="" and="" enos="" expression="" and="" decreased="" nrf-2,="" gsk-3β,="" and="" gpx="" levels="" in="" ho,-induced="" huvecs.="" treatment="" with="" 0.2="" ug/ml="" of="" bpme="" significantly="" decreased="" oxidative="" stress="" and="" vascular="" inflammation="" and="" increased="" antioxidant="" factor-related="" mrna="" expression="" when="" compared="" with="" oxidative-stressed="" huvecs.="" vegf="" expression="" levels="" showed="" a="" significant="" two-fold="" increase="" in="" 0.2="" ug/ml="" of="" bpme-treated="" cells="" only="" when="" compared="" to0.1="" ug/ml="" of="" bpme.="" vegf="" expression="" was="" not="" detected="" in="" huvecs="" with="" oxidative="" stress="" induced="" by="" h2o2.="" the="" observed="" effect="" was="" significantly="" higher="" than="" that="" of="" 0.1="" ug/ml="" bpme="" or="" quercetin="" (10="">

4. Diskussion
Vid extracellulär eller intracellulär stress övertar biotillgängligheten av reaktiva syrearter (ROS) antioxidantförsvaret och oxidativ stress stör redoxsignalering och kontroll [31]. Utvecklingen av oxidativ stress är förknippad med patogeneserna av kroniska sjukdomar, såsom neurodegenerativa sjukdomar, diabetes och åderförkalkning. Såsom oxidativ stress initierar endoteldysfunktion och främjar systemisk inflammation och rekrytering av makrofager [32]. Aktiverade immunceller migrerar in i kärlsystemet och frigör cytokiner och kemokiner associerade med kärlsammandragning och ombyggnad av glatta muskelcellers blodkärl och inflammation som påverkar kärlmuskelceller och kärlväggen [33]. Ökad vaskulär oxidativ stress slutar med vaskulär skada, stelhet i glatta muskelceller och strukturella elastinavvikelser. Dessutom har vaskulär oxidativ stress stimulerats vid andra patologiska tillstånd, såsom visceral fetma eller ateroskleros, på grund av ökad NADPH-oxidas (NOX-2) aktivitet i perivaskulär fettvävnad [34]. Vaskulär oxidativ stress orsakar huvudsakliga epigenetiska förändringar som inträffar under åldrandet, och det slutar med en tidig åldrandeprocess [35].
Utvecklingen av ROS-produktion och oxidativ stress i det biologiska systemet beror till stor del på mitokondriell dysfunktion, förutom NOX-2, endotelialt xantinoxidas, okopplat eNOS och lipoxygenas [36]. Antioxidantegenskaper hos kostmedel kan neutralisera ROS-generering via ökad antioxidantkapacitet [26]. Ginkgo Biloba-extrakt skyddar mot utvecklingen av åderförkalkning genom att minska ROS-generering och lipoxygenasaktivitet vid OxiLDL-inducerad endoteldysfunktion [37]. Dessutom har olika fenoliska föreningar och flavanoider från ätbara växter och spannmål egenskapen att ta bort ROS och lipidperoxidation [38]. Rödbetsskal (Beta vulgaris) metanoliskt extrakt har antioxidantpotential på grund av tillgången på hög fiber, antocyaniner och flavonoider som vitexin och betanin [39]. I den föreliggande studien valdes BPME för att identifiera den mitokondrieberoende mekanistiska metoden för att upptäcka dess effekt på den mitokondriella membranpotentialen, LPO-släckning och hämning av vaskulär inflammationsrelaterade mRNA-uttrycksnivåer.
MTT-analysen bekräftade att BPME signifikant ökade cellproliferationen, vilket bekräftas av den ökade kärnintegriteten i PI-färgning med den effektiva dosen av {{0}},2 ug/mL BPME jämfört med testade 0. 1 ug/ml BPME. Identifiering av en effektiv dos med låg koncentration och högsta aktivitet kan anses vara fysiologiskt säker. Vi hittade fluorescensmikroskopisk färgning av JC -1, och mitokondriernas membranpotential återställdes både i normala och HO-inducerade externt stimulerade oxidativt stressade HUVECs efter 0,2 ug/mL BPME-behandling. Mitokondriell dysfunktion förändrar oxidativ fosforylering, som misslyckas med att omvandla syreradikaler (O,.-) till H, O och H, Oby glutationperoxidas. På grund av otillräcklig ROS-avgiftning eller okontrollerad ROS-produktion är ökad mitokondriell oxidativ stress kopplad till ateroskleros [40]. Extrakt av rödbetsskal återställde effektivt mitokondriernas membranpotential, vilket framgångsrikt ökade ROS-avgiftning och H2O2-generering. Annexin V/PI-färgningsanalys bekräftade att BPME-behandling bibehöll andelen viabla celler och förbättrade cellproliferationsstadiet både i normala HUVEC och HUVEC med oxidativ stress inducerad av HO. I detta sammanhang har Choo et al. [41] bekräftade att transplanterade mesenkymala stamceller (MSC) efter generering av överdriven ROS eller exogen HO, vid den ischemiska platsen, kan försämra självproliferation och multi-lineage kapacitet. Inom regenerativ medicin är vaskulära glatta muskelceller de viktigaste regulatorerna av de kontraktila tonusartärerna genom att upprätthålla arteriellt perifert motstånd, blodtrycksregulatorer, blodflöde och reparation av artärer [42]. Dessutom är åldersinducerad fenotypmodulering av ECs. associerad med minskad cellulär kontraktilitet och ökad cellåldring. Vid kontinuerlig stress eller på grund av minskad mekanokänslighet identifieras minskad anpassning av mikromiljösignaler i åldrade glatta muskelceller[43]. Föreliggande resultat bekräftade att BPME-behandlingen bibehöll den livsdugliga cellpopulationen, vilket framgår av angiogeneskapaciteten.
Den identifierade spridningskapaciteten för BPME på HUVECs har stötts av minskningen av LPO-expression och ökade antioxidantgenuttryck. ROS och LPO genereras initialt från mitokondriekomplexet (I och I) och NOX-4 under cellproliferation eller differentiering [44]. Överdriven ROS reagerar och skadar biomolekylerna, särskilt förändrar integriteten av genomiskt DNA, vilket är avgörande för cellulär proliferation och funktioner [45]. Det har dock bekräftats att intag av antioxidantpolyfenoler, såsom epigallokatekin och tokoferol, skyddar cellerna från oxidativ stress och ökar spridningskapaciteten [46]. I vår studie minskade mRNA-expressionsnivåerna av LPO, och NOS-3, Nrf-2 och eNOS visade sig öka två gånger i HUVECs med oxidativ stress inducerad av Hoo. eNOS är den dominerande isoformen av NOS, ansvarig för de flesta av NO.-produkterna i glatta muskelceller och vaskulära vävnader. NEJ. vidgar alla typer av kärl och skyddar trombocytaggregation och leukocytadhesion i ECs[47]. Hittills har det funnits många motstridiga rapporter om kardiovaskulära riskfaktorer, och endoteldysfunktion har associerats med minskat eller ökat eNOS-uttryck [48]. Förhöjt uttryck av eNOS observerades vid vaskulär sjukdom, vilket sannolikt är en konsekvens av överskottsproduktionen av H-Oz. O2-7, en dismutationsprodukt, kan öka eNOS-uttrycket genom transkriptionella och posttranskriptionella mekanismer [49]. Patogenes av den vaskulära sjukdomen åtföljs av en accelererad nedbrytning av NO. efter reaktion med O2-7, och slutligen, ONOO-form, vilket leder till eNOS-frikoppling och NOX-enzymdysfunktion [50]. Oxidativ stress har undertryckts av antioxidantenzymer, och mRNA-nivåerna av GSK-3 och GPX har ökat efter BPME-behandling. BPME innehåller flera fytokemikalier som är biologiskt aktiva, inklusive betalainer, flavonoider, polyfenoler, terapeutiska enzymer, askorbinsyra, dehydroaskorbinsyra (DHAA) och oorganiskt nitrat (NOg), och dessa kan vara involverade i uppregleringen av antioxidantkapaciteten i HUVEC. I detta sammanhang har Cha et al. (2014) [51] rapporterade att klorogensyra effektivt skyddar mot oxidativ stress-inducerad DNA-skada i mänskliga keratinocyter.
Endotelin-1 (Edn-1), en endotelhärledd vasokonstriktor, utför glattmuskelcellmigrering och fungerar som en antiapoptotisk faktor i celler med kväveoxidinducerad stress[52,53]. Processerna med vaskulär ombyggnad, migration, proliferation och extracellulär matrisackumulering har stimulerats av både Edn-1 och NO [54,5]. Vi observerade ökat Edn-1-uttryck efter BPME-behandling i HUVECs med oxidativ stress. Vid oxidativ stress eller LPO-ackumulering är det tidiga stadiet av vaskulär inflammation adhesionen av leukocyter till glatta endotelceller, det är framträdande för de kritiska händelserna av ischemi och ateroskleros [56]. Det förmedlas av VCAM- och ICAM-uttryck; det har stimulerats av många av kemokinerna och kemotaximedlen, såsom NF-kB, IL-1 och TNF-uttryck[57]. Hämning av IL-1-aktivering följt av uttryck av adhesionsmolekyler har uppnåtts av den fenoliska föreningen ellagsyra i kosten [58]. Behandling med BPME mot externt stimulerade HUVECs med oxidativ stress minskade signifikant de vaskulära cellspecifika proinflammatoriska faktorerna, såsom VCAM, ICAM, NF-KB, IL-1 och TNF-x uttrycksnivåer. I detta sammanhang har Crespo et al. [59]rapporterade att kaempferol och quercetin hämmade pro-inflammatoriska gener, såsom VCAM, ICAM, NF-kB respektive IL-1 uttryck. Sammantaget gynnade hämningen av oxidativ stress och vaskulär inflammation-relaterad genuttryckspotential av BPME uttrycket av vaskulära celltillväxtfaktorer och möjligen hjälpte vaskulär cellproliferation och tillväxt.
5. Slutsatser
De nuvarande fynden bekräftar att det ökade uttrycket av antioxidantgener var associerat med släckning av oxidativ stress, vilket bidrog till att övervinna försämringen av HUVEC-proliferation och angiogenes. Svart vitlök som innehåller hydroximetylfurfural undertrycker den inflammatoriska effekten av TNF-inducerad monocytcelladhesion till HUVEC och undertrycker ytterligare ROS-generering, VCAM-1-uttryck och NF-kB-aktivering [60]. Dessutom har He et al. [61] bekräftade att hydroximetylfurfural har potential att skydda mot hypoxi. Rödbetsskal har också identifierats innehålla flavonoider, furan och antioxidantkomponenter, såsom 5-hydroximetylfurfural, metylpyruvat, furfural och 2,3-dihydro-3,5- dihydroxi-6-metyl-4H-Pyran-4-on; dessa komponenter är ansvariga för den förbättrade antioxidantkapaciteten och undertryckandet av proinflammatoriska vaskulära glatta muskelcellsadhesionsmolekyler. Rödbetsskal har använts som ett stimulerande medel för antioxidantpooler för att dämpa den yttre stimulansen eller den interna patologiska stimulansen av peroxidativ cellulär stress. Våra resultat visade att komponenterna i rödbetor hjälper till att minska metabolisk stress och inflammation i HUVEC, vilket kan vara fördelaktigt för vaskulär cellproliferation och angiogenes.
Den här artikeln är extraherad från Genes 2021, 12, 1380. https://doi.org/10.3390/genes12091380 https://www.mdpi.com/journal/genes
