Metformin och åldrande: en recension del 1
May 24, 2022
Vänligen kontaktaoscar.xiao@wecistanche.comför mer information
Nyckelord:Föryngring·Långlivslängd·Hälsospann·Metformin·Fisetin
AbstraktMetformin föreslås ibland vara ett "anti-aging" läkemedel, baserat på prekliniska experiment med lägre ordningens organismer och många retrospektiva data om fördelaktiga hälsoresultat för typ 2-diabetiker. Stora prospektiva, placebokontrollerade studier planeras, i pilotstadiet eller pågående, för att hitta en ny användning (eller indikation) för en åldrande befolkning. Eftersom en av metforminstudierna har "bräcklighet" som slutpunkt, liknande en prövning med en växthärledd senolytikum, diskuteras den senare klassen av nya anti-aging läkemedel kort. Det finns farhågor inte bara för brist på vitamin B12 och B, utan också för om det finns negativa effekter av metformin på individer som försöker förbli friska genom att upprätthålla kardiovaskulär kondition via träning.
Introduktion
Inför uppgiften att skriva en recension om "metformin och åldrande" beslutades det att extrahera information från den senaste litteraturen som är relevant för människor, med fokus på planerade eller pågående kliniska prövningar. Verkningsmekanismer diskuteras kort. En detaljerad analys av bevisen för metformin för att förlänga livslängden för modellorganismer följer.sistancheAnti-aging forskning är ett hett men inte oproblematiskt ämne, vilket kommer att exemplifieras. En översyn från 2017[1] listar 16 bioteknikföretag som utvecklar läkemedel för att bekämpa åldrande och/eller åldersrelaterade sjukdomar, 5" big data" anti-aging-företag och 7 stamcells-/regenereringsföretag. Bland de 5 stora dataföretagen finns Calico Life Sciences LLC," ett av Googles moonshot-projekt." De unika egenskaperna hos den jordlevande mullvadsråttan, som lever ungefär 10 gånger längre än en mus, utvecklar nästan ingen cancer och trotsar Gompertz-lagen (se onlineförsörjning Fig. S1; för allt material på nätet, se www.karger.com/doi/10.1159/000502257), verkar vara av intresse för Calico. Rochelle Buffenstein är nu en ledande anställd i företaget [2](ruta 1 [3-5).

Livslängd och livslängd
Livsförlängning - som en enkel avläsning av att bromsa åldrandet genom manipulering av modellorganismer med antingen droger eller t.ex. dietrestriktioner - har en framträdande plats i bildforskningsforskningen. Detta tillvägagångssätt stimulerades av observationer med mTORCl-hämmaren (mekanistiskt mål för rapamycinkomplex1) rapamycin 2009 [6] när läkemedlet gavs mer eller mindre oavsiktligt [7] till 600-daggamla möss. Livet förlängdes med 28 och 38 procent för
Tillägnad em.O.Univ.Prof. Dr.med.vad är cistancheGeorg Wickon tillfälle av hans 80-årsdag.
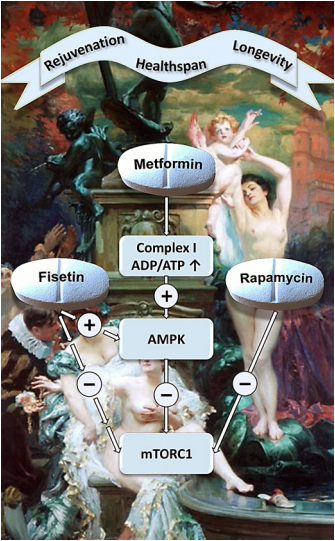
Fig.1. De tre löftena om forskning mot åldrande. Målningen "La Fontaine de Jouvence" av Paul-Jean-Louis Gervais visar ett exempel på en konstnärs intryck av "Ungdomsfontänen" med de tre löftena: "hälsotid", föryngring" och "livslängd." Droger (fisetin, rapamycin och metformin) som testas i kliniska prövningar eller under utveckling för åldersrelaterade sjukdomar, och som sprids för att uppfylla ett eller till och med alla löften, visas i illustrativt syfte. Mekanismer som är relevanta för anti-aging visas med heldragna pilar med ett plus- eller minustecken Avbrutna pilar indikerar aktiviteter som rapporterats i den prekliniska litteraturen utan identifiering av en primär molekylär läkemedelsreceptor Det "klassiska" molekylära målet för metformin är komplex I i den mitokondriella andningskedjan (se huvudtexten). Ett ökat cellulärt ADP/ATP-förhållande vid metforminberikning i mitokondriella matrisen leder till aktivering av AMPK Aktiv AMPK hämmar mTORC1 direkt genom fosforylering av RAPTOR och indirekt genom att aktivera TSC2, en underenhet av TSC. Medan flera andra metforminmål utöver komplex I diskuteras i litteraturen, är rapamycin, genom att bilda ett komplex med FKBP12, utomordentligt selektivt för mTORCl; det finns inga "off-target" bindningsställen. Däremot har fisetin, i likhet med andra växtpolyfenoler, flera cellulära verkan (antioxidant, kinashämning, etc.; se huvudtexten och Schubert et al. [21]). Prekliniska analyser med laboratoriemöss, ibland genetiskt modifierade, använder en förlängning av livslängden och förlängda tidsperioder för att vara fri från åldersrelaterade symtom som viktiga avläsningar. Se onlinetillbehör. Fig. S1 för det teoretiskt slutgiltiga resultatet av all forskning mot åldrande; det exemplifierar en "exceptionell modell för biogerontologi"[101], den nakna mullvadsråttan.Anti-aging cistancheDessa små gnagare behandlas inte med droger. Möjliga undantag är föreningar som produceras av deras tarmmikrobiom, eftersom djuren utövar koprofagi. Nakna mullvadsråttor förblir "för evigt unga och friska" och överlever sina motsvarigheter från råtta och möss som behandlats med senolytika eller något annat läkemedel i minst en storleksordning. Målning: Capitole Toulouse, Salle des Illus-tres, Paul Gervais, 1908 (allmän egendom). hanar respektive honor. Analoger av rapamycin finns i tidiga kliniska studier för åldersrelaterade sjukdomar [8], och moderläkemedlet, som inte är patentskyddat, föreslogs nyligen för att förebygga Alzheimers sjukdom [9].
Föryngring genom eliminering av åldrande celler Termen "föryngring" användes för analys av Chang et al.[10]. Ett av kännetecknen för åldrande är ett ökat antal "åldrande" celler[1]. Dessa irreversibelt tillväxtstoppade celler är resistenta mot apoptos, och många åldersrelaterade sjukdomar påstås vara kopplade till cellulär åldrande[12,13].cistanche benefíciosÅldrande celler utsöndrar en mängd olika bioaktiva faktorer (ålderdomsassocierad sekretorisk fenotyp[SASP]). SASP kan vara skadligt för närliggande celler och till och med inducera åldrande [14].

Cistanche kan anti-aging
Föreningar som selektivt eliminerar åldrande celler i cellkultur eller i gnagare klassificeras som senolytiska; föreningar som undertrycker SASP kallas senomor-phics[15]. De första molekylerna, som påstods ha upptäckts av "bioinformatik"[16] men mer sannolikt av "fenotypisk screening"[17], var dasatinib (en federal läkemedelsadministration [FDA]-godkänd kinashämmare) och quercetin. När de (så kallade) Koch-liknande kriterierna i preklinisk testning var uppfyllda [18] gick dasatinib och quercetin, som en fast doskombination, in i den första kliniska prövningen i en öppen pilotstudie (NCT02874989) för patienter med idiopatiska lungfibros [19].
Fisetin är ett annat senolytikum, testat i en klinisk prövning för åldersrelaterade störningar (NCT03675724; AFFIRM-LITE). Fisetin uppfyllde också de Koch-liknande kriterierna [20] och var pat-"Viviremos 135 anos!"("Vi kommer att leva i 135 år") fanns på titelsidan för den spanska tidningen "El Mundo" den 15 oktober 2015. Prisade var spanska forskare som publicerade en artikel i Nature Cell Biology [3]. Däri, rollen som nukleär faktor kappa-lättkedjeförstärkare av aktiverade B-celler (NF-KB) och dess nedströmsmål, såsom störare av telomer tystnad 1-liknande (DOT1L), som är en histon H3( H3K79)metyltransferas, förökades som mål för "föryngring." Tre år tidigare hade författarna rapporterat att natriumsalicylat (200 mg/kg genom daglig ip-injektion) avsevärt förlängde livet i progeria-musmodeller [4]. Det tog fyra år tills 2015 års uppsats[3] drogs tillbaka av Nature Cell Biology i mars 2019 [5]. I januari 2019 drogs ytterligare 8 publikationer från samma grupp tillbaka från Journal of Biological Chemistry. Detta illustrerar att i den ganska unga vetenskapliga disciplinen anti-aging forskning är konkurrensen hård och reproducerbarhet av andra, oberoende forskargrupper är viktigast. Återkallelserna inträffade slutligen på grund av många kommentarer och klagomål, särskilt om "photoshopping" (sehttps://pubpeer.com/).

angett för att förbättra minnet (US7897637B2). Fisetin är en av flera andra föreningar som antas fungera som "geroneuro-skyddare"[21]. Fisetin och dess huvudmetabolit Geraldo passerar tydligen blod-hjärnbarriären när de ges oralt till möss[22]. Fisetin är typiskt för främlingsfientliga växter och liknar quercetin och genomgår flera biotransformationer. Mer än 50 metaboliter identifierades hos gnagare[23]. Fisetin marknadsförs som ett näringsämne (t.ex. under varumärket Novusetin).
Den intresserade allmänheten undersöker tydligen ClinicalTri-als.gov för pågående anti-aging studier och började omedelbart konsumera fisetin, ofta tillsammans med quercetin och reducerade nikotinamidadenindinukleotid (NADH) boosters, antingen dagligen eller två gånger i veckan (som i den kliniska prövningen), och rapportera sina självexperimentella resultat på en webbplats [24].
HealthSpan
Matt Kaeberlein föreslog nyligen att avstå från att använda termen healthspan i den vetenskapliga litteraturen eftersom hälsa inte är en binär egenskap med bara två tillstånd (bra eller dåliga)[25]. Det används dock i många prekliniska publikationer för att betona att en intervention (med ett läkemedel eller på annat sätt) förlänger inte bara livslängden utan också den procentuella tiden utan några hälsobrister, enligt definitionen av författarna.
Till skillnad från rapamycin, där data från alla prekliniska prövningar på musmodeller och andra organismer av lägre ordning visar att läkemedlet ökar livslängden ("livslängden"), finns det få sådana bevis för metformin (se nedan). Rapamycin ökar också hälsospännet eller till och med vänder åldersrelaterade sjukdomar ("föryngring") hos maskar, flugor, möss, råttor och hundar [9].
Metformins verkningsmekanism
Metformin stimulerar hormonutsöndringen från tarmen Metformin är endast aktivt vid typ 2-diabetes (T2D)/pre-diabetes när det appliceras oralt. Den vanliga dosen av en formulering med omedelbar frisättning är cirka 2 per dag (12 mmol). Cirka 6 mmol utsöndras dagligen via njurarna (aktiv sekretion). Njurceller såväl som epitel i urinvägarna exponeras för koncentrationer högre än 4 mM. Den andra hälften av läkemedlet försvinner i avföringen [26]. Tjocktarmen utsätts för koncentrationer på upp till 40 mm. Koncentrationer av metformin i humana jejunala biopsier efter dos är 4,000 μmol per kg 【27】, och i kolonbiopsier (steady-state) är de mellan 26 och 1 820 μmolper kg [28].
Det är inte känt i vilket cellulärt utrymme (cytosol, mitokondrier, endoplasmatiskt retikulum eller endo-/ly-lysosomer) läkemedlet är sekvestrerat. Tidigare har det postulerats att levern är läkemedlets primära målorgan. Denna syn har förändrats, eftersom tarmen (upptag i enterocyter och enteroendokrina celler medieras av specifika bärare) nu erkänns vara ansvarig för det mesta av den antidiabetiska (och förebyggande) aktiviteten [29]. Bevisen är baserad på effekten av en formulering med fördröjd frisättning som skonar den övre delen av tarmen (duodenum och jejunum) med lägre systemisk tillgänglighet såväl som leverexponering [30], och på kliniska studier med antagonister som blockerar tarmhormonet glukagonliknande peptid-1(GLP-1) [31]. Förutom GLP-1 ökar plasmanivåerna av två andra hormoner, peptid YY(PYY) och tillväxt/differentieringsfaktor 15(GDF15), signifikant under metforminbehandling. Den senare, producerad huvudsakligen i tarmen via den "integrerade stressresponsen"[32], verkar uteslutande på nervceller i bakhjärnan (area posture ma) för att kontrollera aptit, matintag, kroppsvikt och plasmanivåer korrelerar med fördelar vid prediabetes [ 33].
Metformin ökar aktiviteten hos adenosinmonofosfataktiverat proteinkinas
Aktiviteten av adenosinmonofosfataktiverat proteinkinas (AMPK) ökar vid kronisk metformindosering i mänsklig skelettmuskel [34] och fettvävnad [35]. Aktivering av AMPK föreslås också delta i den akuta frisättningen av tarmhormonerna GLP-1 och PYY från humana mukosala preparat, eftersom metforminstimulering blockeras av en hämmare av kinaset[36].AMPK kan aktiveras av "kanonisk" väg (ökning i förhållandet adenosindifosfat/adenosintrifosfat [ADP/ATP] och fosforylering av uppströms leverkinas B1 [LKB1]) eller genom AMP-oberoende mekanismer [37] inklusive en lysosomal väg utlöst av en minskning av fruktos 1 6-bisfosfat [38].
Mitokondriellt komplex IIinhibering, frånkoppling eller blockering av lysosomalt vakuolärt ATPas?

Den klassiska "receptorn" för "antidiabetiska" biguanider (metformin<>
Som ett alternativ till den mitokondriella vägen (komplex I "hämning" och/eller "avkoppling"), postulerades direkt aktivering av AMPK och inhibering av mTORCl via blockering av lysosomalt vakuolärt ATPas (V-ATPas) [43]. Från och med april 2019 har varken ett struktur-aktivitetssamband för guanidiner, som för mitokondrier och komplex I, eller dossvar rapporterats. På samma sätt har underenheten av V-ATPas som antas binda läkemedlet inte publicerats.
Den här artikeln är extraherad från Gerontology 2019;65:581–590 582 DOI: 10.1159/000502257
