Mononatriumglutamat inducerar förändringar i lever- och njurmetaboliska profiler och tarmmikrobiom hos Wistar-råttor
Feb 22, 2022
Abstrakt:Kort- och långtidskonsumtionen av mononatriumglutamat (MSG) ökar urinens pH men effekterna på de metaboliska vägarna i levern, njure och tarmmikrobiotan förblir okänd. För att lösa detta problem undersökte vi vuxna Wistar-hanråttor som tilldelats dricksvatten med eller utan 1 g procent MSG under 2 veckor (n=10, vardera). Vi utförde en kärnmagnetisk resonans (NMR) spektroskopibaserad metabolomisk studie av jejunum,lever, ochnjurar, medan fekala prover samlades in för bakteriell DNA-extraktion för att undersöka tarmmikrobiotan med användning av 16S rRNA-gensekvensering. Vi observerade betydande förändringar ileverav MSG-behandlade råttor jämfört med kontroller i nivåerna av glukos, pyridoxin, leucin, isoleucin, valin, alanin, kynurenat och nikotinamid. Blandnjuremetaboliter ökade nivån av trimetylamin (TMA) och pyridoxin minskade efter MSG-behandling. Sekvensering av 16S rRNA-genen avslöjade att MSG-behandlade råttor hade ökat Firmicutes, tarmbakterierna associerade med TMA-metabolism, tillsammans med minskade Bifidobacterium-arter. Vår data stöder effekten av MSG-konsumtion påleverochnjureämnesomsättning. Baserat på förändringarna i tarmmikrobiomet spekulerar vi att TMA och dess metaboliter såsom trimetylamin-N-oxid (TMAO) kan vara förmedlare av effekterna av MSG pånjurhälsa.
Nyckelord:mononatriumglutamat; tarmmikrobiota; Metabolisk väg; metabolomik; mikrobiom; trimetylamin; Njure; Lever
IntroduktionMononatriumglutamat (MSG) tillsätts vanligtvis till livsmedel för att öka smakligheten, särskilt i det asiatiska köket och industriellt bearbetade livsmedel [1]. MSG anses vara en säker ingrediens för mänsklig konsumtion oavsett mängd av Food and Drug Administration (FDA) [2] trots att färska data visar att det genomsnittliga dagliga MSG-intaget är 3–4 g och att varje extra gram MSG ökar risken för att utveckla metabolt syndrom [3]. Förhöjda mängder MSG i kosten är associerade med övervikt [4,5] och hypertoni [6], men resultaten är inkonsekventa [7,8].

Försök har gjorts för att avslöja effekterna av MSG på metaboliska organ hos djur genom antingen parenteralt [9,10] eller oralt intag [11,12]. I ett av dessa försök att undersöka effekterna av MSG i råttanjurar, visade resultaten att både kort- [13] och långvarig [11] MSG-konsumtion orsakade alkalisk urin hos råttor, även om mekanismen för urinalkalisering inte är etablerad. Metabolomics är en vanlig metod för att definiera förändringar i metaboliter från olika tillstånd [14,15]. Den kortsiktiga MSG-konsumtionen orsakade specifika förändringar i urinmetaboliter inklusive dimetylamin (DMA) och metylamin (MA), som är tarmhärledda metaboliter från trimetylamin (TMA). TMA är en flyktig kortkedjig alifatisk amin som ger den karakteristiska fisklukten. Faktum är att tarmbakterierna producerar TMA från kostfiskar eller så kan den genereras från andra näringsämnen, inklusive kolin och karnitin, som finns rikligt i ägg och rött kött [16]. Huvuddelen av TMA omvandlas enzymatiskt till den luktfria trimetylamin-N-oxiden (TMAO), och höga TMAO-plasmanivåer är associerade med hjärt-kärlsjukdom (CVD) [17], kroniskanjursjukdom(CKD) [18] och diabetes [19].
Vi utnyttjade häri metabolomiska verktyg för att undersöka effekterna av kortvarig MSG-konsumtion på metabolomen av plasma,lever,njureoch tarm, och analyserade korrelationen mellan de metabolomiska resultaten och förändringarna i tarmmikrobiotan. Våra data kan ge nya mekanistiska insikter om effekterna av MSG i kosten samtidigt som de visar biomarkörer för MSG-inducerad organskada.
Material och metoder
DjurTjugo 6-veckor gamla Wistar-hanråttor (vikt cirka 200 g) erhölls från National Laboratory Animal Center (Mahidol University, Salaya, Bangkok, Thailand), acklimatiserade i individuella metaboliska burar av rostfritt stål under 2 veckor, och hålls sedan under standardförhållanden med temperatur (23 ± 2 ◦C), luftfuktighet (30–60 procent) och ljusstyrka (350–400 lux) på 12 timmar mörker/12 timmars ljuscykel. Råttor försågs med en kommersiell pelletdiet nr CP 082 (Perfect Companion Group, Bangkok, Thailand) under studien. Alla experiment utfördes enligt riktlinjerna från Northeast Laboratory Animal Center (NELAC), Khon Kaen University, Thailand. Dessutom godkändes studien av Animal Ethics Committee vid Khon Kaen University, Thailand (AEKKU-NELAC5/2558).
ReagensRen livsmedelskvalitet (99 procent) MSG (Ajinomoto, Tokyo, Japan) användes för att mata djuren. Metanol och kloroform av kommersiell kvalitet köptes från RCI LABSCAN LIMITED (Bangkok, Thailand) för vävnadsextraktion, vatten av LC-MS-kvalitet köptes från Merck (Darmstadt, Tyskland), kaliumdivätefosfat (KH2PO4) och deuteriumoxid (D2O) köptes från Merck (Darmstadt, Schweiz), natriumazid (NaN3) producerades av European Chemicals Agency (ECHA, Helsingfors, Finland), natriumtrimetylsilyl-[2,2,3,3-2H4]-propionat (TSP) , en intern standard för NMR-analys, erhölls från Santa Cruz Biotechnology (Santa Cruz CA, USA). För masspektrometri köptes isopropanol (C3H8O) och myrsyra (CH2O2) av kommersiell kvalitet från RCI LABSCAN LIMITED (Bangkok, Thailand).
Experimentell designRåttor tilldelades slumpmässigt att få dricksvatten antingen med (n=10) eller utan (n=10) 1 g procent MSG under 2 veckor. Vatten med omvänd osmos (RO) användes (klorkoncentration på 3–4 ppm) för djurstudien när alla råttorna hade fri tillgång till mat. Dagligt intag av vatten (ml) och mat (g) registrerades, såväl som veckokroppsvikten (g). Den 24 hurinära utsöndringen (ml/råtta/dag) registrerades under hela studieperioden. Blodprover från avföring och svans (100 µL plasma) togs 2 veckor före avlivningen av djur med koldioxid (CO2) efter en 12-h fasta. Vävnadsprover, dvs jejunum,leverochnjure,uppsamlades och snabbfrystes i flytande kväve innan de förvarades vid t80 ◦C tills de användes för analys.
Provberedning och analysVarje vävnad (100 mg våt massa) användes för metabolitextraktion enligt de tidigare publicerade protokollen [20]. Innan NMR-insamling återsuspenderades den polära fasen av vävnadsextrakt i en NMR-buffert på 580 µL (100 mM natriumfosfatbuffert, pH 7,4, i D2O, innehållande 0,1 mM TSP och 0,2 procent NaN3), vortexades kort och centrifugerades vid 12,000× g i 5 min vid 4 ◦C. Därefter överfördes 550 µL av blandningen till ett NMR-glasrör (Duran Group, Mainz, Tyskland) med en ytterdiameter av 5 mm före NMR-analys. Ungefär 250 mg avföring blandades med 500 µL vatten av HPLC-kvalitet (Merck, Darmstadt, Tyskland) och homogeniserades med användning av en virvelblandare med hastigheten 2500 rpm under 15 minuter vid rumstemperatur. Avföringssuspensionen centrifugerades sedan vid 12,000x g under 15 minuter vid 4 ◦C och 540 µL supernatant överfördes till rena 1,5 mL mikrorör och 60 µL NMR-buffert (1,5 M KH2PO4-buffert, pH 7,4) i D2O, innehållande 2 mM TSP och 1 procent NaN3) tillsattes. Därefter virvlades rören kortvarigt, centrifugerades vid 12, 000 x g i 10 minuter, och slutligen överfördes 580 µL av blandningen till ett NMR-glasrör med en ytterdiameter på 5 mm för analys.
Vävnadsextrakt och fekala prover analyserades med en 400 MHz NMR-spektrometer (Bruker Biospin, Rheinstetten, USA) vid en temperatur av 298,15 K. Spektrana hänvisades till TSP-toppen (δ1H { {14}}.00), fasad och baslinjekorrigerad med MATLAB (Mathworks, Natrick, MA USA). Signalen för TSP-topp (δ1H H1.000–0,005) från alla vävnader och TSP-topp (δ1H H1.20–0,157) från feces avlägsnades. Dessutom avlägsnades vattentoppen från jejunum (δ1H 4,50 och 5,20),lever(δ1H 4,68 och 5.00),njure(51H 4,31 och 5,74) och feces (51H 4,18 och 5,23). Dessutom utsattes råspektra för toppanpassning och normalisering [21]. Spektraldata för alla prover analyserades med användning av oövervakad principal komponentanalys (PCA) och övervakad ortogonal signalkorrigeringsprojektion till latent strukturdiskriminerande analys (O-PLS-DA). Data var medelcentrerade och skalade med enhetsvarians (UV). O-PLS-DA-modellerna utvärderas av R2X-, R2Y- och Q2Y-värdena, som representerar fifitness, bråkdel av varianser för Y-matrisen respektive prognosförmåga hos modellen [22]. För att undvika överanpassning utfördes 7-faldig korsvalidering för 500 upprepningar. Permutations p-värde användes för att indikera modellens validitet. Signifikanta variabler för varje giltig modell valdes ut genom O-PLS-DA-korrelationskoefficienter med Benjamini-Hochbergs korrigering för falsk upptäcktsfrekvens (p < 0,05).="" statistisk="" totalkorrelationsspektroskopi="" (stocsy)="" [23],="" interna="" databaser="" för="" kemikalieskift="" och="" human="" metabolome="" database="" (hmdb="" version="" 4,="" usa)="" [24]="" användes="" för="" identifiering="" av="">
Bananrikningsanalys utfördes också med hjälp av MetaboAnalyst (http://www. metaboanalyst.ca/ (tillgänglig den 14 juli 2020)) [25]. Illustrationen av den metaboliska vägen genererades av Cytoscape [26]. Förändringar i metaboliter identifierades av STOCSY och univariat analys utfördes genom att undersöka den relativa koncentrationen av signifikant differentiella metaboliter, beräkna integrationen av spektratoppar. Enligt p-värdet beräknat av studentens t-test med GraphPad Prism 7 (Ver. 7, GraphPad Software, Inc., La Jolla, CA, USA).
Plasmaprovberedning för UHPLC-ESI-QTOF-MS-analysPlasma (50 µL) blandades med 150 µL isopropanol (IPA), följt av 24-h inkubation vid 20 ◦C för att fälla ut proteinet. Alla prover centrifugerades två gånger vid 13,000× gat 4 ◦C under 10 min. Totalt 50 µL togs från varje prov och slogs samman i ett 1,5 mL mikrocentrifugrör för att konstruera ett kvalitetskontrollprov (QC) och 120 µL av varje provblandning överfördes till en HPLC-glasinsats.

UHPLC-ESI-QTOF-MS-analysUHPLC-ESI-QTOF-MS-analys användes vid Khon Kaen University International Phenome Laboratory (KKUIPL). Vattenfasextrakten av prover analyserades på en omvänd fasplattform. Separationsdelen utfördes med ett UHPLC-system (Bruker, Darmstadt, Tyskland) när Bruker intensitet solo HPLC C18 2.1 × 100 mm, 2 µm kolumn (Bruker, Darmstadt, Tyskland) användes. Kolonntemperaturen sattes till 55 ◦C och autosamplertemperaturen ställdes till 4 ◦C. Mobil fas A var 10{{20}} procent vatten av HPLC-kvalitet med 0,1 procent myrsyra (FA), och mobil fas B var 10 {{30}} procent metanol med 0,1 procent FA. Flödeshastigheten sattes till 0,4 mL/min och elueringsgradienten sattes till—99,9 procent A (0.{{40}}–2.{{46 }} min, 0.25 mL/min), 99,9–75 procent A (2.0–10.0 min, 0. 4 mL/min), 2{{60}} procent A (10,0–12,0 min, 0,4 mL/min), 10 procent A (12,0–21,0 min, 0,4 mL/ min), 0,1 procent A (21,0–23,0 min, 0,4 ml/min), 99,9 procent A (24,0–26,0 min, 0,4 ml/min). En provinjektionsvolym på 4 µL applicerades för både positiva och negativa joniseringspolaritetslägen.
Masspektrometrianalyser utfördes med användning av ett kompakt ESI-Q-TOF-system (Bruker, Darmstadt, Tyskland). Natriumformiat (HCOONa) innehållande 2 mM natriumhydroxid, 0,1 procent FA och 50 procent IPA injicerades direkt som en extern kalibrering med flödeshastighet 0,5 µL/min. Tillståndet i positiv joniseringspolaritetsläge—massområde 50–1300 m/z, konspänning 31 V, kapillärspänning 4500 V, källtemperatur 220 ◦C, desolvationstemperatur 220 ◦C, desolvationsgasflöde 8 L/min. Villkoren för negativ joniseringspolaritet – m/z-intervall: 50–900 m/z, konspänning 31 V, kapillärspänning 4500 V, källtemperatur 220 ◦C, desolvationstemperatur 220 ◦C, desolvationsgasflöde 8 L/min.
TarmmikrobiomanalysDNA extraherades med hjälp av QiAamp® PowerFecal® Pro DNA-kit (Qiagen, Hilden, Tyskland). Extraherat DNA mättes vid OD 260/280 med användning av en Nanodrop2000c spektrofotometer (Thermo scientific, Waltham, MA, USA). Allt extraherat DNA bevarades vid t20 ◦C fram till analyser. V3-V4-regionen av 16S ribosomala RNA (rRNA)-genen för varje prov amplifierades med användning av den universella framåtriktade primern V3 (50-CCTACGGGNGG CWGCAG-30) och den omvända primern V4 ({ {11}}GACTACHVGGGTATCTAATCC-30). PCR-reaktionen bestod av 2x KAPA HiFi HotStart ReadyMix, 12,5 ng DNA-mall och 5 µM av varje primer, med initial denaturering vid 95 ◦C i 3 minuter följt av 25 cykler av denaturering vid 95 ◦C i 30 s, 55 annealing C i 30 s, förlängning vid 72 ◦C i 30 s, och sista förlängning vid 72 ◦C i 10 min. En Agilent DNA 1000 Chip och Agilent 2100 Bioanalyzer (Agilent Technologies, Palo Alto, CA, USA) kombinerades för att kvantifiera den amplifierade produkten. PCR-amplikoner renades med användning av AMPure XP-pärlor för att rena. Den partiella 16S rRNA-genen sekvenserades med hjälp av Illumina MiSeq-plattform (Illumina Inc., San Diego, CA, USA).
16S rRNA-sekvenseringsbiblioteket preparerades med hjälp av genomiskt DNA (gDNA), och matchande parade ändsekvenser slogs samman med FLASH (http://ccb.jhu.edu/software/ FLASH/ (tillgänglig den 29 juni 2020)) [27] . Kvalitetsfifiltrering tog bort sekvenser som innehöll avläsningar av låg kvalitet och utfördes med CD-HIT-OTU (http://weizhong-lab.ucsd.edu/cd-hit-otu (tillgänglig den 29 juni 2020)) [28] och rDnaTools paket. OTUs (Operational taxonomic units) klassificerades med 97 procent tröskelidentitet med hjälp av UCLUST-algoritm baserad på 100 procent likhet. Sekvenser som delar Större än eller lika med 97 procent likhet tilldelades samma OTU. Representativa OTU-sekvenser anpassades och klassificerades taxonomiskt med Ribosomal Database Project (RDP) och jämfördes med referens NCBI-databaserna. Klassificeringen baseras på Green genes-databasen (http://greengenes.lbl. gov/ (tillgänglig den 29 juni 2020)). Resultatet av en klassificering av läsningar på flera taxonomiska nivåer - rike, filum, klass, ordning, familj, släkte och arter med hjälp av Quantitative Insights Into Microbial Ecology (QIIME) [29].
Statistisk analysDen statistiska analysen av föda och vattenintag, urinvolym och kroppsvikt rapporterades som medelvärde ±SD per grupp av djur och skillnaderna mellan grupperna jämfördes för statistisk signifikans med Students t-test med p-värde < {{2} }.05 anses vara statistiskt signifikant.
Resultat
PÅVERKAN av MSG på mat- och vattenintag, kroppsvikt och urinvolymMSG-behandlade råttor och kontrollråttor hade en liknande mängd födointag (17,44 ± 1,94 respektive 18,46 ± 1,37 g/råtta/dag) (Figur 1A) och kroppsvikt (333,58 ± 17,23 respektive 333,80 ± 15,50 g)/råtta. (Figur IB). Vattenintaget var dock betydligt högre hos MSG-behandlade råttor (52,38 ± 18,36 ml/dag) jämfört med kontroller (38,38 ± 8,39 ml/dag) (Figur 1C). I både MSG-behandlade och kontrollgrupper tenderade urinuttaget att öka med tiden, även om en signifikant ökning endast sågs hos MSG-behandlade råttor (15,42 ± 3,92 ml/råtta/dag vid förbehandling och 29,09 ± 8,78 ml/råtta/ dag efter behandling). Även om det inte var statistiskt signifikant var urinproduktionen från MSG-behandlade råttor (29,09 ± 8,78 ml/råtta/dag) uppenbarligen högre än hos kontrollerna (23,15 ± 10,55 ml/råtta/dag) (Figur 1D).

Metaboliska förändringar i metaboliskt viktiga organNMR-spektra för de insamlade vävnadsproverna analyserades efter två veckors MSG-behandling. PCA av NMR-spektraldata utfördes initialt för att observera alla uppenbara kluster och extremvärden (Figur 2). Den tydliga klustringen och fullständiga separationen observerades i levermetabolitprofiler mellan kontrollgruppen och MSG-behandlade gruppen med ett permutations-p-värde på 0.002, R2X på 58 procent , Q2Y på 0,84 och R2Y på 0,93 illustrerade i PCA- och O-PLS-DA-poängdiagram (Figur 2A, B). En representativ OPLS-motsvarande koefficient laddningsdiagram med metabolittilldelning presenteras i figur 3 med signifikantlevermodeller som anges i figur 3A; alla signifikanta förändringar i metaboliter sammanfattas i tabell 1. I levern hittades högre nivåer av sex metaboliter inklusive glukos, pyridoxin, 2-deoxiuridin, inosin, okänd 1 och 2 i den MSG-behandlade gruppen, medan elva metaboliter , nämligen leucin, isoleucin, valin, alanin, N-acetylglykoprotein, aceton, 1,3-dimetylurat, histamin, xantin, kynurenat och nikotinamid, var signifikant högre i kontrollgruppen. PCA-poängplotten baserad pånjur-metaboliter (Figur 2C) visade ingen tydlig klustring mellan två grupper, och O-PLS-DA-modellen var statistiskt signifikant med ett permutations-p-värde på 0.018, R2X på 56 procent, Q2Y av 0.29 och R2Y på 0.74 (Figur 2D). Två förändrade metaboliter hittades injurvävnadermed signifikant högre trimetylaminnivå och signifikant lägre pyridoxin i den MSG-behandlade gruppen jämfört med kontroller (Figur 3B). Däremot avslöjade resultaten av jejunum (Figur 2E, F), feces och plasma (Figur 2 och Figur S1) ingen klustring mellan behandlings- och kontrollgrupperna som illustreras i PCA- och O-PLS-DA-poängdiagram.


Korrelationsvägarna för de signifikanta metaboliterna ileverochnjurvävnaderundersöktes med hjälp av KEGG ID:n och genererade av Cytoscape-programvaran. Metaboliterna visade sig länka det metaboliska nätverket. När dessa resultat kombinerades för att rita en metabolisk vägkarta för att illustrera en mer intuitiv korrelation, visade sig metaboliterna huvudsakligen vara associerade med metaboliska vägar, såsom leverglukoneogenes, grenkedjiga aminosyror, vitamin B6 och trimetylaminmetabolismer ( Figur S3).

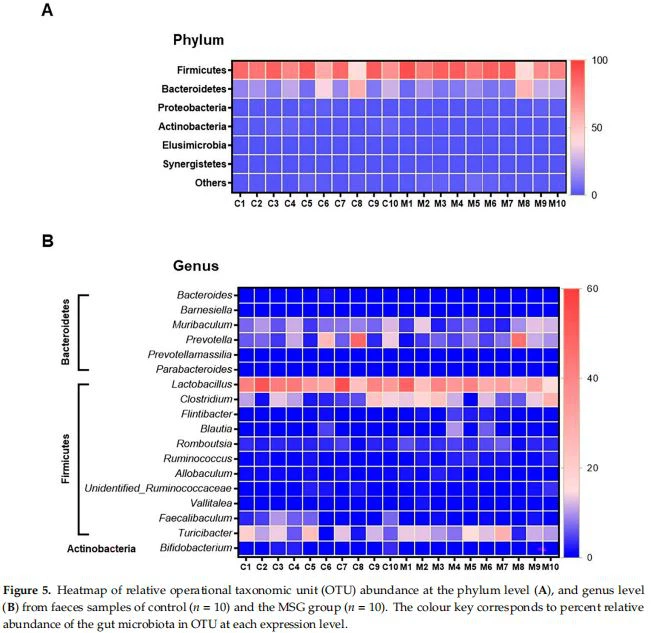
MSG-konsumtion förändrar tarmmikrobiomResultaten av analys av avföring av bakteriell sammansättning visade på sju phyla, 15 klasser, 19 ordnar, 46 familjer, 127 släkten och 220 arter från alla djurgrupper. De 7–10 bästa arterna valdes ut och procentuell relativ förekomst av bakteriesamhällen på fylum, klass, ordning, familj, genus och artnivåer genererades (Figur 4). På filumnivån var de fyra översta relativt rikliga filorna i följande ordning: Firmicutes > Bacteroidetes > Proteobacteria > Actinobacteria hos alla djur (Figur 4A). Förekomsten av Actinobacteria var signifikant lägre hos MSG-behandlade råttor (0,30 procent) än hos kontrollråttor (1,32 procent) (Figur 5A).
På klassnivå var den vanligaste mikrobiotan Baciller > Clostridia > Bacteroidia > Erysipelotrichia hos alla djur (Figur 4B). Den MSG-behandlade gruppen hade signifikant högre Clostridia (31,59 procent) än kontrollgruppen (19,25 procent). De MSG-behandlade råttorna hade dock signifikant lägre Actinobacteria (0,15 procent) än kontrollråttor (1,09 procent) (Figur 4B). När de tolkades på ordningsnivå var Lactobacillales, Clostridiales, Bacteroidales, Erysipelotrichales rikliga hos alla djur (Figur 4C). Clostridiales var signifikant högre hos MSG-behandlade råttor (31,59 procent) än hos kontrollråttor (19,25 procent), medan Bifidobacteriales var signifikant lägre hos MSG-behandlade råttor (0,06 procent) jämfört med kontrollråttor (1,06 procent).
De fyra vanligaste familjerna som vanligtvis observerades i alla försöksdjur var i följande ordning - Lactobacillaceae > Erysipelotrichaceae > Clostridiaceae > Prevotellaceae (Figur 4D). På familjenivå var Bififidobacteriaceae signifikant lägre, men oidentifierade Clostridiales var signifikant högre hos MSG-behandlade råttor jämfört med kontrollråttor. Den relativa förekomsten av topp fyra släkten som observerades i alla djuren var i följande ordning - Lactobacillus > Turicibacter > Prevotella < clostridium="" (figur="" 4e).="" en="" värmekarta="" över="" de="" relativa="" förekomsterna="" på="" släktnivå="" visade="" lägre="" förekomst="" av="" lactobacillus="" och="" högre="" förekomst="" av="" clostridium="" i="" msg-behandlade="" råttor="" (figur="" 5b).="" dessutom="" observerades="" det="" lägre="" förekomsten="" av="" bifidobacterium="" även="" hos="" msg-behandlade="" råttor="" (0,06="" procent)="" jämfört="" med="" kontrollråttor="" (1,06="">
På artnivå var de fyra främsta tarmbakteriearterna vanliga hos alla råttor Lacto bacillus intestinalis, Turicibacter sanguinis, Clostridium saudiense och Muribaculum intestinale i ordning (Figur 4F). I den MSG-behandlade gruppen var Flintibacter butyricus signifikant mer förekommande än i kontrollgruppen, medan Faecalibaculum rodentium och Bififidobacterium pseudolongum var betydligt mindre förekommande.

Diskussion
Flera bevis har konsekvent kopplat MSG-konsumtion till negativa effekter på människors hälsa, såsom högre förekomst av metabolt syndrom [3], övervikt [4,5] och arteriell hypertoni [6]. Icke desto mindre har data varit motstridiga i vissa fall och de underliggande mekanismerna är fortfarande oklara. För att ta itu med detta problem undersökte vi de metaboliska förändringarna i vävnaden och de mikrobiella förändringarna i tarmen som induceras av MSG-konsumtion. Som illustreras i den schematiska representationen i figur 6, förändrade MSG-konsumtion metaboliterna associerade med leverglukoneogenes, metabolism med grenad aminosyra (BCAA), vitamin B6 och trimetylaminmetabolism. Dessutom undertryckte den kortsiktiga MSG-konsumtionen den relativa förekomsten av Bififidobacterium, som anses vara en nyttig bakterie, och Clostridium relaterad till TMA- och TMAO-produktion [30].

I levern var metaboliter som glukos, pyridoxin (B6), 2-deoxiuridin, inosin, okänd 1 och 2 signifikant högre hos MSG-behandlade djur än hos kontroller, medan elva metaboliter (dvs. leucin, isoleucin, valin) , alanin, N-acetylglykoprotein, aceton, 1,3-dimetylurat, histamin, xantin, kynurenat och nikotinamid) var signifikant lägre. För det första kan högre nivåer av glukos indikera en ökning av leverglukoneogenes associerad med MSG, vilket är i överensstämmelse med tidigare rapporterad hög plasmaglukos hos nyfödda grisar som får MSG-tillskott (1 g/kg kroppsvikt) [31]. För det andra kan de reducerade nivåerna av alanin och tre BCAA, inklusive valin, leucin och isoleucin, korrelera med aminosyrakatabolism och energimetabolism där deras kolskelett kan användas som prekursorer för glukoneogenes (alanin, valin och isoleucin som glukogena aminosyror) och energiproduktion via trikarboxylsyracykeln (TCA). I överensstämmelse med den tidigare rapporten fann vi att nedbrytningsprodukterna av leucin och lysin, beta-hydroxiisovalerat respektive 5-aminovalerat, var signifikant högre i urinen hos MSG-behandlade råttor [13]. För det tredje, förhöjt pyridoxin ileveroch minskat pyridoxin injureav MSG-behandlade råttor föreslog förändring av vitamin B6-metabolismen. Vi fann också minskade nivåer av histamin, kynurenat och nikotinamid ileverav MSG-behandlade råttor, som är produkter av B6-beroende enzymer i histidin- och tryptofanmetabolismen. Sambandet mellan MSG-intag och metabolism av vitamin B6, histidin och tryptofan behöver undersökas ytterligare. För det fjärde hade MSG-behandlade råttor högre nivåer av trimetylamin (TMA) injure. TMA syntetiseras från kostbeståndsdelar, inklusive kolin, L-karnitin och betain genom inverkan av mikrobiella enzymer [16]. TMA absorberas till stor del på ett passivt sätt i portalcirkulationen och oxideras huvudsakligen till trimetylamin-N-oxid (TMAO) av lever-flavin-innehållande monooxygenaser (FMO). En mindre del av TMA oxideras till dimetylamin (DMA) och metylamin (MA) och utsöndras slutligen i urinen [32,33]. Högre nivåer av DMA och MA i urinen från MSG-behandlade råttor rapporterades tidigare [13]. Flera studier har visat att de förhöjda TMA-prekursorerna, kolin, eller dess metaboliter, TMAO, kan leda till progressivnjur-tubulointerstitiell fifibros, kardiovaskulär sjukdom och kronisknjursjukdom[34–36]. Därför är den förhöjda nivån av TMA injurekan utgöra länken mellan MSG-intag ochnjurskada.
Med utgångspunkt från de observerade förändringarna i TMA, undersökte vi tarmmikrobiotan hos MSG-behandlade råttor och visade förändringen av de två stora phyla, Firmicutes och Bacteroidetes. Det högre förekomsten av Firmicutes, men lägre förekomsten av Bacteroidetes, observerades hos MSG-behandlade råttor. På släktnivå hade MSG-behandlade råttor högre överflöd av Clostridium och lägre förekomst av Lactobacillus och Bifidobacterium. Släktet Clostridium omfattar en grupp mikroorganismer som tillhör phylum Firmicutes. Vissa Clostridium spp. är associerade med TMA-metabolism genom att producera enzymer för att omvandla kolin eller dietbeståndsdelar till TMA [33,37,38]. De ökade TMA-producerande tarmbakterierna, dvs Clostridium spp., stöder höjningen av TMA-metaboliter injureoch urin från MSG-behandlade råttor. Dessutom minskade MSG-konsumtionen Bifidobacterium-populationen, en probiotisk bakterie som spelar viktiga roller i tarmens homeostas och hälsa [39]. Enkla och smältbara kolhydrater som laktos och sackaros omsätts i den övre mag-tarmkanalen av värden och bakterier som laktobaciller. Emellertid metaboliseras icke-smältbara kolhydrater, dvs kostfiber, i det nedre mag-tarmkanalen av medlemmarna i tarmmikrobiotan, inklusive Bififidobacterium. En diet med höga halter av mättade fetter och enkla sockerarter men utarmad på kostfiber som en diet i västerländsk stil kan bidra till ett lägre antal nyttiga bakterier [40]. Minskningen av Bififidobacterium, en bra bakterie, har rapporterats vid kroniska inflammatoriska sjukdomar som fetma [41], hepatit B [42] och diabetes [43,44]. Effekten av MSG-konsumtion på tarmmikrobiotan hos människor rapporterades tidigare utan några signifikanta förändringar i mikrobiell sammansättning jämfört med baslinjen [45]. Den låga effekten av MSG på tarmmikrobiotan i denna studie kan bero på den låga dosen av MSG-tillskott (2 g/dag), eftersom det genomsnittliga dagliga MSG-intaget i vår observation är 4 g/dag [3]. Vi fann att varje 1 g dagligt MSG-intag ökade risken för att ha metabolt syndrom. Även om mekanismen för MSG-konsumtion som leder till metabola sjukdomar inte är etablerad, kan minskningen av Bifidobacterium hos MSG-behandlade djur vara en ledtråd. Tillfälligtvis liknar den minskade Bifidobacterium i MSG-behandlade råttor som hittats i denna studie den hos råttor med vitamin B6-brist [46]. Den intensiva studien av hur MSG minskar goda bakterier och förändrar vitamin B6-status behöver utredas ytterligare.

Vi visade att MSG-konsumtion inducerade lever ochnjur-metabola förändringar involverade i glukoneogenes och grenkedjig aminosyra, vitamin B6 och TMA-metabolism, åtföljda av förändringar i tarmmikrobiotans sammansättning. Dessa observationer tyder på att de förändrade metabola vägarna kan vara associerade med skadliga effekter av långvarig MSG-konsumtion, särskilt påleverochnjure.
