Del 1 Heme Oxygenases roll-1 som immunmodulator vid njursjukdom
Jun 05, 2023
Abstrakt
Proteinet hemoxygenas (HO)-1 har varit inblandat i reglerna för flera immunologiska processer. Det är välkänt att njurskador påverkas av immunmekanismer och att olika njursjukdomsformer kan vara ett resultat av autoimmun sjukdom. Den aktuella studien beskriver i detalj rollen av HO-1 vid njursjukdom och ger de senaste observationerna av effekten av HO-1 på immunvägar och svar både i djurmodeller av immunmedierade sjukdomsformer och slutenvårdsstudier.
Nyckelord
hem oxygenas; njure; immunskada.

Klicka här för att fåCistanche fördelar
Inledning Heme-oxygenas (HO)-1 har kopplats till reglerna för immunologiska och patofysiologiska processer, såsom inflammation, apoptos och cytoprotection, främst genom dess nedströms effektormolekyler, kolmonoxid, bilirubin och biliverdin. Inflammation och autoimmuna sjukdomar är nyckelfaktorer för njursjukdom. I njurarna kan glomerulära kapillärer bli mål för inflammation, vilket i slutändan leder till allvarlig och irreversibel vävnadsskada. Inblandningen av HO-1 i immunmedierade former av njurskada har studerats omfattande. Den aktuella studien beskriver i detalj den potentiella rollen av HO-1, i olika former av njurskador, som en förmedlare av immunologiska mekanismer som driver sjukdomens manifestation och progression.
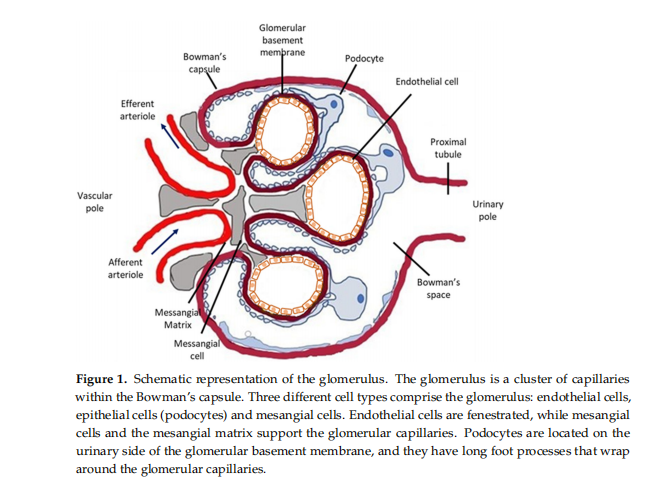
De olika formerna av njurskada uppstår vanligtvis på grund av skada på njurglomerulus. På grund av sin mycket specialiserade struktur och funktion är njurglomeruli kända för att vara särskilt känsliga för skador. Kortfattat är glomerulus (Figur 1) en tri-cellulär struktur omgiven av den glomerulära (Bowmans) kapseln. Endotelceller kantar den luminala sidan av det glomerulära basalmembranet (GBM); epitelceller, även kända som podocyter, är förankrade på den yttre ytan av GBM; och mesangiala celler stödjer kapillärslingorna. Glomeruli bildar en komplex mikrovaskulär bädd, den glomerulära tuften, som fungerar som ett mycket selektivt plasmafilter samtidigt som de behåller högmolekylära molekyler och celler i cirkulationen (Figur 1).
HO-1 och IgA nefropati
IgA-nefropati är en form av kronisk glomerulonefrit som kännetecknas av avsättning av IgA-immunkomplex i glomeruli. Det är den vanligaste formen av glomerulonefrit i världen (1] Majoriteten av fallen är idiopatiska, men på senare år har sekundära former av sjukdomen uppträtt efter olika infektioner (Haemophilus para in. influenza, HIV cytomegalovirus)[2].
Symtom inkluderar uppkomsten av makroskopisk hematuri vanligtvis en eller två dagar efter en afebril infektionsepisod, vilket efterliknar infektiös glomerulonefrit. Urinanalys av patienter med lgA har upptäckt förekomsten av deformerade röda blodkroppar och ibland avgjutningar av röda blodkroppar. Mild proteinuri (<1 g/day) is also typical and may occur without hematuria, while serum creatinine levels are usually normal at diagnosis [3].
Den patogena mekanismen som orsakar IgA-nefropati är fortfarande okänd, men ackumulerade bevis har lett till "fyraträffshypotesen", som börjar med ett onormalt glykosyleringsmönster av IgA (galaktosbrist IgA1) som manifesteras genom ökade nivåer av dåligt O-galaktosylerad lgA1 (gd) -lgA1) i blodcirkulationen, vilket orsakar produktionen av cirkulerande autoantikroppar och följaktligen bildandet och avsättningen av immunkomplex i mesangium [4,5].
Diagnosen av IgA-nefropati bekräftas med en njurbiopsi och immunfluorescensmetodik, som avslöjar granulära IgA- och komplementfaktor 3 (C3) avlagringar lokaliserade i mesangium med foci av proliferativa eller nekrotiska segmentella lesioner. MesangiallgA-avlagringar anses dock vara ospecifika och kan upptäckas vid många andra störningar såsom immunglobulin A-relaterad vaskulit, HIV-infektion, psoriasis, lungcancer och flera andra störningar i bindväven. Undersökning av njurvävnadssnitt erhållna från IgA-patienter, under ett elektronmikroskop, visade ökad cellularitet och en ökad matris i mesangium, den endokapillära proliferationen av neutrofiler och subendotelavlagringar. Slutligen detekteras normala nivåer av komplementfaktorer med immunanalyser, medan en förhöjd lgA-plasmakoncentration ibland kan detekteras med serumelektrofores (6].

Cistanche-tillskott och Cistanche-piller
Kväveoxid (NO) och avancerade oxidationsproteinprodukter (AOPP) är starka markörer för oxidativ stress, och deras förhöjda koncentrationer har bestämts i serumprover från patienter med svår IgA-glomerulopati [7]. Nakamura et al. jämförde patienter som led av IgA-nefrit med friska kontroller, vilket visade att exponering för oxidativ stress i IgA var av skadlig betydelse för utvecklingen av njurskada [8]. Detta kan bero på underuttrycket av superoxiddismutas (SOD) och den åtföljande exacerbationen av vävnadsskada på grund av undertryckandet av reaktiva syreämnen (ROS) rensande förmåga (10). Vidare har studier identifierat en upprepad dinukleotidguanosintymin (GT) polymorfism av HO-1-genpromotorn som resulterar i ökat HO-1-uttryck när GT-längden är kortare (S-allel) snarare än när den är längre (L-allel). Dessa två olika alleler kan påverka uppkomsten och utvecklingen av många olika njursjukdomar [9], och flera studier har visat ett direkt samband mellan korta (GT)n upprepningar och en högre induktionshastighet av HO-1, vilket främjar progression av IgA nefropati [10].
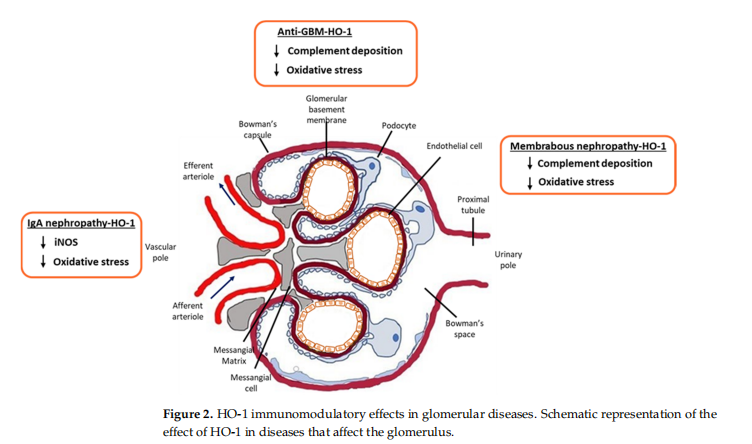
Efter intravaskulär hemolys frigörs fritt hem, det naturliga substratet av HO-1 och en kraftfull aktivator av komplementkaskaden. Heme har rapporterats aktivera den alternativa komplementvägen [11] och kan därför vara inblandad i komplementmedierad njurskada [12]. Fritt hem påverkar medfödda immunsvar genom aktivering av Toll-liknande receptor 4 och ROS-beroende vägar, som i sin tur, genom komplexa signalvägar, främjar uttrycket av proinflammatoriska cytokiner. Dessutom utgör biprodukter av hemnedbrytning (CO, biliverdin, bilirubin) och HO-1 nyckelmolekyler som uppreglerar utsöndringen av antiinflammatoriska cytokiner, såsom IL-10 [13] (Figur 2). Å andra sidan är många pro-inflammatoriska enzymer, såsom cyklooxygenas-2 (COX-2) och inducerbart kväveoxidsyntas (iNOS), hemoproteiner vars funktioner kan försämras på grund av otillräckligt fritt hem när det hem har katalyserats av HO-1 [14]. Mikro- och/eller makroskopisk hematuri är ett typiskt symptom på IgA-nefropati som tyder på potentiell induktion av HO-1 i glomeruli [15]. En tidigare studie använde olika koncentrationer av hemin för att inducera glomerulär HO-1-expression in vitro och rapporterade att när koncentrationen av hemin nådde en kritisk nivå på 200 µM, började HO-1-uttrycket att minska. Detta kan delvis förklaras av det faktum att olika former av glomerulär sjukdom uppvisar ökade nivåer av fria radikaler (OH−), väteperoxid (H2O2) och aktivt Fe2 plus. Dessa kan ytterligare förstärkas av hemnedbrytningen av HO; därför kan en HO-1-uttrycksbegränsande mekanism vara nödvändig [16].
Det kliniska förloppet för IgAN är mycket varierande. I många fall går sjukdomen obemärkt förbi och kräver ingen behandling. De viktigaste parametrarna som påverkar sjukdomsprogression inkluderar graden av proteinuri, okontrollerbar hypertoni och histopatologiska lesioner på biopsier [17].
Patientbedömning utförs vanligtvis med "IgA Nephropathy Prediction Tool" (IIgAN-PT) som använder parametrar som histologiska fynd, eGFR, graden av proteinuri, blodtrycksvärdet, medicinering före biopsi och demografi (sex, ålder, etnicitet) ) för att uppskatta den individuella femåriga risken för njurprogression mot njursjukdom i slutstadiet (ESRD). Oberoende av IIgAN-PT-resultat bör alla patienter få stödjande hypertoni- och proteinuribehandling. Understödjande terapi består av mediciner som hämmar renin-angiotensin-axonet, såsom angiotensinreceptorblockerare (ARB) eller angiotensinomvandlande enzymhämmare (ACEi) [18]. Dessa minskar både systemiskt och intraglomerulärt blodtryck – och därmed glomerulär skada på grund av hypertoni – och sänker graden av proteinuri. Om en patients eGFR är större än 30 ml/min/1,73 m2, tillsats av natrium-glukos co-transporter 2 (SGLT2) till deras terapi kan ytterligare minska proteinuri [19]. Slutligen, på grund av toxicitetseffekter, stöds användningen av steroider endast i fall av snabb minskning av njurfunktionen och okontrollerad ökning av proteinuri [20].
HO-1 och membranös nefropati (MN)
MN är en autoimmun glomerulär sjukdom och en viktig orsak till nefrotiskt syndrom i den vuxna befolkningen. Symtom inkluderar smygande ödem, framträdande proteinuri med milda urinsediment, normal eller försämrad njurfunktion och normalt eller förhöjt blodtryck 21]. Spontan remission kan ses hos cirka 30 procent av patienterna. I de flesta fall (cirka 70 procent) rapporteras MN som idiopatisk. I dessa fall är antikroppar mot M-typ fosfolipas A2-receptorn (PLA2R) som finns i podocyter kopplade till det specifika stället och bildar immunkomplex in situ som aktiverar komplementmembranattackkomplexet (MAC, C5b-9). Men MN kan också utvecklas som sekundär MN på grund av en specifik etiologisk faktor. De främsta orsakerna är solida tumörer (lunga, tjocktarm, ändtarm, njure, bröstmage), autoimmuna sjukdomar och mikrobiella infektioner. Faktum är att i områden som är endemiska för infektioner, såsom malaria eller schistosomiasis, kommer det senare att bestå av huvudorsaken till MN [21].
Diagnosen MN baseras också på njurbiopsi. Optisk mikroskopi avslöjar den diffusa förtjockningen av GBM som en reaktion på subepitelial bildning av immunkomplex. Ingen cellulär hyperplasi eller inflammatoriska celler detekteras. Det glomerulära basalmembranet tjocknar homogent men skapar gradvis utsprång i det subepiteliala utrymmet som så småningom omfattar och integrerar immunkomplexen i det. Immunfluorescens detekterar granulära avlagringar av lgG och C3 längs källarmembranet. kli, medan elektronmikroskopi avslöjar diffus utplåning av podocytfotsprocesser såväl som täta avlagringar i subepitelområdet (21]. Heymann et al. beskrev för första gången en experimentell råttmodell av MN där immunkomplexens patogena roll var bekräftat (22]. Heymann nefrit (HN) inducerades genom injektioner av proximala tubuli-borstkantantigener (aktivt HN) eller deras motsvarande antikroppar (passiv HN) i råttor. Autoantigenmålet i HNis megalin, ett transmembranprotein beläget i borstkanten av proximala tubuli och på podocytfotsprocesser hos råttor (23]. Studier av aktivt och passivt HN visade att subepiteliala avlagringar bildas in situ mot ett konstitutionellt endogent antigen snarare än genom ett cirkulerande immunkomplex 24). HN-modellen har gjort det möjligt för forskare för att identifiera den viktiga rollen av komplementmedierad cytotoxicitet vid podocytskada och proteinuri i denna modell Tidiga studier i HN visade samlokalisering av C3 och C5b-9 till immunavlagringarna. Dessutom visades det att podocyterna som fanns i urinen från passiva HN-råttor var belagda med C5b-9 [25]. HN-progression korrelerade med ihållande urinutsöndring av C5b-9, vilket indikerar kontinuerlig komplementaktivering vid GBM.

Herba Cistanche
Membranbundna proteiner, kända som komplementregulatoriska proteiner (CRP), verkar för att eliminera komplementaktivering och därför MAC-bildning och lys. En välkänd CRP är den sönderfallsaccelererande faktorn (DAF, CD55). DAF accelererar sönderfallet av C3- och C5-konvertaser och begränsar därmed MAC-bildning [26]. Hos råttor är andra CRP:er Crry och CD59 [26]. Studier av DAF-uttryck hos råttor har avslöjat konstitutivt DAF-uttryck uteslutande i podocyter [27]. För att studera den skyddande rollen av DAF i komplementinducerad podocytskada, genererade en tidigare studie en transgen råttmodell av DAF-utarmning (Daf -/-) [28]. Histologiska, kliniska och biokemiska undersökningar (kreatininnivåer, albuminuri, urinalbumin till urinkreatininkvot) hos Daf plus/plus och Daf −/− råttor visade inga signifikanta skillnader före administrering av komplementfixerande antikropp anti-Fx1A. Efter administrering av anti-Fx1A var proteinurinivåerna signifikant förhöjda hos Daf -/- råttor. Immunfluorescensfärgning hos råttor som fick anti-Fx1A visade på större C3-avsättningar i Daf -/- råttor än i Daf plus / plus råttor, vilket tyder på en skyddande roll för DAF vid podocytkomplementinducerad skada [28]. Flera studier har visat att HO-1 uppreglerar DAF, vilket i sin tur minskar komplementaktivering och komplementmedierad skada [16]. I det sammanhanget kan HO-1-induktion vara ett användbart verktyg som en potentiell behandlingsstrategi mot komplementmedierad glomerulonefrit via dess immunmodulerande effekter, inklusive DAF-induktion.
För att utforska de tidigare nämnda egenskaperna hos HO-1, Wu et al. använde en experimentell djurmodell av inducerad MN i BALB/c-möss genom att introducera intravenöst katjoniskt bovint serumalbumin och dela upp djuren i tre grupper. Den första gruppen behandlades med en veckovis intraperitoneal administrering av koboltprotoporfyrin (CoPP), en HO-1-inducerare; den andra med tennprotoporfyrin (SnPP), en HO-1-hämmare; och den tredje med saltlösning. MN-CoPP-gruppen uppvisade en HO-1-uppreglering och visade en tydlig förbättring av symtomen (en minskning av proteinuri och normalisering av serumalbumin- och kolesterolnivåerna). CoPP-behandling minskade också signifikant produktionen av anti-cBSA-antikroppar i serum. Även om immunfluorescensfärgning förblev positiv för alla tre grupperna, uppvisade MN-CoPP-gruppen lägre intensitet i det glomerulära membranet och minskade C3-avsättningar avseende de andra två grupperna, särskilt MN-SnPP-gruppen. Koncentrationerna av markörer för oxidativ stress, såsom tiobarbitursyrareaktiva substanser (TBARS), utvärderades både i serum och njurar och visade sig vara avsevärt högre för icke-MN-möss, men signifikanta skillnader bedömdes mellan MN-CoPP-gruppen och MN-SnPP-gruppen. CoPP-behandling minskade oxidativ stressmarkörer både i serum och njurar, vilket tyder på att HO-1 kan ha en antioxidativ effekt på lokal och systemisk nivå [29].
Komplementaktivering verkar inducera ROS i podocyter som genomgår mitokondriell dysreglering i MN [24]. Pyroptos är en nyligen identifierad typ av reglerad celldöd som följer på bakteriella eller virusinfektioner (40). Komplexa signalvägar, inklusive aktivering av inflammasomer och pro-inflammatoriska cytokiner, leder till aktivering av kaspas-1 och följaktligen bildning av porer på membranen, vilket resulterar i celldöd och överskott av pro-inflammatoriska cytokiner och ROS [30]. Wang et al. beskrev komplementmedierad pyroptos i podocyter med samtidig mitokondriell depolarisering och ROS-produktion. Blockering av ROS-produktion omvände komplementmedierad pyroptos. Immunhistokemi av MN glomeruli bekräftade samlokaliseringen av pyroptosrelaterade proteiner, såsom kaspas-1 och gastrin D (GSDMD), såväl som synaptopodin, ett aktinassocierat protein som finns i podocyter. Dessutom främjade C3a och C5a överuttryck av kaspas-1 och GSDMD i podocyterna in vitro och påverkade integriteten hos cellmembranen och depolariseringen av podocyternas mitokondriella membran. När podocyterna från MN-patienter inkuberades med hämmare av viktiga pyroptosmolekyler, påverkade inte C3a och C5a podocytmembranintegriteten [31].

Cistanche-extrakt
Nyligen genomförda studier har utvärderat rollen av HO-1 för att blockera pyroptos. Kolmonoxid (CO) som en biprodukt av HO-1-katalysen av hemin verkar blockera aktivering av kaspas-1 genom direkt hämning av dess inducermolekyl, NLRP3-ASC [32,33] . Den NFE2-relaterade faktorn (Nrf2) är en transkriptionsfaktor som reglerar det cellulära antioxidantsvaret på oxidativ stress genom att inducera uttryck av antioxidant- och cytoskyddande molekyler, varav en är HO-1 [34]. Sirtuin är ett deacetylasprotein som är väsentligt för integriteten hos podocyternas cytoskelett [35]. Under stressförhållanden verkar sirtuin inducera överuttryck av Nrf2 vilket leder till uppreglering av HO-1-uttryck i podocyter [36]. I en murin njurischemi/reperfusion (I/R) skademodell, Diao et al. undersökte rollen av den NF-E2-relaterade faktorn/hemoxygenasen-1 (Nrf2/HO-1) som en skyddande faktor mot pyroptos [37]. Proteinargininmetyleringstransferas 5 (PRMT5) är involverad i ett stort antal fysiologiska och patologiska tillstånd, bland dem embryonal utveckling, vävnadshomeostas och maligniteter [38]. PRMT5 är inblandad i I/R-inducerad ROS-produktion. Dess hämning resulterade i en uppreglering av Nrf2/HO-1, en minskning av oxidativ stressmarkörer och en minskning av vävnadsskada [37].
Det mycket varierande förloppet av MN gör att dess personliga behandling är avgörande beroende på risken för njurfunktionsnedsättning. Spontan remission kan inträffa hos cirka 30 procent av patienterna; dock bör alla patienter med proteinuri behandlas antingen med en angiotensinreceptorblockerare (ARB) eller en ACEi under tre till sex månader. Enligt de senaste MN-behandlingsriktlinjerna ska alla patienter bedömas för anti-M-typ fosfolipas A2-receptor (PLA2R) antikroppsnivåer i blodet före och under behandlingen, eftersom det saknas anti-PLA2R-antikroppar hos en patient med en initial positiv test indikerar remission. Kortikosteroider plus administrering av cyklofosfamid, tillsammans med understödjande terapi, rekommenderas för patienter med allvarligt nefrotiskt syndrom och en snabb nedgång i njurfunktionen i början av sjukdomen [39]. Hos måttlig till högriskpatienter kan immunsuppressiv behandling med rituximab, kalcineurinhämmare (CNIs) och kortikosteroider plus cyklofosfamid användas om inte remission uppnås inom sex månader efter enbart understödjande terapi, om det inte är kontraindicerat på grund av gravt nedsatt njurfunktion, diffus interstitiell fibros eller återkommande infektioner [18].
Referenser
1. Barratt, J.; Feehally, J. IgA nefropati. J. Am. Soc. Nephrol. JASN 2005, 16, 2088–2097. [CrossRef]
2. Saha, MK; Julian, BA; Novak, J.; Rizk, DV Sekundär IgA nefropati. Kidney Int. 2018, 94, 674–681. [CrossRef]
3. Penfold, RS; Prendecki, M.; McAdoo, S.; Tam, FW Primär IgA nefropati: Aktuella utmaningar och framtidsutsikter. Int. J. Nephrol. Renov. Dis. 2018, 11, 137–148. [CrossRef] [PubMed]
4. Suzuki, H. Biomarkörer för IgA-nefropati baserade på patogenes med flera träffar. Clin. Exp. Nephrol. 2019, 23, 26–31. [CrossRef] [PubMed]
5. Dotz, V.; Visconti, A.; Lomax-Browne, HJ; Clerc, F.; Hipgrave Ederveen, AL; Medjeral-Thomas, NR; Cook, HT; Pickering, MC; Wuhrer, M.; Falchi, M. O- och N-glykosylering av serumimmunoglobulin A är associerad med IgA nefropati och glomerulär funktion. J. Am. Soc. Nephrol. JASN 2021, 32, 2455–2465. [CrossRef]
6. Yau, T.; Korbet, SM; Schwartz, MM; Cimbaluk, DJ Oxford-klassificeringen av IgA-nefropati: En retrospektiv analys. Am. J. Nephrol. 2011, 34, 435–444. [CrossRef]
7. Descamps-Latscha, B.; Witko-Sarsat, V.; Nguyen-Khoa, T.; Nguyen, AT; Gausson, V.; Mothu, N.; Cardoso, C.; Noel, LH; Guerin, AP; London, GM; et al. Tidig förutsägelse av IgA-nefropatiprogression: Proteinuri och AOPP är starka prognostiska markörer. Kidney Int. 2004, 66, 1606–1612. [CrossRef] [PubMed]
8. Nakamura, T.; Inoue, T.; Sugaya, T.; Kawagoe, Y.; Suzuki, T.; Ueda, Y.; Koide, H.; Node, K. Fördelaktiga effekter av olmesartan och temocapril på fettsyrabindande proteinnivåer av urinlevertyp hos normotensiva patienter med immunglobin A nefropati. Am. J. Hypertens. 2007, 20, 1195–1201. [CrossRef] [PubMed]
9. Courtney, AE; McNamee, PT; Heggarty, S.; Middleton, D.; Maxwell, AP Association of functional hem oxygenase-1 genpromotorpolymorfism med polycystisk njursjukdom och IgA-nefropati. Nephrol. Ringa. Transplantation. Av. Publ. Eur. Ringa. Transpl. Assoc.-Eur. Ren. Assoc. 2008, 23, 608–611. [CrossRef]
10. Chin, HJ; Cho, HJ; Lee, TW; Na, KY; Yoon, HJ; Chae, DW; Kim, S.; Jeon, USA; Gör, JY; Park, JW; et al. Genotypen hem oxygenas-1 är en riskfaktor för nedsatt njurfunktion av IgA-nefropati vid diagnos, vilket är en stark prediktor för dödlighet. J. Korean Med. Sci. 2009, 24, S30–S37. [CrossRef]
11. Merle, NS; Grunenwald, A.; Rajaratnam, H.; Gnemmi, V.; Frimat, M.; Figueres, ML; Knockaert, S.; Bouzekri, S.; Charue, D.; Noe, R.; et al. Intravaskulär hemolys aktiverar komplement via cellfritt hem och hemladdade mikrovesiklar. JCI Insight 2018, 3. [CrossRef]
12. Frimat, M.; Tabarin, F.; Dimitrov, JD; Poitou, C.; Halbwachs-Mecarelli, L.; Fremeaux-Bacchi, V.; Roumenina, LT Komplementaktivering av hem som en sekundär träff för det atypiska hemolytiska uremiska syndromet. Blood 2013, 122, 282–292. [CrossRef]
13. Li, Y.; Ma, K.; Han, Z.; Chi, M.; Sai, X.; Zhu, P.; Ding, Z.; Song, L.; Liu, C. Immunmodulerande effekter av Heme Oxygenase-1 vid njursjukdom. Främre. Med. 2021, 8, 708453. [CrossRef]
14. Gosselin, R.; Jeney, V.; Soares, MP Mechanisms of cell protection by heme oxygenase-1. Annu. Rev. Pharmacol. Toxicol. 2010, 50, 323–354. [CrossRef]
15. Shepard, M.; Dhulipala, P.; Kabaria, S.; Abraham, NG; Lianos, EA Heme oxygenas-1 lokalisering i råttnefronet. Nephron 2002, 92, 660–664. [CrossRef]
16. Detsika, MG; Lianos, EA Reglering av komplementaktivering av Heme Oxygenase-1 (HO-1) vid njurskada. Antioxidanter 2021, 10, 60. [CrossRef] [PubMed]
17. Trimarchi, H.; Barratt, J.; Cattran, DC; Cook, HT; Coppo, R.; Haas, M.; Liu, ZH; Roberts, IS; Yuzawa, Y.; Zhang, H.; et al. Oxford Classification of IgA Nephropathy 2016: En uppdatering från IgA Nephropathy Classification Working Group. Kidney Int. 2017, 91, 1014–1021. [CrossRef]
18. Rovin, BH; Adler, SG; Barratt, J.; Bridoux, F.; Burdge, KA; Chan, TM; Cook, HT; Fervenza, FC; Gibson, KL; Glassock, RJ; et al. Sammanfattning av KDIGO 2021-riktlinjen för hantering av glomerulära sjukdomar. Kidney Int. 2021, 100, 753–779. [CrossRef] 19. Barratt, J.; Floege, J. SGLT-2 inhibition in IgA nephropathy: The new standard of care? Kidney Int. 2021, 100, 24–26. [CrossRef] [PubMed]
20. Kidney Disease: Improving Global Outcomes Glomerular Diseases Work Group. KDIGO 2021 kliniska riktlinjer för hantering av glomerulära sjukdomar. Kidney Int. 2021, 100, S1–S276. [CrossRef] [PubMed]
21. Keri, KC; Blumenthal, S.; Kulkarni, V.; Beck, L.; Chongkrairatanakul, T. Primär membranös nefropati: omfattande genomgång och historiskt perspektiv. Postgrad. Med. J. 2019, 95, 23–31. [CrossRef]
22. Heymann, W.; Hackel, DB; Harwood, S.; Wilson, SG; Hunter, JL Produktion av nefrotiskt syndrom hos råttor av Freunds adjuvans och råttnjursuspensioner. Proc. Soc. Exp. Biol. Medicin. Soc. Exp. Biol. Med. 1959, 100, 660–664. [CrossRef]
23. Farquhar, MG; Saito, A.; Kerjaschki, D.; Orlando, RA Heymann nefrit antigena komplex: Megalin (gp330) och RAP. J. Am. Soc. Nephrol. JASN 1995, 6, 35–47. [CrossRef]
24. Cybulsky, AV; Quigg, RJ; Salant, DJ Experimentell membranös nefropati redux. Am. J. Physiol. Ren. Physiol. 2005, 289, F660–F671. [CrossRef]
25. Ma, H.; Sandor, GD; Beck, LH, Jr. Rollen av komplement i membranös nefropati. Semin. Nephrol. 2013, 33, 531–542. [CrossRef] [PubMed]
26. Miwa, T.; Song, WC Membrane komplement regulatoriska proteiner: Insikt från djurstudier och relevans för mänskliga sjukdomar. Int. Immunopharmacol. 2001, 1, 445–459. [CrossRef] [PubMed]
27. Bao, L.; Spiller, OB; St John, PL; Haas, M.; Hack, BK; Ren, G.; Cunningham, PN; Doshi, M.; Abrahamson, DR; Morgan, BP; et al. Uttryck av sönderfallsaccelererande faktor i råttnjuren är begränsat till den apikala ytan av podocyter. Kidney Int. 2002, 62, 2010–2021. [CrossRef]
28. Detsika, MG; Goudevenou, K.; Geurts, AM; Gakiopoulou, H.; Grapsa, E.; Lianos, EA Generering av en ny förfallsaccelererande faktor (DAF) knock-out råttmodell med klustrade, regelbundet mellanrum korta palindromiska upprepningar, (CRISPR)/associerat protein 9 (Cas9), genomredigering. Transgenic Res. 2021, 30, 11–21. [CrossRef] [PubMed]
29. Wu, CC; Lu, KC; Lin, GJ; Hsieh, HY; Chu, P.; Lin, SH; Sytwu, HK Melatonin förstärker endogent hemoxygenas-1 och undertrycker immunsvar för att förbättra experimentell murin membranös nefropati. J. Pineal Res. 2012, 52, 460–469. [CrossRef]
30. Yu, P.; Zhang, X.; Liu, N.; Tang, L.; Peng, C.; Chen, X. Pyroptosis: Mekanismer och sjukdomar. Signalöverföring. Mål. Ther. 2021, 6, 128. [CrossRef]
31. Wang, H.; Lv, D.; Jiang, S.; Hou, Q.; Zhang, L.; Li, S.; Zhu, X.; Xu, X; Wen, J.; Zeng, C.; et al. Komplement inducerar podocytpyroptos vid membranös nefropati genom att förmedla mitokondriell dysfunktion. Celldöd Dis. 2022, 13, 281. [CrossRef]
32. Shi, J.; Zhao, Y.; Wang, K.; Shi, X.; Wang, Y.; Huang, H.; Zhuang, Y.; Cai, T.; Wang, F.; Shao, F. Klyvning av GSDMD genom inflammatoriska kaspaser bestämmer pyroptotisk celldöd. Naturen 2015, 526, 660–665. [CrossRef]
33. Fu, L.; Zhang, DX; Zhang, LM; Song, YC; Liu, FH; Li, Y.; Wang, XP; Zheng, WC; Wang, XD; Gui, CX; et al. Exogen kolmonoxid skyddar mot mitokondriell DNA-inducerad hippocampus pyroptos i en modell av hemorragisk chock och återupplivning. Int. J. Mol. Med. 2020, 45, 1176–1186. [CrossRef]
34. Ryter, SW Heme Oxgenase-1, en kardinalmodulator av reglerad celldöd och inflammation. Cells 2021, 10, 515. [CrossRef]
35. Nakatani, Y.; Inagi, R. Epigenetisk reglering genom SIRT1 i podocyter. Curr. Hypertens. Upps. 2016, 12, 89–94. [CrossRef] [PubMed]
36. Chen, XJ; Wu, WJ; Zhou, Q.; Jie, JP; Chen, X.; Wang, F.; Gong, XH Avancerade glykeringsslutprodukter inducerar oxidativ stress genom Sirt1/Nrf2-axeln genom att interagera med AGE-receptorn under diabetiska tillstånd. J. Cell. Biochem. 2018. [CrossRef] [PubMed]
37. Diao, C.; Chen, Z.; Qiu, T.; Liu, H.; Yang, Y.; Liu, X.; Wu, J.; Wang, L. Inhibering av PRMT5 dämpar oxidativ stress-inducerad pyroptos via aktivering av Nrf2/HO-1-signalvägen i en musmodell av njurischemi-reperfusionsskada. Oxidativ Med. Cell. Longev. 2019, 2019, 2345658. [CrossRef] [PubMed]
38. Kim, H.; Ronai, ZA PRMT5 funktion och målinriktning i cancer. Cell Stress 2020, 4, 199–215. [CrossRef]
39. Fernandez-Juarez, G.; Rojas-Rivera, J.; Logt, AV; Justino, J.; Sevillano, A.; Caravaca-Fontan, F.; Avila, A.; Rabasco, C.; Cabello, V.; Varela, A.; et al. STARMEN-studien indikerar att alternerande behandling med kortikosteroider och cyklofosfamid är överlägsen sekventiell behandling med takrolimus och rituximab vid primär membranös nefropati. Kidney Int. 2021, 99, 986–998. [CrossRef]
Virginia Athanassiadou 1 , Stella Plavoukou 1 , Eirini Grapsa 1 och Maria G. Detsika 2,
1. Department of Nephrology, School of Medicine, National and Kapodistrian University of Athens, Aretaieion University Hospital, 11528 Athens, Grekland
2. 1st Department of Critical Care Medicine & Pulmonary Services, GP Livanos och M Simou Laboratories, Evangelismos Hospital, National and Kapodistrian University of Athens, 10675 Athens, Grekland






