Sidt2 är ett nyckelprotein i den autofagi-lysosomala nedbrytningsvägen och är avgörande för upprätthållande av njurstruktur och filtreringsfunktion
Nov 07, 2023
Regleringen och homeostasen av autofagi är avgörande för att upprätthålla organmorfologi och funktion. Som ett lysosomalt membranprotein, effekten avSidt2pånjurstrukturochnjurautofagiär fortfarande okänd. I denna studie fann vi att njurarna avSidt2−/−möss visade förändringar i basalmembranförtjockning, fotprocessfusion och mitokondriell svullnad, vilket tyder på attstrukturen i njuren skadades. Ökat urinprotein vid 24 timmar indikerade attnjurfunktionskadades också. Samtidigt är frånvaron avSidt2orsakade en minskning av antalet sura lysosomer, en minskning av sur hydrolasaktivitet och uttryck i lysosomen, och en ökning av pH i lysosomen, vilket tyder på att lysosomfunktionen var försämrad efterSidt2radering. Ackumuleringen av autofagolysosomer, ökade LC3-II- och P62-proteinnivåer och minskade P62-mRNA-nivåer tydde på att frånvaron avSidt2genen orsakade onormal autofagivägflaj. Klorokinexperiment, immunofluorescensautofagosom, lysosomfusionsanalys och Ad-mcherry-GFP-LC3B indikerade vidare att efterSidt2deletion ökade inte produktionen av autofagosomer, men sammansmältningen av autofagosomer och lysosomer och nedbrytningen av autofagolysosomer försämrades. Vid ruvningSidt2−/−celler med autofagiaktivatorn rapamycin, fann vi att det kunde aktivera autofagi, vilket manifesterade sig som en ökning av autofagosomer, men det kunde inte förbättra autofagolysosomnedbrytningen. Samtidigt illustrerade det ytterligare attSidt2genen spelar en viktig roll i den smidiga utvecklingen av autofagolysosomprocesser. Sammanfattningsvis, frånvaron avSidt2genen orsakade försämrad lysosomfunktion och ett minskat antal sura lysosomer, vilket ledde till bildandet och nedbrytningsrubbningarna av autofagolysosomer, som så småningom manifesterade sig somonormal njurstruktur och funktion. Sidt2är avgörande för att upprätthålla lysosomernas normala funktion och njurarnas fysiologiska stabilitet.

INTRODUKTION
Den traditionella uppfattningen är att lysosomer är cellernas sophantering för att ta bort avfall som produceras av celler [1–3]. Men många studier har visat att lysosomernas roll är mycket mer komplex och kan involvera cellsignaltransduktion, tumörbildning, utveckling och andra aspekter som påverkar kroppens livsaktiviteter [4–10]. Lysosomer anrikas vanligtvis i vävnader som lever och njure [11]. Därför är lysosomal dysfunktion också nära besläktad med vävnadssjukdomar i lever och njure, såsom Gauchers sjukdom [12], mukopolysackaridos [13], Niemann-Picks sjukdom [14], fördröjd glomeruloskleros [15], idiopatisk membranös nefropati [16] , etc. Lysosomala membranproteiner (LMP) är membrankomponenterna vars funktion inte bara är att upprätthålla lysosomens integritet utan som också är involverade i olika aspekter såsom intracellulär signaltransduktion och reglering som är väsentliga för att upprätthålla lysosomens funktion och celllivsaktiviteter [17–19].
Hittills har mer än 100 LMP upptäckts, men funktionerna för de flesta av dem är fortfarande okända [20]. Transmembran 7 superfamiljmedlem 1 (TM7SF1) är avgörande för upprätthållandet av njurens podocytfunktion [21] och spelar en viktig roll i processen för njurutveckling [22]. Chloride Voltage-Gated Channel 5 (ClC-5) är en kloridjonkanal (Cl(−)) uttryckt i njurtubuli, vilket är avgörande för normal njurfunktion [23]; när den är muterad kan den orsaka Dents sjukdom [24]. Överuttryck av Chloride Voltage-Gated Channel 7 (ClC-7) förhindrar apoptos av renala tubulära epitelceller orsakad av nedsatt redoxtillstånd [25]. Dessa studier visar att LMP, som komponenter i lysosomberikad njurvävnad, är väsentliga för att upprätthålla normal funktion, men den specifika mekanismen för deras relaterade patogenicitet är fortfarande oklar.
SID1 transmembranfamiljen, medlem 2 (Sidt2) är en nyupptäckt LMP som är starkt uttryckt i lever- och njurvävnader [26]. Tidigare studier har visat att Sidt2-deletion kan orsaka leverrelaterade sjukdomar, som visar sig som leversteatos och leverfettomsättningsstörningar [11, 18]. I en nyligen genomförd studie fann vi att njurarna hos Sidt2−/−möss också upplevde skada, men den specifika mekanismen är oklar. Lysosomer är viktiga verkställande organ för autofagi [10]. Är autofagireglering inblandad? I denna studie undersökte vi korrelationen mellan lysosomal funktion (autofagi) och sjukdom och utforskade den underliggande mekanismen som involverar Sidt2 som orsakar njurskador, vilket kommer att vara till stor hjälp för studiet av korrelationen mellan LMP och sjukdom.

RESULTAT
Sidt2−/− modellen visar detnjurskadaär förknippat med autofagolysosomackumulering
Metoden för att konstruera Sidt2−/− möss visas i Fig. 1A. Det erhållna homozygota mussvans-DNA:t sekvenserades och sekvenseringsresultatet var unimodalt (Fig. IB), och en 199 bp fragmentförlust inträffade i det andra exonet. Genom PCR-genotypidentifiering fann vi att Sidt2+/+(Wild Type, WT) möss hade 685 bp DNA-segment, medan Sidt2-/− möss hade 486 bp (Fig. 1C). Som visas i Fig. 1D kunde Sidt2-proteinet knappast detekteras i Sidt2−/− möss än i WT, vilket antydde att modellen konstruerades framgångsrikt. Genom urintest fann man att 24 timmars urinprotein ökade signifikant i Sidt2−/− möss jämfört med WT (Fig. 1E), vilket tyder på att njurfiltreringsbarriären försämrades efter att Sidt2 raderades. Transmissionselektronmikroskopiobservationer (Fig. 1F) visade att, jämfört med WT-möss (a–f), Sidt2−/− musnjurar uppvisade diffus fusion av fotprocesser, förtjockning av det glomerulära basalmembranet (g, h), renalt tubulärt epitel. cellödem, skador på mikrovilli (i, j), mitokondrieödem, vakuolliknande förändringar och försvinnande av ryggar (k, l). Intressant nog har Sidt2−/− möss också uppvisat ett stort antal autofagolysosomansamlingar (visas med röda pilar, m, n), och antalet var betydligt högre än för kontrollen (Fig. 1G). På cellnivå fann vi att Sidt2 också var avgörande för överlevnaden av njurceller. Borttagningen av Sidt2-genen orsakar minskad proliferation och ökad apoptos av MPC5- och SV40 MES 13-celler (kompletterande fig. 1).
Sidt2-gendeletion leder till förändringar i antalet och funktionen av sura lysosomer i musnjurceller
Crispr-Cas9-teknologin användes för att slå ut Sidt2-genen i MPC5- och SV40 MES 13-celler för att erhålla cellmodellerna. MRNA- och proteinnivåverifieringarna (Fig. 2A-C) utfördes med qRT PCR respektive western blotting, vilket visar att modellerna konstruerades framgångsrikt. Det lysosommedierade nedbrytningssystemet är ett nyckelsteg i nedbrytning av autofagi. Som en oumbärlig LMP, kommer knockouten av Sidt2 att påverka uttrycket av lysosomrelaterade proteiner? Vi mätte det huvudsakliga LMP-lysosomalassocierade membranproteinet 1 (LAMP1). Resultaten visade att uttrycket av LAMP1 minskade efter Sidt2-deletion i MPC5- och SV40 MES 13-celler (Fig. 2D, E). Vi använde vidare LysoTracker för att märka de sura lysosomerna och fann att antalet sura lysosomer minskade efter Sidt2-deletionen i båda typerna av celler (Fig. 2F, G). Därefter mätte vi det lysosomala katepsin B (CTSB) och fann att i musnjurvävnad (Fig. 2H, I), MPC5-celler (Fig. 2J, K) och SV40 MES 13-celler (Fig. 2L, M), uttrycken av CTSB i Sidt2−/−-modellerna reducerades alla, vilket tyder på att den proteolytiska enzymaktiviteten i lysosomerna minskade när Sidt2-genen raderades. På liknande sätt reducerades uttrycket av prekursorn CTSB i de två typerna av celler i Sidt2−/−-gruppen signifikant, vilket tyder på att CTSB också påverkades efter Sidt2-deletion. Vi använde vidare LysoSensor för att detektera den sura miljön i lysosomerna. Ju lägre fluorescensintensitetsförhållande desto högre pH-värde i lysosomen. Resultaten visade att efter Sidt2-deletion ökade pH-värdet (Fig. 2N, O) och försurningen var onormal. För att ytterligare undersöka om ovanstående lysosomala abnormiteter berodde på onormalt antal lysosomer eller onormala lysosomala funktioner, undersökte vi cellerna med elektronmikroskopi (Fig. 2P). Vi fann att det inte finns några uppenbara förändringar i antalet primära lysosomer och det totala antalet lysosomer (inklusive primära och sekundära lysosomer) efter Sidt2-deletion (Fig. 2Q).

Den renala autofagivägen är onormal efter Sidt2-borttagning
Som nämnts ovan observerades ett stort antal autofagolysosomansamlingar i njurcellerna hos Sidt2−/− möss, vilket tyder på att autofagivägen var onormal. Med hjälp av western blot-analys visades det att det fanns en signifikant ökning av proteinnivån av LC3-fosfatidyletanolaminkonjugat (LC3-II) och Sequestosome 1(P62) i njuren av Sidt2−/− möss, och en ökning av autofagi-relaterade proteinuttryck av Autophagy-relaterad 5(Atg5), Autophagy-relaterad 7(Atg7) och Autophagy-relaterad 12(Atg12) (Fig. 3A, B). Men P62-mRNA-nivån minskade signifikant (Fig. 3C), vilket tyder på att autofagivägen var onormal efter elimineringen av Sidt2 in vivo. Sedan fann vi att uttrycken av autofagiproteinerna LC3-II, P62, Atg5, Atg7 och Atg12 också ökade (Fig. 3D–G) i de två typerna av njurceller efter Sidt2-deletion, vilket var konsekvent med in vivo. Ökningen av LC3-II indikerade en ökning av autofagosomer i njurcellerna efter Sidt2-deletion, vilket kan orsakas av aktivering av autofagi eller blockerad nedbrytning av autofagosomer. P62-immunfluorescens (Fig. 3H) visade tydligt en ökning av P62-innehållet i Sidt2−/−-cellerna (Fig. 3I). I motsats till proteinnivån visade qRT-PCR att P62 minskade signifikant på mRNA-nivån (Fig. 3J), vilket indikerar att ökningen av P62 var relaterad till otillräcklig nedbrytning. Ökningen av Atg5, Atg7 och Atg12 indikerade att autofagi började och bildades normalt, men ackumuleringen av P62 antydde också hinder för autofagiprocessen, och denna motsägelse krävde att vi ytterligare utforskade den verkliga situationen för autofagiflöde.
In vitro indikerar klorokinapplikation minskat autofagiflöde efter Sidt2-förlust. Klorokinexperimentet är ett av de klassiska experimenten för att observera autofagiflöde. För att förstå orsakerna till ökningarna av LC3-II och P62 efter Sidt2-deletion använde vi klorokin (CQ), en nedströmshämmare av autofagi, för att verka på cellerna för att observera autofagiflödet. Först använde vi olika koncentrationsgradienter för att bekräfta att mättnadskoncentrationen som hämmades av CQ var 50 μM (Fig. 4A–F) i MPC5- och SV40 MES 13-cellerna. Utöver denna koncentration, när CQ-koncentrationen fortsatte att öka, ökade inte LC3-II och P62 ytterligare för att nå mättnad. Därför använde vi 50 μM CQ-stimulering under 16 timmar för att fullständigt hämma autofagiflödet, och vid denna tidpunkt försvann LC3-II-skillnaderna mellan Sidt2+/+-gruppen och Sidt2-/−-gruppen i MPC5- och SV40 MES 13-cellerna. På samma sätt, efter 50 μM CQ-bearbetning, försvann P62-skillnaderna orsakade av raderingen av Sidt2 också (Fig. 4G, H, J, K). Statistiken om autofagiflöde visade att det minskade när Sidt2 saknades (Fig. 4I, L), vilket ytterligare bekräftade att ökningarna i LC3-II- och P62-uttryck efter Sidt2-deletionen berodde på misslyckande med autofagi-clearing snarare än ökningen av nivån i autofagi (aktiveringen av autofagi).
Avbrott i autofagosom-lysosomfusion in vitro efter Sidt2-deletion Clearance och nedbrytning är de mellersta och sena stadierna i autofagiprocessen, som involverar fusionen av autofagosomen med minskad efter deletionen av Sidt2 (fig. 5D), vilket indikerar att fusionen av autofagosomer och lysosomer var försämrade.
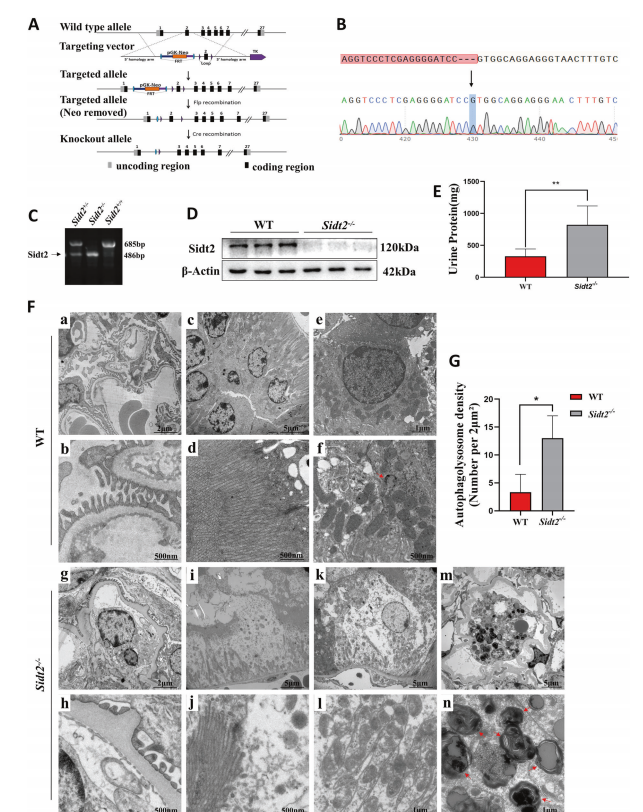
figur 1Njurskadoroch autofagolysosomackumulering i Sidt2−/− möss. Ett schematiskt schema för målsökning av Cre-LoxP-systemets gen; B ovan är det exporterade sekvensdiagrammet för Sidt2-genen knockout-mussvans-DNA; nedan är sekvenskartan, pilen som indikerar platsen för den saknade genen. Jämfört med WT-möss inträffar en genförlust på 199 bp i exon 2; C DNA-nivåverifiering av Sidt2 (extraherad från svansvävnad). Den primerförstärkta produkten innehåller basens knockout-region, visad som Sidt2+ /+(WT), Sidt2+/− eller Sidt2−/−; D-proteinnivåverifiering för att detektera Sidt2-proteinuttrycksnivåer genom western blöt; E njure 24 h urinprotein i WT och Sidt2−/− möss; F ultramikromorfologisk struktur av njurarna hos WT-möss (a, f) och Sidt2−/−-möss (g–n). Jämfört med WT-musen uppvisar Sidt2−/− musnjuren fotprocessfusion, basalmembranförtjockning (g, h), renalt tubulärt epitelcellsödem, skador på mikrovilli (i, j), mitokondriell destruktion (k, l) och autofagolysosomackumulering (m, n); G totalt antal renala autofagolysosomer i WT- och Sidt2−/−-möss. *P < 0.05, **P < 0,01.
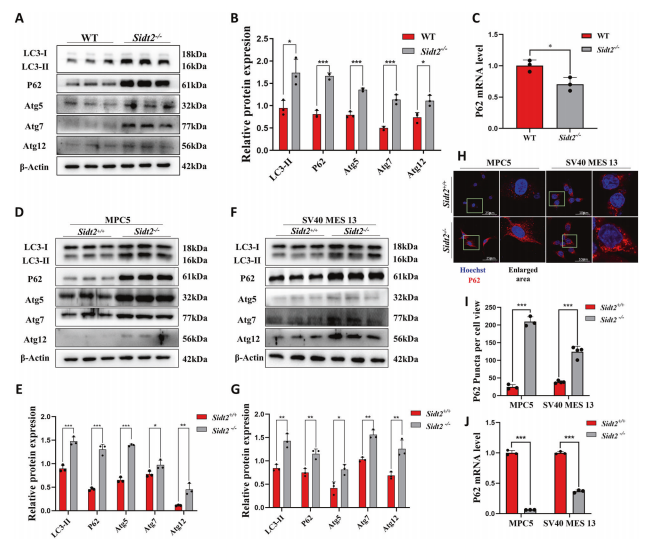
Fig. 3 Sidt2-deletion stör autofagivägen. En Detektion av WT och Sidt2−/− cell autofagi-relaterade proteinuttrycksnivåer genom western blöt; B statistiska diagram över Western blot-testresultaten; C P62 mRNA-uttrycksnivå i njurvävnad hos WT- och Sidt2−/−-möss; D-expressionsnivåer av MPC5-cellautofagivägsproteiner före och efter Sidt2 knockout; E statistisk graf av (D) diagram; F-uttrycksnivåer av proteiner i autofagivägar i SV40 MES 13-celler före och efter Sidt2 knockout; G statistiskt diagram över (F) diagrammet; H P62-immunfluorescens i MPC5- och SV4-0 MES 13-celler före och efter Sidt2-knockout; I statistiska diagram över immunofluorescensresultaten; J P62 mRNA-expressionsnivåer i MPC5- och SV40 MES 13-celler före och efter Sidt2-knockout. *P < 0,05, **P < 0,01, ***P < 0,001.

Ad-mCherry-GFP-
Dubbelmärkning av LC3B-fluorescens tyder på att autofagolysosombildning och dess nedbrytningsväg blockerades efter Sidt2-deletion. Ad-mCherry-GFP-LC3B-transfektionsexperimentet kan användas för att detektera förändringar i dynamiskt autofagiflöde i celler. Under autofagiprocessen samlas mCherry-GFP-LC3B på autofagosommembranet och manifesterar sig i form av gula fläckar under ett fluorescensmikroskop. När autofagosomer och lysosomer smälts samman för att bilda autofagolysosomer, kommer den sura miljön i lysosomen att släcka fluorescensen av GFP så att den manifesterar sig i form av röda fläckar. Därför kan GFP bundet till LC3 endast användas för att detektera autofagosomer, medan mCherry kan upptäcka autofagosomer och autofagolysosomer samtidigt. När de gröna och röda fluorescensfläckarna kombineras och visas som gula fluorescensfläckar, motsvarar detta autofagosomer. Vid denna tidpunkt kan den röda fluorescensen indikera autofagolysosomer, och det kan också indikera jämnheten av autofagolysosombildning [27]. MPC5-celler och SV40 MES 13-celler i både Sidt2+/+- och Sidt2−/−-grupperna transfekterades med Ad-mCherry GFP-LC3B-adenovirus och fotograferades med ett konfokalt lasermikroskop (Fig. 6A). Det visade sig att antalet gula fluorescerande prickar ökade och antalet röda fluorescerande prickar minskade (Fig. 6B, C) efter Sidt2-deletion, vilket visade att antalet autofagosomer ökade och autofagolysosomerna minskade i Sidt2−/−-gruppen. Detta beror på att det fanns hinder för bildandet av autofagolysosom, och autofagolysosomnedbrytningsvägarna blockerades, vilket ledde till hinder för autofagosomnedbrytning.

Rapamycin förbättrade inte P62-ackumuleringen orsakad av Sidt2-deletion utan förvärrade den snarare. Rapamycin (RAPA) är en hämmare av mTOR och aktiverar autofagi. När RAPA verkade på MPC5- och SV40 MES 13-celler i Sidt2+/+- och Sidt2−/−-grupperna, ökade det mängderna LC3-II i båda grupperna. Detta innebar att RAPA kunde aktivera uppströmsvägen för autofagi. På liknande sätt fann vi att ökningen av LC3-II-nivån i Sidt2−/−-gruppen med RAPA var mer uppenbar än den i kontrollen (Sidt2+/+gruppen), vilket visade att när RAPA agerade på Sidt2−/−-gruppen förbättrades fortfarande inte nedbrytningen av autofagosomer. Samtidigt observerade vi också förändringarna i P62 och fann att när RAPA verkade på Sidt2+/+-gruppen av MPC5- och SV40 MES 13-celler, förändrades P62 inte signifikant, vilket tyder på att autofagiflödet var normalt. När RAPA verkade på Sidt2−/−-gruppen ökade uttrycksnivån av P62 ytterligare jämfört med den före administrering och var också mer uppenbar än den i kontrollen efter RAPA-behandling (Fig. 7A, B, D, E). Därefter, för att undersöka orsakerna till det inkonsekventa uttrycket av P62-protein efter att Sidt2+/+- och Sidt2−/−-gruppen behandlats med RAPA, mätte vi mRNA-nivåerna av P62 och fann att nivån ökade efter RAPA-behandling i både Sidt2+/+- och Sidt2−/−-grupperna och Sidt2+/+-gruppen hade en högre nivå än i Sidt2−/−-gruppen (Fig. 7C , F), vilket ytterligare skulle kunna bevisa att autofagiflödet var jämnt i Sidt2+/+-gruppen, medan autofagiflödesstörningen inträffade i slutet av autofagi i Sidt2−/−-gruppen, det vill säga nedbrytningen av autofagolysosomer länk. Vi studerade också effekten av Sidt2 på proliferation och apoptos av njurceller under tillstånd av aktiverad autofagi och fann att efter serumfri mediuminducerad cellaktivering av autofagi, jämfört med kontrollgruppen, proliferationen av Sidt2−/− gruppen hämmades ytterligare och apoptosen var mer uppenbar (kompletterande fig. 2).
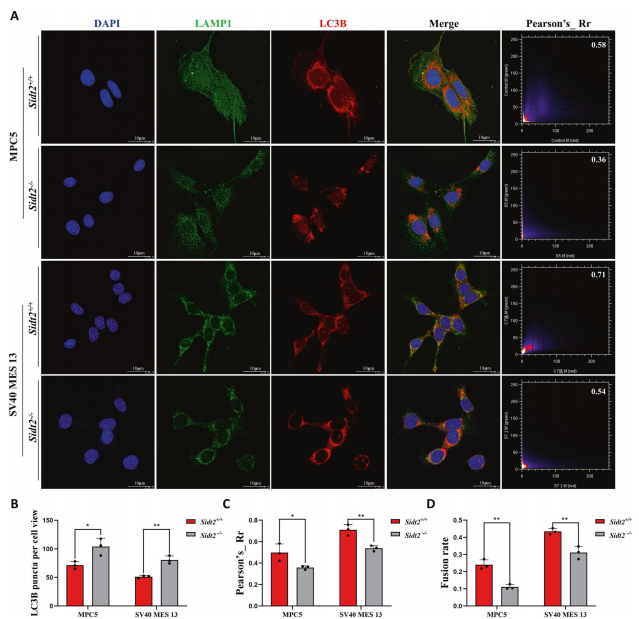
Fig. 5 Autofagosom- och lysosomfusion förhindras efter Sidt2-deletion. En immunfluorescenssamlokalisering av LC3B och LAMP1 i MPC5- och SV40 MES 13-celler före och efter Sidt2-knockout, analys med Pearsons korrelationskoefficient; B-jämförelse av LC3B-fluorescenspunkter före och efter Sidt2-knockout i MPC5- och SV40 MES 13-celler; C jämförelse av Pearsons korrelationskoefficient före och efter Sidt2 knockout i MPC5 och SV40 MES 13 celler; D jämförelse av fusionshastigheten före och efter Sidt2 knockout i MPC5 och SV40 MES 13-celler (förhållandet mellan antalet samlokaliserade fluorescerande fläckar av LAMP1 och LC3B och antalet fluorescerande fläckar av LAMP1); *P < 0,05, **P < 0,01.
Supportive Service Of Wecistanche - Den största cistanche-exportören i Kina:
E-post:wallence.suen@wecistanche.com
Whatsapp/Tel:+86 15292862950
Handla för fler specifikationer:
https://www.xjcistanche.com/cistanche-shop






